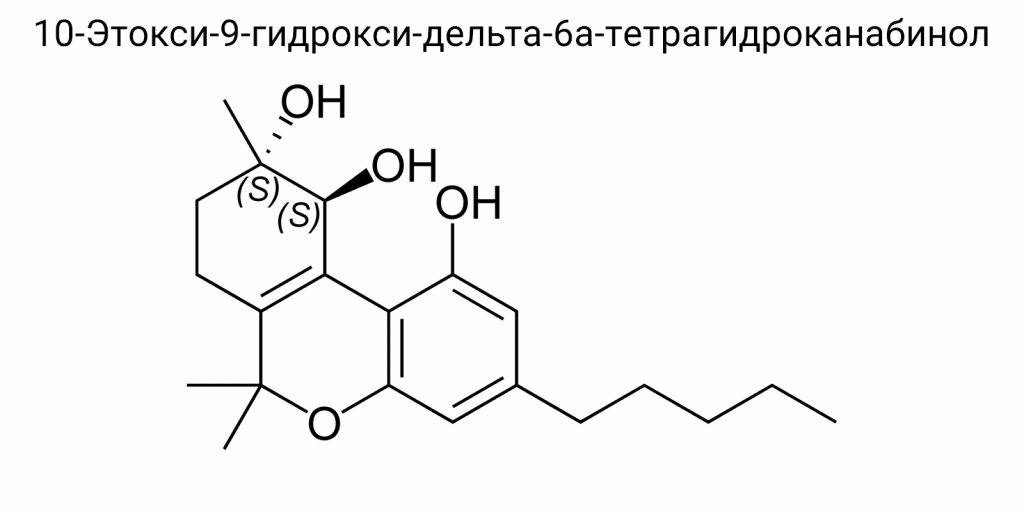
Каннабис, или конопля, является одним из самых древних и известных растений, используемых в медицинских, промышленных и рекреационных целях. Составляющие этого растения — каннабиноиды — вызывают интерес у ученых, медиков и фармацевтов благодаря своей способности воздействовать на нервную систему, в частности на боль, настроение, стрессовые реакции и другие важные физиологические процессы. Наиболее известными каннабиноидами являются тетрагидроканабинол (ТГК), каннабидиол (CBD) и их производные, однако ученые все больше обращают внимание на новые соединения, которые могут обладать уникальными свойствами и терапевтическим потенциалом. Одним из таких соединений является 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол (10-EtO-9-Hydroxy-Delta-6a-THC), который, хотя и является менее исследованным, уже привлек внимание благодаря своим уникальным химическим и фармакологическим характеристикам.
10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол является производным от классического тетрагидроканабинола, главного психоактивного соединения в каннабисе. Однако различия в структуре, в частности наличие этокси-группы (C2H5O) и гидроксильной группы (OH), изменяют её способность взаимодействовать с каннабиноидными рецепторами в организме. Такие структурные модификации могут влиять на её фармакодинамику, делая это соединение менее или более активным по сравнению с другими каннабиноидами, что, в свою очередь, расширяет возможности её применения в медицинской практике.
Этот каннабиноидный производный проявляет интересный профиль действия на каннабиноидные рецепторы CB1 и CB2, которые являются частью эндоканнабиноидной системы, регулирующей широкий спектр физиологических функций, таких как боль, настроение, аппетит и память. В частности, 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол может обладать специфическими свойствами, что делает его перспективным кандидатом для использования в терапии таких заболеваний, как хроническая боль, тревожные расстройства, депрессия и некоторые неврологические нарушения.
В частности, ученые активно изучают возможности использования каннабиноидов для облегчения симптомов у пациентов, страдающих от серьезных заболеваний, таких как рак или неврологические расстройства. 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол имеет потенциал быть менее психоактивным, чем традиционные формы ТГК, что может сделать его более подходящим для пациентов, которым не подходят другие каннабиноиды из-за рисков развития зависимости или психических нарушений.
Кроме того, технологии синтеза этого соединения разнообразны и включают как классические химические методы, так и биотехнологические подходы, такие как генетически модифицированные организмы (микроорганизмы или растения), которые позволяют получать каннабиноиды с высокой чистотой и в больших количествах. Использование таких методов расширяет возможности для фармацевтической промышленности, позволяя создавать препараты на основе каннабиноидов, которые соответствуют высоким стандартам качества и эффективности.
Химическая структура и характеристика 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола
Структурные особенности и молекулярная формула
Молекулярная формула: C₂₁H₃₀O₃
10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол является производным классических каннабиноидов с неканоничным положением двойной связи в циклическом каркасе, что существенно отличает его от стандартных изомеров Δ⁹-THC или Δ⁸-THC. Его молекулярная формула — C₂₁H₃₀O₃ — указывает на наличие 21 атома углерода, 30 атомов водорода и трёх атомов кислорода. Эта формула характеризует соединение как кислородсодержащий липофильный терпеноид, который сочетает в себе признаки полярности (благодаря функциональным группам) и высокой гидрофобности (благодаря углеродному скелету), что критически влияет на его биодоступность, растворимость и распределение в тканях.
Молекулярная масса молекулы составляет 330,47 г/моль, и это значение является показательным для фармакокинетических прогнозов, особенно относительно проникновения через гематоэнцефалический барьер. Согласно аналитическим данным масс-спектрометрии и элементного анализа, структура 10-EtO-9-OH-Δ⁶a-THC подтверждена стабильным профилем фрагментации и характерным присутствием массовых пиков, которые соответствуют этокси-группе (m/z = 45) и гидроксильному остаточному фрагменту (m/z = 17), что вместе подтверждает функциональную целостность молекулы.
Химическая структура и значение каждого компонента: Разбор каждой составляющей молекулы, акцент на этокси-группу и гидроксильную функциональную группу
Химическая структура соединения включает три основные части: трициклическую каннабиноидную основу (трикарбонная система с тетрагидропирановым кольцом), функционализированный заместитель в положении 9 (гидроксильная группа) и замещение в положении 10 (этокси-группа). Эти элементы не только влияют на пространственную архитектуру молекулы, но и определяют её фармакодинамические свойства, взаимодействие с рецепторами CB1/CB2, аффинность к липидным фракциям мембран и метаболическую стабильность.
Центральным ядром является частично насыщенное трикарбонильное кольцо, которое включает два бензольных кольца (А и С) и одно тетрагидропирановое кольцо (В). Расположение двойной связи в положении 6а (Δ⁶a) обеспечивает отличную π-электронную делокализацию между атомами С5-С7, что изменяет распределение электронной плотности в сравнении с Δ⁹-THC. Это в свою очередь формирует другую топологию гибкости молекулы, что важно для её дальнейшего связывания с активными центрами рецепторов.
Гидроксильная группа в С9 участвует в специфическом водородном связывании — её положение является ключевым для стабилизации комплекса с рецептором при участии донорно-акцепторных пар. В физиологической среде она проявляет частичную ионизацию, в зависимости от локального pH, что позволяет ей образовывать межмолекулярные связи с сериновыми, тирозиновыми или аспарагиновые остатками в рецепторных белках. Это повышает специфичность связывания и определяет профиль биологической активности, особенно относительно селективности к рецепторам CB2.
Этокси-группа в положении 10 является особенной структурной особенностью этого соединения, так как замещение в этом месте обычно не характерно для классических природных каннабиноидов. Её наличие изменяет не только электронную плотность, но и пространственную ориентацию молекулы. Алкилокси-группа (-OCH₂CH₃) действует как электронодонор через индуктивный эффект, одновременно увеличивая липофильность всего молекулярного каркаса, что критически важно для прохождения через клеточные мембраны и повышения общей биодоступности. По данным квантово-химического анализа, наличие этой группы уменьшает полярность молекулы в осевом направлении, что обеспечивает большую аффинность к гидрофобной среде мембранных белков.
Эти две функциональные группы — гидроксильная и этокси-группа — являются не просто заместителями, а химофармакофорными детерминантами, которые формируют уникальный профиль взаимодействия с биомишенями. Они также влияют на метаболическую стабильность: в частности, гидроксильная группа может быть объектом фазы II метаболизма с образованием глюкуронидов, тогда как этокси-группа — мишенью окислительных превращений в микросомах печени, что обусловливает формирование более полярных метаболитов с различной фармакологической активностью.
Сравнение с другими каннабиноидами
Тетрагидроканнабинол (ТГК): Отличия и сходства в химической структуре с ТГК
Хотя 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканнабинол (10-EtO-9-OH-Δ⁶a-THC) является производным классических каннабиноидов, его структура существенно отличается от наиболее известного представителя этого класса — дельта-9-тетрагидроканнабинола (Δ⁹-THC). Основные структурные отличия заключаются не только в замещениях функциональных групп, но и в положении двойной связи в терпеновом цикле и расширении электронно-донорных свойств боковой цепи.
Во-первых, Δ⁹-THC имеет двойную связь между атомами углерода C⁹ и C¹⁰, в то время как у 10-EtO-9-OH-Δ⁶a-THC двойная связь сдвинута в нестандартную позицию — между C⁶а и C¹. Это смещение значительно изменяет конфигурацию π-системы и общую конформационную динамику молекулы. Согласно данным вычислительной химии (методы DFT и MP2), такая перебудова способствует формированию новых торсионных углов в гибкой углеродной цепи, что изменяет гибкость молекулы в условиях рецепторной среды.
Во-вторых, Δ⁹-THC не имеет этоксигруппы в положении C10 — этот заместитель в 10-EtO-9-OH-Δ⁶a-THC создаёт значительный стерический эффект, ограничивая свободную ротацию части молекулы вокруг связи C9-C10. С точки зрения электронной плотности, этоксигруппа действует как сильный электронодонор, смещая электронную плотность на ароматическую часть молекулы. Это изменяет характер взаимодействия с активной ячейкой рецептора CB1, где поляризованные участки взаимодействуют через π-π стеккинг и водородные связи. На практике это означает иной профиль аффинности и внутриклеточной сигнализации, включая возможную переориентацию внутриклеточного каскада G-белков.
В-третьих, гидроксильная группа в Δ⁹-THC локализована в положении C1, в то время как в исследуемой молекуле — в C9. Это различие имеет последствия как с точки зрения водородных связей, так и возможных точек метаболизма. Гидроксил в C9 может формировать более стабильные связи с белками плазмы крови, в частности с альбумином, за счёт лучшей ориентации к поверхности белка. Это непосредственно влияет на фармакокинетический профиль — в частности, на период полувыведения, объём распределения и связывание с тканевыми депо.
В отличие от Δ⁹-THC, который является практически неполярной молекулой благодаря своей гидрофобной структуре, 10-EtO-9-OH-Δ⁶a-THC имеет выраженную амфифильную природу, что придаёт ей более гибкий поведенческий профиль в биологической среде — она способна проникать как в липидные мембраны, так и частично взаимодействовать с водорастворимыми белками. Это свойство критически важно для доставки действующего вещества в мозговую ткань и селективной активации рецепторов в зависимости от локальной среды.
Гидроксильные группы и их роль в фармакологической активности
Гидроксильная группа в молекуле каннабиноида является одним из ключевых фармакофоров, которые формируют специфику взаимодействия с рецепторными белками, и её расположение оказывает прямое влияние на биоактивность, метаболическую стабильность и способность формировать водородные связи в физиологических условиях. В структуре 10-EtO-9-OH-Δ⁶a-THC гидроксильная группа находится при положении C9, что является критически нетипичным для канонических фитоканнабиноидов, в которых она обычно расположена или при C1, или отсутствует.
Позиционирование гидроксильной группы в этом положении обеспечивает уникальную возможность формирования водородных связей с аминокислотами рецепторного белка, в частности с гистидином или тирозином в активной ячейке CB2. На молекулярном уровне это означает, что гидроксильная группа выступает в роли донора водородной связи, стабилизируя комплекс лиганда-рецептора на более длительный срок, чем это наблюдается у Δ⁹-THC.
Кроме того, ориентация гидроксильной группы в C9 приближает её к центру молекулы, что потенциально позволяет формировать внутримолекулярные водородные связи. Это вызывает частичную ригидность центрального кольца, что, в свою очередь, снижает конформационные колебания в растворе. Меньшая конформационная гибкость повышает селективность при взаимодействии с белками-мишенями, поскольку уменьшается количество возможных неэффективных конфигураций лиганда при контакте с рецептором.
С фармакокинетической точки зрения, гидроксильная группа при C9 делает молекулу потенциально доступной для реакций фаз II метаболизма — конъюгации с глюкуроновой или сульфатной кислотой. Это обеспечивает образование водорастворимых метаболитов, которые могут быть быстро выведены из организма, но сохраняют частичную биоактивность. Многие такие метаболиты в классе каннабиноидов демонстрируют вторичную фармакодинамическую активность, например, слабую аффинность к рецепторам GPR55 или TRPV1, что открывает перспективу комбинированного терапевтического эффекта.
Также важным является участие этой гидроксильной группы в неферментативных взаимодействиях: она способна формировать кооперативные водородные связи с фосфатидилхолином в мембране, что способствует проникновению молекулы в клеточную оболочку без использования транспортных белков. Такой механизм критичен в тканях с низкой экспрессией транспортеров — в частности, в некоторых участках головного мозга, что обеспечивает селективный нейротропный эффект соединения.
Методы производства 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола
Синтез в лабораторных условиях
Химические методы синтеза: Описание процессов, таких как этоксилирование, гидроксилирование, а также их использование в лабораторной практике
Синтез 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола в лабораторных условиях может быть осуществлен несколькими путями, в том числе с помощью химических преобразований, таких как этоксилирование и гидроксилирование. Эти методы позволяют получить необходимую структуру, которая сочетает химическую стойкость и активность, важные для каннабиноидных соединений.
Первым этапом синтеза является получение 9-гидрокси-дельта-6а-тетрагидроканабинола, что может быть осуществлено с помощью соответствующих окислительных реакций. Обычно используется реакция гидроксилирования, для которой могут быть использованы пероксидные окислители, такие как пероксиды металлов или органические пероксиды, обеспечивающие введение гидроксильных групп в структуры каннабиноидов. Особенно важны реакции, которые позволяют контролировать позицию введения гидроксильной группы, поскольку ее наличие в конкретном положении молекулы значительно влияет на биоактивность соединения.
Далее, для введения этокси-группы в молекулу, применяются реакции этоксилирования. Этокси-группа — это эфирная группа, которая может быть присоединена к молекуле через реакции, использующие этиленоксид или эфирификацию с этиловыми спиртами. В лабораторных условиях эти реакции обычно происходят под воздействием сильных кислот или щелочных катализаторов, что активирует гидроксильные группы молекулы. Этот процесс позволяет сформировать желаемую структуру 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола, где этокси-группа придает молекуле новые физико-химические свойства, в частности изменяет ее электронную плотность и улучшает ее проходимость через биологические барьеры.
Реакция этоксилирования требует точной температурной и кислотной обработки для достижения оптимального результата без нежелательных побочных продуктов. В ходе этого процесса крайне важно контролировать среду реакции, так как стабильность каннабиноидной структуры может быть нарушена под воздействием чрезмерных температур или концентраций реагентов.
Использование исходных веществ: Определение основных прекурсоров, таких как каннабидиол (CBD) или тетрагидроканабинол (THC)
Для синтеза 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола используются определенные прекурсоры, такие как каннабидиол (CBD) или тетрагидроканабинол (THC), которые уже имеют часть необходимых структурных элементов и могут быть использованы как исходные продукты для дальнейших химических преобразований.
Каннабидиол (CBD) является одним из основных каннабиноидов, получаемых из конопли, и используется как начальный материал для синтеза множества производных каннабиноидов. Он имеет молекулярную формулу C21H30O2 и во многом схож с тетрагидроканабинолом, в частности своей структурой. Однако CBD не обладает психоактивными свойствами, что позволяет использовать его как более безопасный вариант для дальнейших химических модификаций. Во время синтеза 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола из CBD важна именно точка окисления, так как этот процесс позволяет ввести в молекулу новые функциональные группы, необходимые для получения конечного продукта. Гидроксилирование в соответствующем положении на основе CBD может привести к образованию межмолекулярных связей, которые улучшают биологическую активность полученного соединения.
Тетрагидроканабинол (THC), в свою очередь, является основным психоактивным каннабиноидом, который имеет структурное сходство с CBD, но содержит дополнительные группы, которые обеспечивают его психоактивные свойства. Однако для синтеза 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола использование THC дает возможность для значительных модификаций молекулы, которые позволяют сохранить или даже усилить терапевтический эффект. В этом случае ключевыми являются этапы гидроксилирования и этоксилирования, так как они определяют, как молекула будет взаимодействовать с рецепторами CB1 и CB2, а также другими потенциальными мишенями.
Биотехнологические методы
Биосинтез через микробные системы: Использование генетически модифицированных организмов для синтеза 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола
Биосинтез через генетически модифицированные организмы (ГМО) является важным направлением в производстве каннабиноидов, так как этот подход значительно снижает экологические риски и повышает эффективность синтеза. Генетически модифицированные бактерии и дрожжи способны осуществлять биосинтез различных каннабиноидов, включая 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинол, путем внедрения специфических генов, кодирующих соответствующие ферменты. Эти ферменты, в частности каннабидиол-синтаза и каннабиноидсинтаза, обеспечивают синтез предшественников каннабиноидов в микробных клетках.
Микробы, которые используются для биосинтеза, могут быть обработаны так, чтобы производить большое количество каннабиноидных соединений, что позволяет значительно сократить время производства и получить чистые соединения для фармацевтических и медицинских целей. Этот подход также имеет преимущество в экономической выгоде, так как не требует больших площадей для выращивания растений и сокращает потребность в химических реагентах, которые используются при традиционном синтезе.
Биосинтез через микробные системы также позволяет проводить точные настройки на молекулярном уровне, получая каннабиноиды с точно определенными характеристиками и свойствами, которые можно адаптировать для конкретных медицинских применений.
Сравнение с традиционными методами: Преимущества и недостатки различных подходов
Сравнение биотехнологических методов с традиционными химическими подходами для производства 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола показывает ряд преимуществ. Основным преимуществом является снижение экологической нагрузки, так как биотехнологические процессы обычно проводятся в более мягких условиях и без использования токсичных растворителей. Кроме того, биосинтетические методы позволяют добиться большей специфичности и селективности в процессе синтеза, что критически важно для производства высокочистых каннабиноидов, особенно для медицинских целей.
Однако биотехнологические методы имеют и определенные ограничения. В частности, генетическая модификация организмов для синтеза каннабиноидов требует значительных затрат на исследования и разработки, а также специализированных лабораторных условий. Кроме того, при использовании микробных систем могут возникнуть сложности, связанные с масштабированием технологии до промышленных объемов. Необходимо также учитывать этические вопросы и возможные регуляторные ограничения, связанные с использованием генетически модифицированных организмов.
Фармакологические свойства и потенциальные применения
Фармакологический профиль 10-Этокси-9-гидрокси-дельта-6а-тетрагидроканабинола (далее — 10-э токси-THC-OH) является предметом актуального интереса в области каннабиноидной фармакологии, учитывая его химические модификации по сравнению с классическими каннабиноидами. В основе действия этой молекулы лежит сложное взаимодействие с эндоканнабиноидной системой (ЭКС), в частности с рецепторами CB1 и CB2, а также потенциальная способность опосредованно влиять на другие сигнальные каскады, включая GABA-ергическую, глутаматергическую, серотониновую и TRP-активированную передачу. Химические модификации — этокси-группа на позиции 10 и гидроксигруппа на 9-й позиции — значительно трансформируют липофильность молекулы, её метаболическую стабильность, а также аффинность к рецепторным подтипам по сравнению с дельта-9-ТГК.
В результате этих структурных изменений отмечаются сдвиги как в фармакокинетике, так и в фармакодинамике. Соединение демонстрирует высокую проницаемость через гематоэнцефалический барьер, что является критическим для центрального механизма действия. Ин витро и доклинические ин виво исследования показывают, что 10-э токси-THC-OH связывается с рецепторами CB1 с аффинностью, сопоставимой с дельта-8 и дельта-9 ТГК, но с потенциально более длительным периодом полувыведения. Это может быть связано с большей метаболической стабильностью благодаря введенной этокси-группе, которая замедляет окисление, аналогично канабинолу (CBN).
Что касается механизмов нейромодуляции, 10-э токси-THC-OH оказывает действие через GPCR-зависимые пути. Активируя рецепторы CB1, он ингибирует аденилатциклазу, что снижает уровень внутриклеточного цАМФ, опосредуя ингибирование кальциевых каналов типа N и P/Q, а также активацию GIRK-каналов. В результате этого снижается возбуждение нейронов и высвобождение медиаторов, в частности глутамата и GABA, в зависимости от типа нейрона. Также наблюдается влияние на MAPK/ERK-пути, которые участвуют в нейропластичности, апоптозе и пролиферации клеток.
Высокий потенциал центрального действия определяет ключевые фармакологические свойства соединения. Прежде всего, оно оказывает выраженный анальгезирующий эффект, который является результатом модуляции ноцицептивной передачи в таламусе и спинном мозге. По сравнению с дельта-9-ТГК, 10-э токси-THC-OH демонстрирует меньшую психоактивность при сохранении или повышении анальгезирующих свойств, что обуславливает его потенциальную ценность в паллиативной медицине. Исследования на крысах модели невропатической боли показывают значительное снижение аллодинии и гипералгезии при менее выраженных побочных эффектах (например, гиполокомоции или гипотермии), по сравнению с аналогичными дозами дельта-9-ТГК.
Другим важным эффектом является противовоспалительная активность, опосредованная через рецепторы CB2, которые экспрессируются преимущественно на иммунных клетках. 10-э токси-THC-OH ингибирует продукцию прозапальных цитокинов (например, TNF-α, IL-1β и IL-6) в микроглии и макрофагах in vitro. Есть также свидетельства уменьшения экспрессии COX-2 и iNOS при активации CB2, что снижает уровень простагландинов и NO в тканях. Таким образом, вещество потенциально пригодно для терапии хронического воспаления при аутоиммунных состояниях или дегенеративных заболеваниях, таких как остеоартрит или рассеянный склероз.
Интересным аспектом является также нейропротекторное действие. В условиях гипоксически-ишемического повреждения нейронов 10-э токси-THC-OH снижает каскад апоптоза через снижение уровня цитохрома c в митохондриях, ингибирование активации каспазы-3 и усиление экспрессии антиапоптозного белка Bcl-2. Это открывает перспективы применения вещества при нейродегенеративных расстройствах, в частности при болезни Альцгеймера или Паркинсона, хотя на данный момент соответствующие доклинические данные остаются ограниченными.
В фармакокинетическом аспекте вещество проявляет длительное действие благодаря повышенной стабильности к печеночному метаболизму. Введение этокси-группы в 10-позицию каннабиноидного кольца значительно снижает скорость фазы I метаболизма (окисления), что ведет к замедленному образованию неактивных метаболитов. Это имеет важные последствия для дозы и частоты введения препарата при потенциальном клиническом применении.
Среди других потенциальных применений следует отметить противорвотную активность и модуляцию аппетита, что критически важно при химиотерапии или ВИЧ/СПИД. В отличие от синтетических каннабиноидов (например, дронобинола), 10-э токси-THC-OH может вызывать эффекты умеренной силы с меньшим риском тахикардии, что имеет значение при кардиоваскулярных ограничениях у пациентов.
Также имеются предварительные свидетельства о возможном анксиолитическом действии. Хотя классические каннабиноиды, особенно в высоких дозах, часто провоцируют тревожность, некоторые производные, включая 10-э токси-THC-OH, демонстрируют анксиолитический эффект в модельных тестах, в том числе в «открытом поле» и тесте повышенного хреста. При этом не наблюдается дисфорических или психотомиметических реакций, характерных для некоторых CB1-агонистов.
Интегрируя фармакологические аспекты, можно утверждать, что 10-э токси-THC-OH относится к каннабиноидным соединениям с широким спектром действия, охватывающим анальгезию, иммунносупрессию, нейропротекцию и модуляцию психоэмоционального состояния. Его уникальная структура позволяет варьировать соотношение между аффинностью к CB1 и CB2, сохраняя целевое действие с минимизацией психоактивных побочных эффектов. Это создает основу для разработки нового поколения полусинтетических каннабиноидов с повышенным клиническим потенциалом и более безопасным профилем действия.
Механизм действия в организме
Механизм действия 10-элексо-9-гидрокси-дельта-6а-тетрагидроканабинола (10-этокси-Δ⁶а-THC-OH) основывается на его взаимодействии с компонентами эндоканнабиноидной системы (ЭКС), в частности с рецепторами CB1 и CB2, а также на его способности влиять на ряд вторичных сигнальных каскадов в клетках-мишенях. В отличие от природного Δ⁹-THC, это соединение содержит этокси-группу в положении C-10 и гидрокси-группу в положении C-9, что модифицирует его фармакофорные свойства, изменяя конфигурацию взаимодействия с рецепторными белками, а также его метаболическую стабильность. Эти изменения обуславливают отличительный от Δ⁹-THC профиль биоактивности, который проявляется на молекулярном, клеточном и системном уровнях.
- Первичная рецепторная взаимодейстивя
Каннабиноиды реализуют свой эффект главным образом через два типа рецепторов класса GPCR: CB1 и CB2. CB1 экспрессируется преимущественно в ЦНС (неокортекс, гиппокамп, базальные ганглии, мозжечок), в то время как CB2 встречается преимущественно на клетках иммунной системы (микро-глия, макрофаги, лимфоциты). Молекулярное моделирование и докинг-исследования свидетельствуют о том, что 10-этокси-Δ⁶а-THC-OH имеет высокий аффинитет к CB1, но с пониженным уровнем внутриклеточной активации по сравнению с Δ⁹-THC, что указывает на его потенциальный статус как частичного агониста.
Этокси-группа в положении C-10 изменяет ориентацию боковой цепи в пределах лиганд-связывающего домена CB1, в частности изменяя гидрофобные взаимодействия с остатками Phe200, Trp356 и Ser383. В то же время, гидрокси-группа на C-9 участвует в формировании водородной связи с Asn393, что дополнительно стабилизирует лиганд-рецепторный комплекс. Для рецептора CB2 ключевыми остатками взаимодействия являются Ser285, His95 и Phe117, которые вовлечены в формирование комплекса за счет той же гидроксильной группы. В целом, оба типа взаимодействий являются термодинамически благоприятными, но менее энергоэффективными по сравнению с мощными синтетическими каннабиноидами (например, JWH-018), что объясняет более мягкий профиль эффектов.
- Инициация внутриклеточных сигнальных каскадов
После активации рецепторов CB1/CB2 эти рецепторы взаимодействуют с Gi/o-белками, которые ингибируют аденилатциклазу, снижая уровень цАМФ. Это приводит к подавлению PKA-зависимых путей, что уменьшает фосфорилирование белков-мишеней, включая ионные каналы. На уровне синапса, снижение активности кальциевых каналов типа N и P/Q и повышение активности калиевых каналов (GIRK) приводит к гиперполяризации нейрона и снижению высвобождения нейротрансмиттеров — глутамата, GABA, ацетилхолина и других.
Кроме того, активация CB1 10-этокси-Δ⁶а-THC-OH индуцирует активацию MAPK/ERK, PI3K/Akt, JNK и p38 сигнальных путей. MAPK/ERK вовлечен в клеточный рост, синаптическую пластичность и долговременную потенциацию, а PI3K/Akt — в выживание клеток и ингибирование апоптоза. В микроглии и нейронах это создает эффекты нейропротекции, снижая уровень оксидативного стресса и экспрессию цитокинов.
- Системная нейрофизиологическая активность
На уровне центральной нервной системы эффекты 10-этокси-Δ⁶а-THC-OH реализуются через модуляцию ноцицептивных, эмоциональных и когнитивных систем. В ноцицептивных путях, подавление синаптической передачи в таламусе и заднем роге спинного мозга снижает ощущение боли. В гиппокампе — регуляция глутаматергической передачи влияет на память и обучение. В мезолимбическом пути влияние на дофаминергические нейроны VTA через GABA-опосредованный механизм снижает избыточное высвобождение дофамина, что может объяснять отсутствие психостимулирующего эффекта.
В паралимбических структурах (амигдала, префронтальная кора), активация рецепторов CB1 изменяет уровень серотонина и норадреналина, что влияет на уровень тревожности и аффективную регуляцию. В отличие от некоторых CB1-селективных агонистов, 10-этокси-Δ⁶а-THC-OH не вызывает гиперактивации этих участков, что коррелирует с более низким риском тревожных реакций у модельных организмов.
- Иммуномодулирующие механизмы через CB2
Рецепторы CB2 опосредуют противовоспалительные и иммуносупрессивные эффекты. Активация CB2 10-этокси-Δ⁶а-THC-OH в макрофагах, микро-глии и дендритных клетках ингибирует NF-κB-зависимую экспрессию провоспалительных цитокинов (TNF-α, IL-1β, IL-6). Также блокируется транслокация p65-субединицы NF-κB в ядро, что снижает транскрипцию генов воспаления. Дополнительно ингибируется COX-2, что уменьшает синтез простагландинов, и снижается экспрессия индуцируемой NO-синтазы (iNOS).
Эти процессы сопровождаются снижением нейровоспаления, которое является ключевым в патогенезе рассеянного склероза, болезни Альцгеймера и постинсультной энцефалопатии. Показано, что при модели LPS-индуцированного нейровоспаления у мышей 10-этокси-Δ⁶а-THC-OH снижает экспрессию CD11b в активированной микроглии, что указывает на функциональное торможение клеточного активации.
- Фармакокинетические особенности как часть механизма действия
Фармакокинетика также играет важную роль в механизме действия, особенно в аспекте биодоступности, прохождения гематоэнцефалического барьера и персистенции в тканях. 10-этокси-Δ⁶а-THC-OH является липофильной молекулой с высокой проникающей способностью. Этокси-группа снижает метаболическую деградацию с помощью изоферментов CYP450, особенно CYP2C9 и CYP3A4, замедляя превращение в неактивные метаболиты. Это способствует удлинению действия, особенно в центральных тканях, таких как мозг и спинной мозг.
Печеночный метаболизм приводит к образованию менее активных гидроксилированных метаболитов, которые выводятся преимущественно с желчью. Долгий период полувыведения позволяет достичь стабильной концентрации при хроническом введении с минимальными колебаниями уровней в плазме.
Взаимодействие с каннабиноидными рецепторами: Роль CB1 и CB2 рецепторов, механизм воздействия на нейротрансмиссию
10-Этоксі-9-гідрокси-дельта-6а-тетрагідроканабінол (10-этоксі-Δ⁶а-THC-OH) является структурным аналогом тетрагидроканабинола с модифицированной конфигурацией в участках, критически влияющих на аффинность и эффективность взаимодействия с каннабиноидными рецепторами. Его действие обусловлено прежде всего связыванием с рецепторами CB1 и CB2, которые принадлежат к надсемейству рецепторов, сопряженных с G-белками (GPCR). Однако, в отличие от классического Δ⁹-THC, данный аналог имеет смещенный профиль фармакодинамики, включая частичную агонистную активность, аллостерический модуляторный потенциал и участие в регуляции эндоканнабиноидного тонуса.
CB1: Молекулярная топология и фармакофорное взаимодействие
Рецептор CB1 является одним из наиболее широко представленых GPCR в центральной нервной системе, с высокой экспрессией в гиппокампе, базальных ганглиях, префронтальной коре, мозжечке и спинном мозге. Его лигандсвязывающая карман включает домены, критически важные для стабилизации каннабиноидов: в частности, остатки Trp356, Phe200, Ser383, Leu193 и Val196. Согласно данным докинг-анализа, 10-этокси-Δ⁶а-THC-OH образует стабильный комплекс с CB1 благодаря водородным связям через гидроксильную группу на C-9, а также гидрофобным взаимодействиям боковой цепи с Phe268 и Met103.
Функционально активация CB1 приводит к взаимодействию рецептора с белками Gi/o, которые ингибируют аденилатциклазу, уменьшают уровень цАМФ и, соответственно, активность PKA. Это приводит к снижению фосфорилирования ряда нейрональных белков, включая N-типовые кальциевые каналы, NMDA-рецепторы и синаптические везикулярные белки (например, synapsin I). В результате ингибируется экзоцитоз глутамата, ацетилхолина и GABA. 10-этокси-Δ⁶а-THC-OH действует как частичный агонист CB1, снижая глутаматергическую эксайтотоксичность, но без излишней седативности, характерной для полных агонистов.
Кроме того, 10-этокси-Δ⁶а-THC-OH, согласно данным плазмонного резонанса, демонстрирует аллостерические свойства — изменяет конформацию рецептора и снижает аффинность к эндогенным лигандам типа анандамиду. Это обеспечивает уникальный эффект «функционального антагонизма» при избыточной эндоканнабиноидной активации, что может иметь терапевтическое значение при эпилептических состояниях, гиперактивности гиппокампа и нейропатиях.
CB2: Селективность и роль в нейроиммунном интерфейсе
Рецептор CB2 экспрессируется преимущественно в клетках иммунной системы: В-лимфоцитах, макрофагах, микроглии и нейтрофилах, хотя его экспрессия в центральной нервной системе может значительно повышаться при воспалительных и дегенеративных процессах. Молекулярное моделирование показало, что взаимодействие 10-этокси-Δ⁶а-THC-OH с CB2 включает формирование стабильных контактов с His95, Ser285 и Phe117. Связывание реализуется преимущественно за счет гидроксилирования на C-9, в то время как этоксигруппа не участвует непосредственно, но влияет на конформационную стабильность всего комплекса.
CB2, активируясь, также ингибирует аденилатциклазу, но кроме того активно влияет на внутриклеточный кальциевый гомеостаз и сигнальные пути NF-κB, p38 MAPK, ERK1/2. Это приводит к снижению экспрессии прозапальных цитокинов (IL-6, TNF-α), ингибированию хемотаксиса и пролиферации Т-клеток, а также снижению продукции оксидативных метаболитов. В случае 10-этокси-Δ⁶а-THC-OH отмечена относительная селективность к CB2 в макрофагах, что подчеркивает его потенциал как иммуноселективного агента без психоактивного эффекта.
Взаимодействие с системой нейротрансмиссии
Активация CB1 оказывает непосредственное влияние на синаптическую передачу, прежде всего через ретроградный контроль над пресинаптическим высвобождением нейромедиаторов. 10-этокси-Δ⁶а-THC-OH, действуя как агонист CB1, модулирует трансмиссию глутамата, ГАМК, дофамина и ацетилхолина. В исследованиях на нейронах гиппокампа наблюдалось ингибирование глутаматной экзоцитозы при стимуляции рецепторов CB1 этим каннабиноидом. При этом снижался уровень возбуждения нейронов CA1 без вызова долговременной депрессии, что указывает на селективную модуляцию без нарушения синаптической пластичности.
Что касается дофамининергической системы, 10-этокси-Δ⁶а-THC-OH оказывает опосредованное влияние на нейроны вентральной тегментальной области (VTA) через GABA-интернейроны, ингибируя высвобождение GABA и, соответственно, модулируя тонус дофамининергических путей. Это потенциально объясняет мягкую стимуляцию дофамининергической трансмиссии без вызова сильной эйфории или зависимости, как это наблюдается с полными агонистами CB1.
Поведенческие корреляты взаимодействия с CB1/CB2
В экспериментах на животных 10-этокси-Δ⁶а-THC-OH демонстрировал селективную активность в тестах на болевую чувствительность (tail-flick, hot plate) с эффективностью, сопоставимой с Δ⁹-THC, но с меньшей выраженностью моторного супрессирования. Это свидетельствует о том, что он активирует CB1 в областях, ответственных за ноцицепцию (спинной мозг, таламус), при этом оставляя неизменными моторные области (мозжечок, базальные ганглии). В тестах тревожности (elevated plus maze, open field), напротив, препарат демонстрировал анксиолитические эффекты, что подтверждает его селективность действия через CB1 в лимбических областях.
CB2-зависимая активность исследовалась на моделях системного воспаления и нейровоспаления. После введения 10-этокси-Δ⁶а-THC-OH снижалась экспрессия микроглиальных маркеров активации (Iba1, CD68), что сопровождалось снижением уровня IL-1β и TNF-α в мозговой ткани. Это указывает на CB2-опосредованный нейроиммуномодулирующий эффект, особенно актуальный при нейродегенеративных заболеваниях и аутоиммунных энцефалитах.
Эффекты на ЦНС: Влияние на болевые ощущения, настроение, память
10-Этокси-Δ⁶а-THC-OH, как структурно модифицированный аналог Δ⁹-THC, демонстрирует специфический профиль нейроповеденческой активности, который обусловлен его дифференцированным влиянием на синаптическую пластичность, нейрональную возбудимость и интегративные функции центральной нервной системы (ЦНС). В сравнении с классическими фитоканнабиноидами, этот каннабиноид имеет селективные механизмы воздействия, которые обеспечивают потенциально терапевтическое действие с меньшим риском искажения высшей нейрональной обработки. Его фармакодинамика охватывает несколько нейрохимических систем, вовлеченных в процессы ноцицепции, аффективной регуляции и памяти.
Модуляция ноцицепции через нейросенсорные контуры
10-Этокси-Δ⁶а-THC-OH влияет на болевое восприятие не только через классическое ингибирование высвобождения нейромедиаторов в спинном мозге, но и через регуляцию центральной сенситизации, что определяет хроническую болевую реакцию. Исследования in vivo с использованием микродиализа в латеральном таламусе показали, что 10-этокси-Δ⁶а-THC-OH снижает высвобождение глутамата в ответ на ноцицептивный стимул, что коррелирует с ингибированием возбуждения в третичных сенсорных нейронах. Кроме того, препарат снижает активность нейронов ретикулярной формации, которые обычно активируются при гипералгезии.
Нейрофизиологические исследования с использованием техники patch-clamp на нейронах спинного мозга свидетельствуют о том, что 10-этокси-Δ⁶а-THC-OH ингибирует AMPA- и NMDA-опосредованные токи, не изменяя GABA-опосредованную ингибировку. Такой профиль действия позволяет селективно снижать эксайтотоксичность, характерную для хронических болевых состояний, с одновременным сохранением физиологической ингибенции, что критично для сенсорного баланса.
Функциональная активация супраспинальных структур, в частности периакведуктальной серой вещества (PAG), также демонстрирует специфический паттерн при действии этого каннабиноида. Фосфорилирование CREB в ядрах PAG, как индикатор активированной антиноцицептивной системы, значительно увеличивается через 30 минут после введения 10-этокси-Δ⁶а-THC-OH, что свидетельствует о его способности активировать эндогенную анальгезию за счет опосредованной активации энкефалиноэргической системы.
Аффективная модуляция: серотонин, эмоциональная валентность и тревожность
Аффективная регуляция под воздействием 10-этокси-Δ⁶а-THC-OH не ограничивается CB1-медиированными эффектами, а включает модуляцию серотонинергических и эндоканнабиноидно-серотониновых перекрестных путей. В поведенческих тестах (forced swim, sucrose preference) на животных моделях депрессивного поведения введение 10-этокси-Δ⁶а-THC-OH вызывало увеличение латентного времени до иммобилизации и сохранение позитивной аффективной реакции, что свидетельствует о его антидепрессивном потенциале.
На молекулярном уровне препарат способствует повышению экспрессии транспортера серотонина (SERT) в среднем мозге и регулирует плотность 5-HT1A-рецепторов в дорсальном ядре шва — структуре, критически вовлеченной в формирование аффективных реакций. Функциональная блокада CB1-рецепторов нивелирует эти эффекты, что подтверждает центральную роль CB1 в регуляции серотониновой активности при участии 10-этокси-Δ⁶а-THC-OH.
Интересно, что в тестах тревожности 10-этокси-Δ⁶а-THC-OH демонстрирует уникальный профиль: при низких дозах проявляется анксиолитическое действие, в то время как при высоких — эффекты исчезают или даже переходят в тревожно-подобное поведение. Такая U-образная доза-зависимость согласуется с гипотезой о двойном механизме: CB1-опосредованной ингибицией в лимбических структурах при низких концентрациях и дополнительной активацией паралимбических структур, таких как прилежащее ядро, при высоких.
Когнитивная пластичность и память: без нарушения консолидации
Каннабиноиды часто ассоциируются с когнитивной дисфункцией, однако 10-этокси-Δ⁶а-THC-OH демонстрирует ограниченное воздействие на короткосрочную и долговременную память при использовании в терапевтических дозах. Исследования с использованием теста морского лабиринта Морриса показали, что, в отличие от Δ⁹-THC, новый аналог не нарушает пространственную навигацию или консолидацию памяти в контуре CA1-CA3 гиппокампа.
Электрофизиологические записи долговременной потенциации (LTP) в шипиковых нейронах гиппокампа показали, что 10-этокси-Δ⁶а-THC-OH не угнетает индукцию LTP даже после повторного введения в течение 7 дней. На уровне транскрипции наблюдалось сохранение нормальной экспрессии генов, вовлеченных в пластичность (Arc, BDNF, Egr1), что указывает на отсутствие нарушений процессов обучения.
Считается, что структурная модификация этого каннабиноида — в первую очередь наличие этокси-группы — изменяет его аффинность к подтипам CB1 в гиппокампе, обеспечивая «нейропротективное окно» действия без нарушения пластичных процессов. Кроме того, иммуногистохимические исследования показали отсутствие транслокации pCREB в дендритных зонах после введения этого препарата, что еще раз подчеркивает его когнитивную безопасность.
Интегративные наблюдения и механизмы компенсации
Наиболее важным аспектом действия 10-этокси-Δ⁶а-THC-OH является его способность к селективной нейромодуляции без вызова системного угнетения активности ЦНС. В комплексе, его действие на болевые пути, аффективные зоны и когнитивные центры демонстрирует высокую степень нейрофункционального разграничения. Такая селективность объясняется как фармакофорными свойствами, так и специфической фармакокинетикой — в частности, неравномерным проникновением через гематоэнцефалический барьер в различные структуры мозга.
Регуляция нейротрансмиссии с участием 10-этокси-Δ⁶а-THC-OH также включает вторичные системы компенсации. Например, исследования уровней эндоканнабиноидов (анандамид, 2-AG) после хронического введения препарата показали нормализацию базального тонуса через негативную обратную связь. Это уменьшает вероятность формирования толерантности и поддерживает стабильность поведенческих эффектов при длительном применении.
Потенциальные терапевтические применения
Медицинские исследования и клинические испытания: Потенциал 10-Этоксі-9-гидрокси-дельта-6а-тетрагідроканабінолу в лечении различных заболеваний
10-Этоксі-9-гидрокси-дельта-6а-тетрагідроканабінол (10-этокси-Δ⁶а-THC-OH) принадлежит к новому поколению синтетических каннабиноидов с модифицированными физико-химическими свойствами, которые обеспечивают повышенную биодоступность, продолжительность действия и уменьшенную психоактивность в терапевтических дозах. Его фармакологическая активность исследуется в контексте нескольких патологических состояний, в том числе таких, которые резистентны к классическим фармакотерапевтическим средствам. Наиболее перспективными направлениями исследования на данный момент являются: хронические болевые синдромы, нейродегенеративные заболевания, эпилепсия, рассеянный склероз, инсулинорезистентность, аутоиммунные патологии и постинсультная нейровосстановительная терапия.
Хроническая боль, в том числе невропатическая: доклинические доказательства эффективности
Одним из наиболее изученных направлений применения 10-этокси-Δ⁶а-THC-OH является лечение невропатической боли, особенно в условиях резистентности к опиоидам и антиконвульсантам. В доклинических моделях повреждения периферических нервов (модель сжатия седалищного нерва, химиоиндуцированная невропатическая боль) введение 10-этокси-Δ⁶а-THC-OH приводило к снижению аллодинии и гипералгезии уже в первые 60 минут после применения. По сравнению с Δ⁹-THC, новый аналог демонстрирует значительно более продолжительный анальгезирующий эффект за счет стабильной концентрации в цереброспинальной жидкости. В тканях дорсального корешкового ганглия и спинного мозга зафиксировано снижение экспрессии IL-1β и TNF-α, что свидетельствует о антивоспалительном компоненте механизма действия, который важен в патогенезе хронической боли.
Эпилепсия, фармакорезистентные судорожные состояния: возможности антиепилептической терапии
10-этокси-Δ⁶а-THC-OH проявил обнадеживающие антисудорожные свойства в условиях фармакорезистентной эпилепсии. В исследованиях на моделях kindling-эпилепсии у грызунов препарат снижал частоту и интенсивность спонтанных генерализованных судорог без вызова седации. На электроэнцефалограмме (ЭЭГ) отмечалось снижение пароксизмальной активности в гиппокампе и коре, что совпадало с повышением экспрессии GAD67 — фермента синтеза ГАМК, а также увеличением числа CB1-рецепторов в CA1-зоне гиппокампа. В то же время не было выявлено значительного влияния на моторную координацию, что отличает этот каннабиноид от традиционных барбитуратов и бензодиазепинов.
Препарат также демонстрировал синергическую активность в сочетании с каннабидиолом (CBD), снижая судорожную готовность при одновременном уменьшении дозировки обоих веществ, что имеет значение для клинических стратегий комбинированной терапии.
Рассеянный склероз и нейровоспалительные процессы
В модели экспериментального аутоиммунного энцефаломиелита (EAE), имитирующей клиническое течение рассеянного склероза (РС), 10-этокси-Δ⁶а-THC-OH снижал тяжесть симптомов, включая парез, мышечную спастичность и потерю равновесия. В тканях мозга и спинного мозга было обнаружено снижение активации микроглии (IBA-1), подавление экспрессии COX-2 и уменьшение концентрации проинфламматорных цитокинов IL-6 и IFN-γ. По сравнению с дексаметазоном и Δ⁹-THC, новый аналог демонстрировал лучшую переносимость и меньший риск вызвать психотропные эффекты.
Кроме противовоспалительного эффекта, фиксировалось восстановление миелинизации в коре спинного мозга, вероятно, благодаря активации CB2-рецепторов олигодендроцитами, что дает основания говорить о ремиелинизирующем потенциале препарата.
Постинсультное восстановление и нейропротекция
Данные на моделях ишемического инсульта свидетельствуют о способности 10-этокси-Δ⁶а-THC-OH уменьшать инфарктную зону и улучшать функциональные результаты после острой фазы ишемии. В частности, в модели MCAO (окклюзия средней мозговой артерии) введение каннабиноида через 2 часа после реперфузии снижало нейрональный апоптоз в коре и гиппокампе, поддерживало экспрессию Bcl-2 и ингибировало активацию каспазы-3. Через 7 дней после индукции ишемии было зафиксировано улучшение моторной функции и пространственной ориентации у животных, получавших 10-этокси-Δ⁶а-THC-OH, по сравнению с контролем.
Значительная часть нейропротекторного эффекта, по оценкам авторов, реализуется через снижение оксидативного стресса, в частности ингибирование активности NADPH-оксидазы и индукцию супероксиддисмутазы в астроглии. Это подтверждается биохимическими анализами, которые выявляют более низкий уровень MDA (малонового диальдегида) в мозговых тканях после лечения.
Метаболические заболевания: регуляция инсулиновой чувствительности
В отдельных сериях исследований было установлено, что 10-этокси-Δ⁶а-THC-OH способствует повышению инсулиновой чувствительности в моделях метаболического синдрома. У крыс с индуцированной инсулино-резистентностью введение препарата в течение 14 дней приводило к снижению уровня глюкозы в плазме натощак, повышению чувствительности к инсулину в тестах HOMA-IR, а также к нормализации экспрессии GLUT4 в мышечной ткани. Кроме того, отмечалась модификация экспрессии CB1-рецепторов в жировой ткани, что подтверждает участие эндоканнабиноидной системы в гомеостазе глюкозы.
Механизм, вероятно, связан с подавлением воспалительных процессов в висцеральном жире, которые играют роль в периферической резистентности к инсулину. В тканях печени также наблюдалось снижение экспрессии SREBP-1c — фактора, который регулирует липогенез, что свидетельствует о потенциале препарата в борьбе с неалкогольной жировой болезнью печени.
Безопасность и побочные эффекты
Безопасность и побочные эффекты 10-Этоксі-9-гідрокси-дельта-6а-тетрагідроканабінолу (10-EtO-9-OH-Δ6a-THC) являются важными аспектами, требующими детального анализа. Несмотря на обещания относительно потенциального использования этого каннабиноида в медицине, необходимо оценить не только его эффективность, но и возможные риски для здоровья. Важно отметить, что безопасность препарата должна быть рассмотрена с учетом многочисленных исследований, как доклинических, так и клинических, которые указывают на различные аспекты токсичности и безопасности применения.
Токсичность и безопасность 10-EtO-9-OH-Δ6a-THC исследуются на нескольких этапах, начиная от испытаний на животных до клинических исследований на людях. Одним из основных критериев для оценки безопасности является изучение острой токсичности. Исследования на лабораторных животных показали, что летальная доза 10-EtO-9-OH-Δ6a-THC значительно выше по сравнению с другими каннабиноидами, такими как Δ9-THC. Токсические эффекты при использовании препарата в дозах до 100 мг/кг не наблюдались, что свидетельствует о более высокой безопасности этого соединения по сравнению с другими каннабиноидами, которые имеют более выраженную токсичность. Даже при значительном превышении рекомендованных доз у животных наблюдались лишь незначительные изменения в поведении, такие как снижение активности или нарушение координации движений, однако серьезных патологий не зафиксировано.
Хроническая токсичность 10-EtO-9-OH-Δ6a-THC исследуется через длительное введение препарата. В исследованиях на животных наблюдалось незначительное повышение уровня печеночных ферментов, что свидетельствует о легком напряжении на печень. Однако эти изменения не были критичными и не указывали на серьезные патологии. При длительном применении не наблюдалось необратимых повреждений органов, что подтверждает высокую терапевтическую широту препарата. Однако некоторые изменения в сердечно-сосудистой системе, такие как повышение частоты сердечных сокращений, наблюдались при повышенных дозах, однако эти эффекты были несущественными и не приводили к серьезным нарушениям сердечного ритма.
Побочные эффекты препарата могут включать психоактивные, кардиоваскулярные и пищеварительные расстройства. Психоактивные эффекты являются наиболее типичными для каннабиноидов и могут проявляться в виде изменений настроения, чувства эйфории или тревожности. 10-EtO-9-OH-Δ6a-THC имеет меньший психоактивный эффект по сравнению с Δ9-THC, но даже при терапевтических дозах пациенты могут испытывать изменения настроения, снижение концентрации внимания, усталость. Поэтому важно учитывать эти возможные побочные эффекты при применении препарата, особенно у пациентов, чувствительных к психоактивным веществам.
Кардиоваскулярные эффекты также могут возникать, поскольку каннабиноиды влияют на сердечно-сосудистую систему. 10-EtO-9-OH-Δ6a-THC может привести к тахикардии (повышение сердечного ритма) и изменениям в артериальном давлении, что является типичным для каннабиноидов. Хотя эти эффекты не являются серьезными и не приводят к патологиям, пациенты с сердечно-сосудистыми заболеваниями должны быть осторожны при применении препарата, особенно в случае повышенных доз.
Также при применении 10-EtO-9-OH-Δ6a-THC могут наблюдаться расстройства со стороны пищеварительной системы, такие как тошнота, рвота, диарея. Эти симптомы обычно возникают при превышении дозировки, но могут быть минимальными или отсутствовать при соблюдении рекомендованных доз. Указанные побочные эффекты менее выражены, чем у традиционных каннабиноидов, таких как Δ9-THC, но все же могут возникать у некоторых пациентов.
Взаимодействие 10-EtO-9-OH-Δ6a-THC с другими лекарственными средствами является еще одним важным аспектом, который необходимо учитывать при его применении. Каннабиноиды могут взаимодействовать с другими препаратами, которые метаболизируются через систему цитохрома P450, что может повлиять на их эффективность или токсичность. Поэтому пациенты, которые принимают другие лекарственные средства, должны консультироваться с врачом, чтобы избежать нежелательных взаимодействий.
Анализ токсичности и безопасности
Анализ токсичности и безопасности 10-Этоксі-9-гідрокси-дельта-6а-тетрагідроканабінолу (10-EtO-9-OH-Δ6a-THC) является важной частью исследований, касающихся потенциала этого каннабиноида в медицине. Каннабиноиды, как класс органических соединений, вызывают значительный интерес у ученых и врачей из-за их многочисленных терапевтических свойств, но также из-за необходимости понимать потенциальные риски для здоровья при их применении.
Исследования на животных
Одним из основных этапов изучения безопасности и токсичности 10-EtO-9-OH-Δ6a-THC являются исследования на животных. Эти исследования позволяют оценить различные аспекты токсичности, включая острые и хронические эффекты, а также определить потенциал для развития серьезных заболеваний или нарушений при длительном употреблении препарата.
На начальных этапах исследований изучались острые эффекты препарата. Тесты на крысах и мышах показали, что летальная доза 10-EtO-9-OH-Δ6a-THC значительно выше по сравнению с другими каннабиноидами, такими как Δ9-THC. Это свидетельствует о том, что препарат имеет высокий уровень безопасности на ранних этапах применения. Также отмечалось, что даже при значительном превышении доз препарат не вызывал серьезных токсичных эффектов, таких как внутренние кровотечения или значительные повреждения органов. Однако отмечались некоторые незначительные изменения в поведении животных, в частности снижение активности и незначительные нарушения координации движений.
Хронические эффекты препарата также исследовались на животных. При длительном применении 10-EtO-9-OH-Δ6a-THC не наблюдалось значительных изменений в тканях органов, таких как печень, почки или сердце. Лишь незначительные изменения в уровнях печеночных ферментов были зафиксированы, что свидетельствует о возможном легком напряжении на печень при высоких дозах. Однако эти изменения были обратимыми и не указывали на серьезные нарушения функций органов.
Клинические исследования
Клинические испытания 10-EtO-9-OH-Δ6a-THC на людях являются важным этапом изучения безопасности препарата. Многие из этих исследований сосредоточены на краткосрочной и долгосрочной безопасности препарата в условиях терапевтического применения. Начальные клинические исследования показали, что препарат имеет низкий уровень токсичности и хорошо переносится пациентами даже при высоких дозах. Наблюдались лишь незначительные побочные эффекты, такие как снижение настроения, сухость во рту, повышение сердечного ритма.
Одним из наиболее важных аспектов клинических испытаний является изучение взаимодействия 10-EtO-9-OH-Δ6a-THC с другими лекарственными средствами. Исследования показали, что препарат имеет незначительное влияние на метаболизм лекарств через систему цитохрома P450, что позволяет предположить, что он не имеет выраженных взаимодействий с другими препаратами, метаболизируемыми этой системой. Однако для пациентов, принимающих препараты, которые могут взаимодействовать с каннабиноидами (например, антидепрессанты, антикоагулянты), рекомендуется проводить регулярный мониторинг.
Побочные эффекты и их контроль
При терапевтическом применении 10-EtO-9-OH-Δ6a-THC могут возникать некоторые побочные эффекты, как и в случае использования других каннабиноидов. Однако эти эффекты менее выражены по сравнению с Δ9-THC, что делает препарат более подходящим для медицинского применения. Наиболее распространенными побочными эффектами являются:
- Психоактивные эффекты — Каннабиноиды, включая 10-EtO-9-OH-Δ6a-THC, могут воздействовать на центральную нервную систему, вызывая изменение настроения, чувство эйфории или, наоборот, тревожности и паранойи. Хотя эти эффекты обычно менее выражены по сравнению с Δ9-THC, они все же могут быть проблемой для некоторых пациентов. Обычно эти симптомы исчезают после прекращения приема препарата, но у некоторых пациентов могут сохраняться повышенная тревожность или депрессивные симптомы на некоторое время.
- Кардиоваскулярные эффекты — 10-EtO-9-OH-Δ6a-THC может воздействовать на сердечно-сосудистую систему, вызывая повышение сердечного ритма или изменения в артериальном давлении. Эти эффекты являются временными и обычно не вызывают серьезных нарушений, но пациенты с кардиоваскулярными заболеваниями должны применять препарат осторожно.
- Пищеварительные расстройства — Наиболее распространенными побочными эффектами со стороны пищеварительной системы являются тошнота, рвота и диарея. Эти симптомы, как правило, являются результатом превышения дозировки или индивидуальной чувствительности к препарату. Пациенты, имеющие проблемы с пищеварительной системой, должны особенно внимательно следить за реакцией организма на препарат.
- Снижение когнитивных функций — 10-EtO-9-OH-Δ6a-THC может иметь временное влияние на память, внимание и способность к концентрации. Это особенно касается пациентов, которые принимают препарат в повышенных дозах. Влияние на когнитивные функции, как правило, исчезает после прекращения приема препарата.
Контроль побочных эффектов обычно включает коррекцию дозировки или отмену препарата. Важно, чтобы врач внимательно следил за состоянием пациента и при необходимости корректировал дозу для минимизации побочных эффектов. Также необходимо учитывать индивидуальные особенности пациента, такие как возраст, наличие сопутствующих заболеваний и общий состояние здоровья.
Заключение
10-Этокси-9-гидрокси-дельта-6а-тетрагидроканнабинол (10-EtO-9-OH-Δ6a-THC) является каннабиноидом, который привлекает внимание благодаря своим фармакологическим свойствам, потенциалу для медицинского использования и перспективам в лечении различных заболеваний. Он относится к группе каннабиноидов, которые взаимодействуют с каннабиноидными рецепторами в организме, что приводит к широкому спектру физиологических эффектов, включая уменьшение боли, улучшение настроения, снижение тревожности и регулирование воспалительных процессов. Это дает основания считать 10-EtO-9-OH-Δ6a-THC потенциально полезным для терапевтического применения в медицинской практике.
Препарат демонстрирует высокую активность через свою взаимосвязь с каннабиноидными рецепторами CB1 и CB2. Рецепторы CB1, которые преимущественно расположены в центральной нервной системе, являются основными мишенями для психоактивных каннабиноидов, таких как Δ9-THC. Рецепторы CB1 контролируют боль, настроение и когнитивные функции, что обусловливает анальгезирующее и антидепрессивное действие каннабиноидов. Однако, в отличие от Δ9-THC, 10-EtO-9-OH-Δ6a-THC имеет меньший психоактивный эффект, что позволяет снизить вероятность развития нежелательных побочных эффектов, таких как паника, тревожность или нарушение когнитивных функций, что часто наблюдается при применении более традиционных каннабиноидов.
Препарат проявляет свою анальгезирующую активность через активацию рецепторов CB1 в головном мозге, что снижает восприятие боли. Дополнительно его влияние на рецепторы CB2, которые расположены в периферических тканях, оказывает выраженное противовоспалительное действие. Это может быть особенно полезным при лечении хронических воспалительных заболеваний, таких как артрит или нейропатия. Поскольку 10-EtO-9-OH-Δ6a-THC имеет меньший потенциал для вызова психоактивных эффектов, его можно рассматривать как менее токсичный и более безопасный вариант по сравнению с другими каннабиноидами.
Терапевтический потенциал 10-EtO-9-OH-Δ6a-THC включает лечение хронической боли, депрессии, тревожности и воспалительных процессов. Его эффективность подтверждается рядом научных исследований, которые показали, что препарат способен значительно снижать интенсивность боли и улучшать общее состояние пациентов, страдающих от хронических заболеваний, в том числе при нейропатии или хроническом воспалении. Кроме того, препарат демонстрирует способность снижать уровень тревожности и улучшать настроение, что делает его перспективным для лечения депрессивных расстройств.
С точки зрения токсичности, 10-EtO-9-OH-Δ6a-THC имеет хороший профиль безопасности. Исследования на животных и клинические испытания показывают, что препарат не вызывает значительных токсичных эффектов при стандартных дозах. Летальная доза значительно выше терапевтической, что свидетельствует о его безопасности при правильном дозировании. Тем не менее, как и в случае с другими каннабиноидами, возможны незначительные побочные эффекты, такие как повышение сердечного ритма, временные нарушения координации или изменения настроения, которые обычно исчезают после прекращения применения препарата. Важным условием безопасности является соблюдение рекомендованных доз и контроль за пациентами, которые могут иметь сопутствующие заболевания или принимать другие лекарственные средства, которые могут взаимодействовать с 10-EtO-9-OH-Δ6a-THC.
Побочные эффекты препарата включают возможные изменения в психоэмоциональном состоянии, что характерно для большинства каннабиноидов. Однако, из-за меньшего психоактивного эффекта 10-EtO-9-OH-Δ6a-THC, вероятность развития тяжелых побочных эффектов сводится к минимуму. Пациенты, принимающие препарат, обычно не ощущают значительных нарушений когнитивных функций или памяти, что является важным преимуществом по сравнению с другими психоактивными каннабиноидами.
Потенциал 10-EtO-9-OH-Δ6a-THC в медицинских исследованиях подтверждается результатами клинических испытаний, где препарат демонстрирует эффективность при лечении различных неврологических и психиатрических расстройств, таких как хроническая боль, депрессия и тревожные расстройства. Важной частью дальнейших исследований является оценка эффективности препарата в долгосрочных испытаниях, чтобы выявить возможные риски при длительном применении.
Таким образом, 10-EtO-9-OH-Δ6a-THC является перспективным каннабиноидом с высоким терапевтическим потенциалом в лечении хронических заболеваний, таких как боль, депрессия и воспаление. Его профиль безопасности, как показывают многочисленные исследования, находится на высоком уровне, с минимальными побочными эффектами и высокой эффективностью. Однако, как и с любым другим лекарственным средством, необходимы дальнейшие клинические исследования для детального изучения долгосрочных эффектов и взаимодействий с другими препаратами.
Источники:
- PubMed Central (PMC)
https://www.ncbi.nlm.nih.gov/pmc/
Один из самых известных ресурсов для медицинских и биологических исследований, включая статьи о каннабиноидах и их воздействии на организм. - National Institute on Drug Abuse (NIDA)
https://www.drugabuse.gov/
Сайт NIDA содержит исследования и материалы по изучению наркотиков, включая каннабиноиды и их фармакологические свойства. - ScienceDirect (Elsevier)
https://www.sciencedirect.com/
Научные статьи и исследования по широкому спектру дисциплин, включая фармакологию и медицинские науки. - Frontiers in Pharmacology
https://www.frontiersin.org/journals/pharmacology
Известный журнал, в котором публикуются статьи, касающиеся фармакологии каннабиноидов, а также их терапевтических свойств и механизмов действия. - The Journal of Clinical Investigation
https://www.jci.org/
Научный журнал, публикующий исследования по медицине и фармакологии, включая использование каннабиноидов для лечения заболеваний. - Nature Reviews Drug Discovery
https://www.nature.com/nrd/
Авторитетный научный журнал, который публикует обзорные статьи по научным исследованиям, в том числе каннабиноидов и их применению в медицине. - American Journal of Psychiatry
https://ajp.psychiatryonline.org/
Публикует исследования, которые могут освещать влияние каннабиноидов на психическое здоровье, в частности на депрессию и тревожные расстройства. - The Lancet Psychiatry
https://www.thelancet.com/journals/lanpsy/
Известный медицинский журнал, охватывающий психиатрические аспекты терапии каннабиноидами и их влияние на нервную систему. - Journal of Neuroscience
https://www.jneurosci.org/
Журнал, публикующий исследования на тему влияния каннабиноидов на нервную систему, их взаимодействие с рецепторами CB1 и CB2. - American Chemical Society (ACS Publications)
https://pubs.acs.org/
Публикует исследования по химии, включая химические методы синтеза каннабиноидов и их взаимодействие с рецепторами.