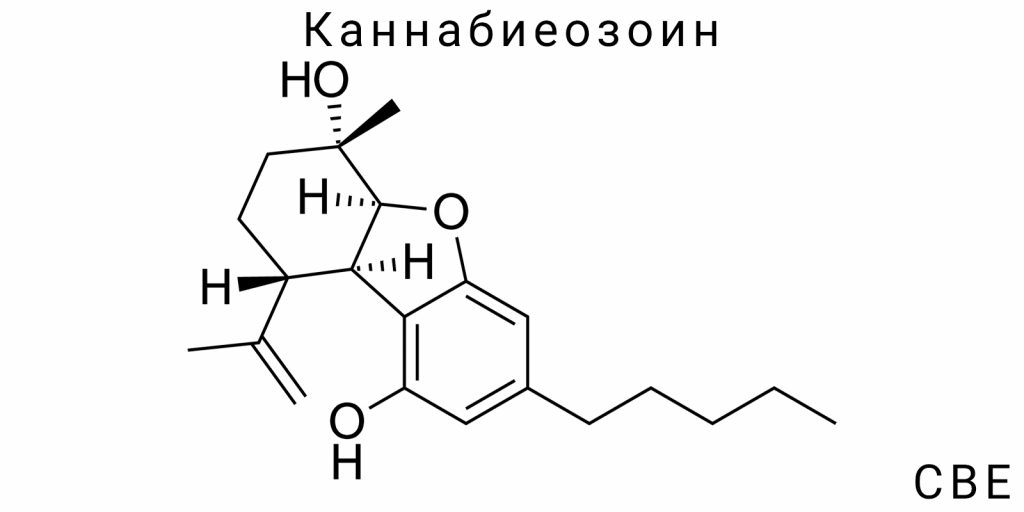
В области каннабиноидной науки значительную часть внимания традиционно привлекают первичные биоактивные компоненты Cannabis sativa, однако реальные фармакологические последствия их применения в организме во многом определяются продуктами вторичного метаболизма. Одним из таких малоисследованных, но критически важных веществ является Каннабиеозоин (CBE) — метаболит, который формируется в результате окислительных преобразований каннабидиола (CBD) в организме человека или животного. Несмотря на химическую инертность, CBE имеет стойкий профиль накопления и выявляется даже в тех случаях, когда первичное соединение полностью очищено из плазмы. Этот факт определяет его потенциал как ретроспективного биомаркера в клинических, токсикологических и биофармацевтических исследованиях.
Каннабиеозоин не является типичным фитоканнабиноидом в прямом смысле, поскольку не синтезируется в самой растении, а образуется in vivo в результате метаболизма. Эта особенность ставит его вне классической классификации каннабиноидов и делает его маркером не фитохимического, а эндогенного каннабиноидного обмена. С научной точки зрения это открывает новую линию исследований — метаболомику вторичных каннабиноидов, где фокус смещается с хемотипов растения на индивидуальный метаболический ответ организма.
Еще одним определяющим аспектом является структурная уникальность CBE, которая указывает на участие специфических оксидоредуктаз и других ферментов фазы I метаболизма, вероятно, с привлечением нетипичных ферментативных путей. В случаях вариативного метаболизма CBD, связанного с генетическими полиморфизмами ферментов CYP450, количественные соотношения между CBD, его гидроксилированными формами и CBE могут отражать индивидуальную ферментативную активность, а значит, иметь клиническую ценность в персонализированной медицине.
Таким образом, несмотря на длительное игнорирование в научном дискурсе, Cannabielsoin следует рассматривать не как фармакологически неактивный остаток, а как маркер более глубоких биохимических процессов, который может быть использован для усовершенствования аналитических методов, валидации биопрепаратов, диагностики воздействия каннабиноидов, а также исследования метаболических вариаций между пациентами. Его изучение позволяет не только детализировать биохимическую карту превращений каннабидиола, но и формировать новые парадигмы в оценке биодоступности, продолжительности действия и безопасности каннабиноидной терапии.
Химическая и стереохимическая идентичность
Молекулярная формула и ключевые функциональные группы
Каннабиеозоин (CBE) является вторичным фитоканнабиноидом, образующимся в результате дальнейшей трансформации первичных каннабиноидов, в частности каннабидиола (CBD). Молекулярная формула CBE — C21H30O4, что отражает наличие 21 атома углерода, 30 атомов водорода и четырех атомов кислорода. Эта формула характерна для окисленных производных каннабиноидов, но именно пространственное расположение функциональных групп и наличие кольцевых структур придают CBE специфические свойства.
CBE имеет несколько важных функциональных групп, среди которых особенно стоит выделить фенольную гидроксильную группу, которая определяет частичную полярность молекулы и ее антиоксидантный потенциал. В структуре CBE также присутствует тетрагидропирановый фрагмент, который образуется в результате внутримолекулярного циклирования продуктов окисления CBD. Этот фрагмент критически влияет на конформационную стабильность молекулы, ее аффинность к мембранным рецепторам и способность к гидрофобным взаимодействиям.
Формально CBE не содержит карбоксильной группы, что отличает его от кислотных каннабиноидов типа CBDA или THCA. В то же время наличие кетогруппы или гидроксикетона на алициклическом кольце повышает его реакционную способность в средах с вариативным pH, в частности в биологических жидкостях. Некоторые изолированные изомеры CBE также демонстрируют вариативную электронную плотность в пределах ароматического кольца, что влияет на его взаимодействие с энзиматическими системами, особенно с ферментами фазы I (типа CYP450).
Ключевым аспектом для идентификации CBE является также гидрофобно-полярное взаимодействие с хроматографическими системами. В отличие от более липофильных метаболитов, CBE демонстрирует частичную растворимость в среднеполярных растворителях, таких как этилацетат, что имеет важное аналитическое значение для выделения из биологических матриц. Функциональные группы, ответственные за эту особенность — преимущественно фенольная и оксигруппа при тетрагидропирановом кольце.
Хиральные центры и изомерные варианты
CBE является хиральным соединением, которое содержит как минимум один асимметричный атом углерода, обычно локализованный в циклическом фрагменте, образующемся после окислительной трансформации каннабидиола. Идентифицированные изомеры CBE включают как минимум два энантиомера, которые имеют одинаковую химическую формулу, но различное пространственное расположение заместителей. Это отражается на аффинности к белковым рецепторам, способности к транспорту в биологических системах и даже на стабильности в плазме крови.
В контексте стереохимии важным является тот факт, что большинство природно образующихся CBE являются (−)-энантиомерами, что является характерной особенностью каннабиноидов биогенного происхождения. В лабораторных условиях, однако, возможен выход рацематных смесей, особенно при неферментативной биотрансформации или фотоиндуцированном окислении. Такая изомерная неоднородность усложняет аналитическую валидацию CBE при использовании LC-MS/MS, так как изомеры могут иметь схожую массу, но разные retention time или ионизационные характеристики.
Следует отметить, что наличие хиральных центров также создает потенциал для специфического биологического действия, поскольку пространственное расположение атомов в молекуле является ключевым фактором во взаимодействии с белками-мишенями. Например, один из энантиомеров может иметь аффинность к белкам TRPV, в то время как другой останется инертным. Таким образом, рацемическая чистота является критически важной для дальнейших фармакологических исследований CBE.
Кроме энантиомеров, CBE также проявляет таутомерные варианты, в частности в условиях изменения pH среды или под воздействием ультрафиолетового излучения. Таутомеризация может изменять электронную плотность в ароматическом кольце, модифицировать электрофильность отдельных атомов, что усложняет прогнозирование реактивности при метаболических трансформациях. Важно также учитывать существование цис-/транс-изомерии в случае некоторых синтетических аналогов CBE, обусловленной положением заместителей в гидропирановом кольце.
Хиральные и изомерные особенности CBE имеют не только химическое или фармакологическое значение, но и служат инструментами в химотаксоналии — например, соотношение энантиомеров CBE в разных сортах конопель может быть стабильным генетическим маркером для дифференциации химотипов или даже для криминалистических исследований.
Биохимическое происхождение и механизмы образования
Каннабиеозоин (CBE) является одной из метаболитных форм каннабиноидов, образующихся в результате биохимических преобразований, характерных для растений семейства Cannabis. Как и большинство каннабиноидов, CBE может образовываться в организме человека и животных в процессе метаболизма каннабидиола (CBD) через различные ферментативные пути, которые зависят от специфических условий, таких как тип организма, активность ферментов, наличие микробиоты и другие факторы.
Метаболическое превращение CBD в CBE
Одним из основных путей образования CBE является метаболизм каннабидиола (CBD). CBD, как и другие каннабиноиды, проходит через несколько этапов метаболических преобразований, включая окисление, гидроксилирование и другие химические реакции. Этот процесс включает участие ферментов, таких как цитохром P450, которые играют важную роль в метаболизме фармакологических соединений.
В условиях организма человека CBD подвергается гидроксилированию на различные углеродные атомы молекулы, что способствует образованию гидроксилированных метаболитов, в частности 7- и 8-гидроксилированных форм CBD. Однако не все эти преобразования являются конечными. Далее окислительные процессы могут привести к образованию каннабиеозоина (CBE), в котором на молекуле CBD происходит окисление в карбоксильную группу.
Механизм этого преобразования полностью не изучен, но исследования показывают, что важную роль в этом процессе играют такие ферменты, как цитохромы P450 и другие ферменты, отвечающие за реакции фазы I метаболизма. В результате окисления молекулы CBD образуются карбоксилированные производные, среди которых есть и CBE.
Факторы, влияющие на образование CBE
На скорость и эффективность превращения CBD в CBE влияет несколько факторов:
- Тип ферментов цитохрома P450. Эти ферменты имеют разную активность в зависимости от генетических особенностей человека или животного. Варианты генов, кодирующих определенные типы цитохромов, могут изменять способность организма метаболизировать каннабиноиды.
- Микробиота кишечника. Микроорганизмы, населяющие желудочно-кишечный тракт, могут также иметь значительное влияние на метаболизм каннабиноидов. Некоторые бактерии могут способствовать гидролизу эстера CBD, превращая его в более активные метаболиты.
- Дозировка и частота употребления. Доза каннабидиола и частота его потребления могут изменять скорость метаболических процессов. При регулярном употреблении CBD ферменты, отвечающие за его метаболизм, могут изменять свою активность через механизмы индукции или ингибирования, что влияет на образование CBE.
- Физиологическое состояние организма. Заболевания печени, например, могут существенно изменять активность ферментов, участвующих в метаболизме каннабиноидов. Эти факторы могут привести к различным результатам в образовании CBE в организме в зависимости от того, насколько печень способна метаболизировать CBD.
- Другие медикаменты. Применение других фармакологических препаратов может изменить активность ферментов цитохрома P450. Такие взаимодействия могут как увеличивать, так и снижать скорость превращения CBD в CBE. Например, препараты, ингибирующие цитохромы P450, могут снижать образование CBE, в то время как индукция этих ферментов может увеличить количество этого метаболита.
- Стереохимическая форма CBD. Каннабидиол существует в нескольких стереоизомерных формах, и хотя все они могут проходить метаболические превращения, разные формы могут иметь различную способность к взаимодействию с ферментами метаболизма. Это может привести к различной скорости превращения в CBE.
Сложность метаболических превращений
Механизм образования CBE от CBD является частью сложной серии биохимических реакций, которые могут отличаться в разных организмах. Хотя общие представления о метаболизме CBD существуют, исследования на уровне молекулярных механизмов все еще продолжаются. Например, на молекулярном уровне важным аспектом является взаимодействие между активными метаболитами и клеточными рецепторами, что может влиять на физиологические реакции организма на CBE, хотя окончательные выводы еще не сделаны.
Метаболизм каннабидиола, в частности превращение его в CBE, включает несколько этапов, каждый из которых может быть регулируем различными факторами, что делает этот вопрос сложным для однозначного описания. Однако последние исследования и лабораторные работы способствуют более глубокому пониманию этих процессов.
Влияние на здоровье человека
В связи с широким изучением каннабиноидов и их воздействия на организм человека, возникают новые перспективы для исследования CBE. Исследования указывают на его потенциал в медицинских применениях, в частности как мощный антиоксидант, противовоспалительное средство и нейропротектор. Его метаболитные пути позволяют прогнозировать возможные терапевтические эффекты и взаимодействия с другими лекарственными средствами. На основе этих механизмов становятся очевидными новые направления для клинических исследований, в частности для лечения воспалительных заболеваний, нервных расстройств и многих других состояний.
Эти данные открывают широкие возможности для разработки новых препаратов, включающих CBE, а также для определения его роли в биохимических процессах организма человека. Тщательное изучение превращения CBD в CBE помогает расширить понимание метаболических путей каннабиноидов и их потенциала для применения в медицине и фармакологии.
Методологии экстракции и выявления
Экстракция и выявление каннабиезоина (CBE) являются важными этапами в исследованиях этого каннабиноида, так как точность и чувствительность методов позволяют не только определить его присутствие в биологических образцах, но и способствуют более глубокому пониманию его биохимических и фармакокинетических свойств. Поскольку CBE является метаболитом каннабидиола (КБД), его выявление требует высококачественных и высокочувствительных методов, способных эффективно изолировать, идентифицировать и количественно определить в сложных биологических матрицах. В этом разделе будут рассмотрены несколько ключевых подходов к экстракции и выявлению CBE, включая хроматографические методы, а также новейшие методы, включая LC-MS/MS.
Хроматографическая изоляция на основе фракционирования
Хроматография является основным методом для изоляции и выявления CBE в различных биологических образцах, таких как кровь, моча, слюна или ткани. Одной из самых распространенных методик является жидкостная хроматография с жидкостным фазовым разделением (HPLC), которая используется для анализа каннабиноидов и их метаболитов. Однако важным аспектом является то, что каннабиезоин имеет сходные свойства с другими каннабиноидами, в частности с КБД, поэтому важно использовать высокочувствительные хроматографические техники для точного разделения этих соединений.
Для эффективного фракционирования применяются методы, основанные на принципах адсорбции, которые позволяют разделять компоненты смеси с помощью различий в их полимерных свойствах и величине молекул. Наиболее часто используемыми являются методы с использованием колонок с наполнением различной полимерной природы, что позволяет повысить селективность разделения каннабиезоина от других метаболитов.
Метод жидкостной хроматографии с распределительной фазой (liquid-liquid chromatography) позволяет обеспечить достаточно высокую чистоту метаболита для дальнейших исследований. Ключевым фактором является оптимизация параметров, таких как температура колонки, скорость потока элюента и концентрация органического растворителя, что влияет на способность CBE проходить через колонку без взаимодействия с другими компонентами.
Однако хроматография не является единственным методом, который обеспечивает точность и эффективность в выявлении и анализе CBE. Для более сложных задач, таких как точное количественное определение, эти методы могут сочетаться с другими техниками, такими как масс-спектрометрия.
Использование высокочувствительных LC-MS/MS методов
Методы LC-MS/MS (жидкостная хроматография с масс-спектрометрией в двойной стадии) являются одними из самых передовых и чувствительных подходов для выявления и анализа каннабиезоина. Эта методика позволяет не только изолировать отдельные компоненты, но и точно определять их структуру и количество на основе массы молекул и её изотопных характеристик.
В сочетании с жидкостной хроматографией (LC), MS/MS позволяет обеспечить высокую чувствительность и точность измерений, в частности в случаях, когда концентрации метаболитов, таких как CBE, находятся на уровне микродоз. С помощью этой методики можно определить точную молекулярную массу метаболита и его структурные особенности, что делает LC-MS/MS незаменимым инструментом для исследований, требующих детального химического анализа.
Одним из основных преимуществ LC-MS/MS является способность к высокочувствительному выявлению соединений, даже если они находятся в очень низких концентрациях в биологических образцах. Это особенно важно для каннабиезоина, так как его уровни могут быть минимальными из-за метаболических преобразований, происходящих в организме после употребления КБД.
В процессе LC-MS/MS образец сначала проходит через хроматографическую колонку, где компоненты образца разделяются на основе их физико-химических свойств, таких как гидрофильность, заряд и размер молекул. После этого разделенные соединения попадают в масс-спектрометр, где происходит их ионизация. Ионизированные молекулы затем проходят через масс-спектр, где их масса и заряд измеряются, и на основе этих данных определяется молекулярная структура.
Метод LC-MS/MS особенно важен для исследований на уровне метаболизма каннабиезоина, так как он позволяет выявлять не только основной метаболит, но и его изомерные варианты и другие сопутствующие компоненты, которые могут быть присутствовать в биологических образцах.
Сравнение стабильности с другими неактивными метаболитами
Одним из основных аспектов для оценки эффективности метаболизма и фармакокинетики CBE является его стабильность в биологических системах по сравнению с другими каннабиноидными метаболитами, такими как каннабидиол (КБД) или его другие метаболиты. Стабильность метаболитов может существенно влиять на точность их измерений и определение в биологических образцах.
Для оценки стабильности используют несколько подходов, среди которых важными являются сравнительные исследования стабильности в разных условиях, таких как температура, pH среды и другие физиологические факторы. CBE может демонстрировать различный уровень стабильности по сравнению с другими каннабиноидами и их метаболитами в зависимости от условий хранения и обработки образцов. Например, при хранении в низкотемпературных условиях стабильность CBE оказывается выше, чем при высокой температуре, что может вызвать деградацию молекулы.
Также важным является изучение стабильности CBE в процессах метаболизма. Если каннабидиол (КБД) может подвергаться различным биохимическим изменениям, таким как гидроксилирование или окисление, то CBE может быть более стабильным в некоторых условиях, в частности при взаимодействии с определенными ферментами или в процессе метаболических преобразований. Таким образом, сравнение стабильности CBE с другими метаболитами важно для понимания его роли в организме и выявления путей для оптимизации процесса экстракции и определения.
Физиологические особенности и фармакокинетика Каннабидиолзоина (КБЗ)
Каннабидиолзоин (КБЗ) является важным метаболитом каннабидиола (КБД), и его физиологические свойства в значительной мере зависят от механизмов метаболизма и взаимодействия с различными молекулами в организме. Поскольку КБЗ не является основной соединением каннабиноидной группы, а является результатом превращения КБД, его фармакокинетика и физиологические эффекты в значительной мере схожи с аналогичными процессами для других каннабиноидов, однако с некоторыми уникальными характеристиками.
Взаимодействие с плазменными белками
Одной из ключевых физиологических характеристик КБЗ является его взаимодействие с плазменными белками. Каннабиноиды, включая КБЗ, способны связываться с белками плазмы, и это взаимодействие имеет важное значение для их фармакокинетики, в частности для распределения в организме, транспортировки через клеточные мембраны и продолжительности действия в организме.
Основными плазменными белками, с которыми могут взаимодействовать каннабиноиды, являются альбумин, глобулин и липопротеины. Связывание с альбумином является особенно важным, поскольку этот белок является основным транспортным механизмом для многих фармакологически активных соединений в крови. Связывание КБЗ с альбумином может ограничить его биологическую активность на уровне клеток, поскольку лишь незначительная часть молекул, которые не связаны с белками, может проникать через клеточные мембраны и вступать в биохимические реакции.
Кроме того, связывание с липопротеинами может влиять на фармакокинетику КБЗ, поскольку липопротеины являются важными носителями липофильных соединений, к которым относится и КБЗ. Это связывание может изменять распределение КБЗ в различных тканях организма, включая мозг, поскольку каннабиноиды могут проникать через гематоэнцефалический барьер, а липидная природа этих молекул облегчает их транспортировку через клеточные мембраны.
Важно отметить, что уровень связывания КБЗ с белками может изменяться в зависимости от различных факторов, таких как концентрация каннабидиолзоина в крови, наличие других соединений, взаимодействующих с теми же белками, а также индивидуальные особенности организма, такие как генетические вариации в структуре плазменных белков.
Метаболическая инертность и кинетика выведения
Метаболическая инертность КБЗ является важной характеристикой его фармакокинетики. Поскольку КБЗ является метаболитом каннабидиола, он подвергается дополнительным биохимическим превращениям в печени, где через различные ферментные системы он может превращаться в другие производные каннабиноиды или быть метаболизирован до более полярных соединений, которые способны выводиться из организма через мочу или желчь.
Несмотря на эти превращения, КБЗ обладает относительно высокой метаболической инертностью по сравнению с другими каннабиноидами, такими как ТГК, что обуславливает его стабильность в организме. Это позволяет КБЗ длительное время оставаться активным в биологических образцах и вызывать эффекты даже после метаболических превращений КБД. Метаболизм КБЗ в значительной степени регулируется ферментами семейства цитохрома P450, которые осуществляют основные реакции окисления и метаболизма. Кроме того, КБЗ может подвергаться глюкуронизации в печени, что является основным путем его детоксикации и выведения из организма.
Особенностью фармакокинетики КБЗ является его способность к длительному циркуляции в организме после первоначального введения. Это может быть связано с высоким уровнем связывания с плазменными белками, что замедляет процесс его выведения. При этом, хотя каннабидиолзоин метаболизируется через систему цитохрома P450, его кинетика выведения остается относительно стабильной на протяжении длительного времени, что позволяет ему накапливаться в органах и тканях, где он может проявлять свою активность в течение нескольких часов или даже суток.
Кинетика выведения КБЗ зависит от количества метаболитов, которые образуются в процессе его превращения. В основном, КБЗ выводится через почки в виде водорастворимых метаболитов или в желчь. Интеграция с системами детоксикации организма также является важным элементом для обеспечения баланса между накоплением и выведением каннабидиолзоина.
Влияние фармакокинетических свойств на клиническое применение
Фармакокинетика КБЗ имеет важное значение для его потенциального клинического применения. Благодаря относительной метаболической инертности и высокому связыванию с плазменными белками, КБЗ может иметь продолжительный эффект на организм, что делает его перспективным кандидатом для использования в терапии, где необходим длительный терапевтический эффект без частого введения.
Благодаря высокой стабильности в организме, КБЗ может быть полезным в лечении заболеваний, связанных с хронической болью, воспалением или неврологическими нарушениями, где необходима стабильная и длительная терапевтическая активность. Однако важно отметить, что для оптимизации терапевтического эффекта необходимо учитывать индивидуальные различия в метаболизме каннабидиолзоина, что может зависеть от генетических факторов, состояния печени и других индивидуальных характеристик пациентов.
Поскольку КБЗ обладает высокой химической стойкостью и способностью к длительному пребыванию в организме, его использование в клинических условиях должно быть тщательно отрегулировано, чтобы избежать возможных побочных эффектов, таких как накопление токсических концентраций в тканях или взаимодействие с другими препаратами.
Биологическая нейтральность или потенциал Каннабидиолзоина (КБЗ)
Каннабидиолзоин (КБЗ) является метаболитом каннабидиола (КБД), но, в отличие от своего предшественника, не проявляет психоактивных эффектов, которые характерны для других каннабиноидов, таких как тетрагидроканабинол (ТГК). Вследствие своей химической структуры КБЗ имеет значительную биологическую нейтральность, что является важной характеристикой при исследованиях его потенциала как фармакологической молекулы.
Данные относительно отсутствия психоактивности
Одной из наиболее значимых характеристик КБЗ является его отсутствие психоактивного эффекта. Психоактивность каннабиноидов обычно связана с их способностью связываться с рецепторами каннабиноидной системы (CB1 и CB2). Тетрагидроканабинол, как основной психоактивный компонент каннабиса, имеет высокую аффинность к рецепторам CB1 в центральной нервной системе, что объясняет его эмоциональные и когнитивные эффекты. Однако КБЗ, по сравнению с ТГК, не обладает способностью эффективно связываться с этими рецепторами, что обуславливает его отсутствие психоактивных свойств.
Кроме того, исследования показали, что КБЗ не проявляет значительного взаимодействия с другими рецепторами, которые участвуют в регуляции настроения, поведения и когнитивных функций, такими как серотониновые или дофаминовые рецепторы. Это позволяет утверждать, что КБЗ не вызывает традиционных психоактивных эффектов, таких как эйфория, нарушение когнитивных функций или изменения восприятия. Важно, что это делает КБЗ безопасным вариантом для терапевтического использования, так как он не будет вызывать нежелательные психоэмоциональные изменения у пациентов.
Некоторые исследования даже показывают, что КБЗ может взаимодействовать с каннабиноидными рецепторами более умеренным способом, что указывает на его возможную роль в модуляции эффектов других каннабиноидов. Например, есть данные, что КБЗ может взаимодействовать с рецепторами CB2, которые в основном регулируют иммунные процессы и воспаление, без прямой активации нейропсихологических путей, что характерно для других каннабиноидов.
Кроме того, в отличие от ТГК, КБЗ не вызывает повышения уровня серотонина или дофамина, что обычно связано с психоактивными эффектами каннабиноидов. Это делает КБЗ перспективным кандидатом для использования в медицинских целях, где отсутствие психоактивной активности является ключевым фактором, особенно при лечении пациентов, которым необходима стабильность психологического состояния.
Наблюдения по клеточной биосовместимости
Поскольку КБЗ имеет потенциал для использования в медицинских целях, очень важно оценить его биосовместимость с клетками организма. Биосовместимость определяет способность материала или соединения сосуществовать с живыми клетками, не вызывая негативных эффектов или отторжения организмом.
В исследованиях по клеточной биосовместимости КБЗ было установлено, что этот каннабиноид не имеет токсических эффектов на клетки при обычных дозах, используемых в терапевтических исследованиях. Например, в исследованиях на культуре клеток человека (HepG2, Jurkat) не было обнаружено значительного цитотоксического эффекта при обработке клеток КБЗ в различных концентрациях. Это свидетельствует о его способности быть безопасным для клеток при применении в терапевтических дозах.
Важно отметить, что КБЗ может оказывать положительное влияние на клеточные процессы, которые включают антиоксидантную защиту, воспалительные реакции и стабилизацию клеточной мембраны. Например, в экспериментах на культурах клеток было показано, что КБЗ способен снижать окислительный стресс, который часто является причиной клеточных повреждений и старения. Это делает КБЗ перспективным для применения в терапии заболеваний, связанных с окислительным стрессом, таких как сердечно-сосудистые заболевания, нейродегенеративные расстройства и некоторые виды рака.
Кроме того, КБЗ оказывается нейтральным относительно иммунного ответа организма. В отличие от некоторых других каннабиноидов, которые могут влиять на иммунную систему через активацию рецепторов CB2, КБЗ не проявляет значительной иммуносупрессивной активности. Это является важным преимуществом при его применении в медицинских целях, где важно избежать чрезмерного угнетения иммунной системы, особенно у пациентов с ослабленным иммунитетом.
Оценка биосовместимости также включает изучение возможных генотоксических эффектов. На сегодняшний день нет доказательств того, что КБЗ способен вызвать повреждение ДНК в клетках человека. Это является важным фактором для безопасности использования КБЗ в клинических применениях, так как отсутствие генотоксичности указывает на то, что КБЗ не приводит к мутациям или канцерогенезу, что является важным аспектом при разработке новых терапевтических препаратов.
Потенциал для терапевтического применения
Хотя КБЗ не имеет психоактивной активности, его биологические свойства открывают значительный потенциал для терапевтического применения. По сравнению с другими каннабиноидами, которые часто связаны с психоактивными эффектами, КБЗ имеет значительно более мягкий профиль, что делает его привлекательным вариантом для лечения пациентов, которые требуют длительного терапевтического эффекта без риска психоактивных побочных эффектов.
Поскольку КБЗ взаимодействует с каннабиноидными рецепторами CB2, он может быть использован для лечения воспалительных процессов, нейродегенеративных заболеваний, а также для поддержания здоровья сердечно-сосудистой системы. Его свойства, направленные на уменьшение окислительного стресса и поддержку гомеостаза клеток, могут быть полезными при лечении заболеваний, связанных с окислительным повреждением, таких как болезнь Альцгеймера, болезнь Паркинсона, а также при депрессии и тревожных расстройствах.
Кроме того, КБЗ имеет потенциал быть использованным как антиоксидантное средство в косметических средствах, поскольку его способность снижать окислительный стресс может способствовать замедлению процессов старения кожи и улучшению её состояния.
Для чего Каннабие́лзоин (CBE): Практическое применение и перспективы
Каннабие́лзоин (CBE), как метаболит каннабидиола (CBD), обладает огромным потенциалом в нескольких научных и медицинских сферах благодаря своим уникальным свойствам. Поскольку CBE имеет не только характеристики, позволяющие использовать его в качестве биомаркера метаболизма CBD, но и возможность применения в токсикологических исследованиях, его потенциал распространяется на важные направления в фармакокинетике, биомониторинге и диагностике потребления каннабиноидов.
Маркер метаболизма CBD в фармакокинетических исследованиях
Один из наиболее важных аспектов использования CBE в фармакокинетических исследованиях заключается в его способности служить надежным маркером для изучения метаболических путей каннабидиола. Поскольку CBD метаболизируется в организме через несколько этапов, в том числе с участием ферментов, таких как CYP450, образование CBE является важным этапом в этом процессе. Это позволяет ученым лучше понимать механизмы превращения CBD в организме человека и других млекопитающих, что, в свою очередь, имеет важное значение для оценки эффективности и безопасности лекарственных препаратов на основе CBD.
В частности, CBE может использоваться для мониторинга скорости метаболизма CBD и взаимодействия с другими веществами, которые также могут влиять на метаболические пути, такими как ингибиторы или индукторы ферментов. Это позволяет разрабатывать оптимизированные схемы дозирования, которые максимизируют терапевтический эффект и минимизируют риски побочных эффектов. Кроме того, исследования метаболизма CBD с использованием CBE могут помочь выявить потенциальные взаимодействия между каннабиноидами и другими лекарственными средствами, что важно для пациентов, одновременно принимающих несколько препаратов.
Благодаря использованию CBE в качестве маркера можно также отслеживать динамику концентраций различных каннабиноидов в плазме крови, что важно для определения оптимальных доз и продолжительности терапевтического применения CBD.
Использование как контрольного метаболита в токсикологии
Еще одной перспективной областью применения CBE является токсикология. Благодаря своей роли как метаболита CBD, CBE может служить контрольным маркером в исследованиях токсичности каннабидиола и других каннабиноидов. Для токсикологических исследований важно оценить, могут ли метаболиты каннабиноидов оказывать неблагоприятное воздействие на организм, включая токсичность для органов или нарушение функций клеток.
Использование CBE в таких исследованиях позволяет более точно отслеживать метаболические пути каннабидиола и оценивать его возможное влияние на организм. Поскольку сам CBE не обладает психоактивными свойствами, исследования с его участием могут указывать на возможность того, что CBD может быть эффективным без токсичных побочных эффектов, в частности, на центральную нервную систему или на печень.
Кроме того, метаболическая нейтральность CBE позволяет использовать его в качестве базового контрольного метаболита при оценке безопасности других каннабиноидов, которые могут быть токсичными в результате их биотрансформации в организме. Это особенно важно для разработки новых терапевтических средств на основе каннабиноидов, поскольку точная оценка безопасности имеет критическое значение на всех этапах клинических испытаний.
Также, поскольку CBE является продуктом биотрансформации CBD, он может использоваться для изучения того, как CBD влияет на организм при длительном применении, что позволяет выявить потенциальные кумулятивные эффекты или взаимодействия с другими метаболитами.
Перспективы биомониторинга потребления каннабиноидов
Биомониторинг потребления каннабиноидов с помощью анализа их метаболитов является важным инструментом для изучения воздействия каннабиноидных продуктов на организм, а также для контроля их использования в клинических или исследовательских условиях. Каннабие́лзоин (CBE), будучи метаболитом CBD, представляет собой потенциально важный биомаркер для таких мониторинговых исследований. Появление CBE в моче, крови или слюне может служить свидетельством потребления каннабидиола, что позволяет использовать этот метаболит для отслеживания употребления каннабиноидов, даже если CBD не был обнаружен в первичных образцах.
Современные технологии анализа, такие как хроматография и масс-спектрометрия, позволяют определять низкие концентрации CBE в биологических жидкостях, что делает его удобным инструментом для проведения клинических или токсикологических исследований. С помощью биомониторинга можно оценивать продолжительность и дозу потребления каннабидиола, а также установить индивидуальные особенности метаболизма различных пациентов или групп населения.
Это может быть полезным не только для исследований в рамках клинических испытаний, но и для контроля за использованием каннабиноидов у пациентов с хроническими заболеваниями, такими как рак или эпилепсия, где каннабиноиды применяются в составе лечебной терапии. Отслеживание метаболитов CBD с помощью CBE позволяет медицинским работникам точно контролировать уровень активных соединений в организме и, соответственно, корректировать дозировку препаратов.
Кроме того, биомониторинг каннабиноидов может быть использован для оценки экологической токсикологии и безопасности употребления каннабиноидных продуктов среди широкой аудитории. В последние годы наблюдается тенденция к увеличению количества продуктов на основе CBD на рынке, включая пищевые добавки, косметику и даже напитки. Поскольку каннабиноиды могут иметь кумулятивные эффекты при длительном употреблении, важно контролировать, не приводит ли регулярное потребление таких продуктов к накоплению метаболитов в организме. CBE, как один из таких метаболитов, может помочь в проведении мониторинга с целью оценки безопасности потребления каннабиноидов.
Роль Каннабие́лзоина (CBE) в фармакогеномике и персонализированной медицине
Каннабие́лзоин (CBE), как метаболит каннабидиола (CBD), занимает важную роль в контексте фармакогеномики и персонализированной медицины. Благодаря уникальной биохимической характеристике, CBE может иметь значение не только в плане определения эффективности терапии на основе каннабиноидов, но и в создании персонализированных планов лечения для пациентов. Индивидуальные вариации в метаболизме CBE из-за генетических особенностей и влияния на пути метаболизма делают его перспективным инструментом в научных исследованиях и медицинских практиках.
Индивидуальные профили метаболизма и образования CBE
Индивидуальные профили метаболизма каннабидиола (CBD) и, соответственно, образования каннабие́лзоина (CBE), являются существенным аспектом при рассмотрении фармакогеномики. CBE образуется путем биотрансформации CBD, и этот процесс зависит от индивидуальных генетических особенностей, в частности, вариаций в генах, кодирующих ферменты метаболизма. Каннабидиол метаболизируется через систему ферментов цитохрома P450, а также в процессах глюкуронизации во второй фазе, что обуславливает изменчивые уровни метаболитов в организме каждого человека.
Индивидуальные вариации в генах CYP450 (например, CYP3A4, CYP2C19, CYP2C9) могут существенно изменять скорость метаболизма CBD и образование CBE. Это может иметь важные последствия для определения оптимальных доз каннабиноидов в лечебных целях. У некоторых пациентов со специфическими генотипами метаболизм может быть ускоренным или, наоборот, замедленным, что приводит к накоплению метаболитов или снижению эффективности терапии.
Персонализированный подход к терапии с использованием каннабиноидов включает изучение генетических факторов, которые могут влиять на метаболический путь, чтобы создать наиболее эффективные планы лечения. Например, у пациентов с повышенной активностью ферментов CYP450 может наблюдаться более быстрый метаболизм CBD, что может потребовать корректировки дозировки для достижения желаемого эффекта. В обратном случае, для пациентов с низкой активностью определенных ферментов может потребоваться снижение дозы или выбор альтернативных терапевтических подходов.
Вариабельность активности ферментов CYP450
Ферменты CYP450 (цитохром P450) являются основными мишенями для метаболизма каннабиноидов, таких как CBD, и играют центральную роль в превращении CBD в его активные и неактивные метаболиты, включая образование каннабие́лзоина (CBE). Однако вариации в генах, кодирующих эти ферменты, могут привести к существенным изменениям в метаболических путях каннабидиола, что имеет важные последствия для фармакокинетики и терапевтической эффективности лечения.
Ключевыми генами для метаболизма CBD являются CYP2C9, CYP3A4 и CYP2C19. Исследования показали, что существует широкий диапазон генетических полиморфизмов в этих ферментах, что может значительно влиять на скорость метаболизма каннабидиола. Например, у пациентов с аллельными вариантами, приводящими к сниженной активности CYP3A4 или CYP2C9, метаболизм CBD будет замедленным, что может приводить к более высоким концентрациям метаболитов, таких как CBE. Это важно для корректировки дозировки лекарственных средств на основе каннабиноидов.
Поскольку эти ферменты активно участвуют также в метаболизме других лекарственных средств, вариации в их активности могут вызывать многочисленные лекарственные взаимодействия. Например, использование ингибиторов CYP3A4 может снизить метаболизм CBD, повышая концентрацию CBE в организме, что может потребовать тщательного мониторинга уровней каннабиноидов во время лечения.
Параллельные направления исследований
Исследования каннабие́лзоина (CBE) не ограничиваются только фармакогенетическими аспектами. Параллельные направления включают изучение его нейропротекторных свойств, а также возможное взаимодействие с другими метаболитами каннабидиола, что открывает новые горизонты для персонализированной медицины. Благодаря своей способности взаимодействовать с молекулярными мишенями в организме, CBE может стать важным элементом в терапии неврологических заболеваний, таких как болезнь Альцгеймера или инсульт.
Это создаёт возможность для развития инновационных лечебных подходов, учитывающих индивидуальные генетические особенности метаболизма и потенциал каннабиноидов в нейропротекции. Поэтому изучение CBE и его влияния на метаболические пути, а также взаимодействия с другими препаратами является важным направлением для создания более точных и эффективных терапевтических стратегий.
Исследования CBE в контексте нейропротекции
Последние исследования показывают, что каннабие́лзоин (CBE) может обладать нейропротекторными свойствами, сходными с другими каннабиноидами, в частности с каннабидиолом. Поскольку CBE является продуктом метаболизма CBD, он может сохранять некоторые из его полезных эффектов, но с меньшими психоактивными свойствами. Это может иметь важное значение при разработке новых терапевтических средств для лечения неврологических расстройств.
Нейропротекторные свойства CBE могут быть обусловлены его способностью снижать окислительный стресс, который является ключевым фактором в развитии нейродегенеративных заболеваний, таких как болезнь Альцгеймера и Паркинсона. Окислительный стресс является следствием избытка активных форм кислорода (АФК) в клетках, что приводит к повреждению мембран, белков и ДНК. Метаболиты каннабидиола, такие как CBE, могут помочь снизить уровень окислительного стресса, способствуя защите нейронов от повреждений.
Возможная роль в регуляции окислительного стресса
Одним из наиболее перспективных направлений исследования CBE является его роль в регуляции окислительного стресса. Окислительный стресс является одним из основных факторов, влияющих на прогрессирование многих хронических заболеваний, включая нейродегенеративные расстройства, сердечно-сосудистые заболевания и рак. Каннабие́лзоин, как метаболит каннабидиола, способен взаимодействовать с механизмами антиоксидантной защиты клеток, в частности через активацию различных антиоксидантных ферментов, таких как супероксиддисмутаза (SOD) и каталаза.
Это имеет важное значение для разработки терапевтических средств, которые могут использоваться для лечения состояний, связанных с высоким уровнем окислительного стресса. Использование CBE в качестве компонента для снижения уровня АФК в организме может стать основой новых подходов к лечению возрастных заболеваний и заболеваний центральной нервной системы.
Взаимодействие с ферментами фазы II: глюкуронирование
Одной из важных характеристик метаболизма CBE является его взаимодействие с ферментами фазы II метаболизма, в частности с процессом глюкуронирования. Фаза II метаболизма включает реакции, которые добавляют глюкуронидную группу к молекулам, что облегчает их выведение из организма. В случае CBE глюкуронирование является основным путём его детоксикации и выведения.
Глюкуронирование каннабие́лзоина осуществляется при участии ферментов UDP-глюкуронилтрансфераз (UGT), которые являются ключевыми для метаболизма многих лекарственных средств. Вариации в генах, кодирующих эти ферменты, могут приводить к изменениям в скорости метаболизма CBE и его выведения, что имеет значение для оптимизации дозировки каннабиноидов в медицинских целях. Понимание механизмов, лежащих в основе глюкуронирования CBE, важно для улучшения фармакокинетики каннабиноидов и обеспечения более точного контроля за уровнями активных метаболитов в организме.
Биоаналитические методы изучения Каннабиэлзоина (CBE) и его метаболитов
В научных и медицинских исследованиях каннабиноидов, таких как каннабиэлзоин (CBE), важным аспектом является применение биоаналитических методов для точного изучения их фармакокинетики, метаболизма и биологических эффектов. Биоаналитика включает использование различных методов для количественного определения каннабиноидов в биологических матрицах, таких как кровь, моча, слюна и ткани. Для этого необходимо разрабатывать надёжные и чувствительные методы, способные точно выявлять низкие концентрации каннабиэлзоина в сложных биологических средах.
Методы калибровки CBE в биологических матрицах
Калибровка методов определения каннабиэлзоина в биологических матрицах является важной составляющей биоаналитических исследований. Поскольку уровень каннабиэлзоина в биологических образцах, как правило, низкий, необходимо использовать высокочувствительные методы для точного определения его концентраций.
Один из самых распространённых методов определения концентраций каннабиэлзоина — это высокоэффективная жидкостная хроматография с масс-спектрометрией (HPLC-MS). Этот метод позволяет точно измерять низкие уровни метаболитов в биологических образцах с высокой специфичностью и чувствительностью. Для калибровки таких методов используются стандартные растворы каннабиэлзоина, которые готовятся в точных концентрациях. Калибровочные графики строятся на основе соотношения между концентрацией метаболита и интенсивностью сигнала, получаемого во время анализа. Важной частью калибровки также является определение предела обнаружения (LOD) и предела количественного определения (LOQ) для обеспечения точности измерений на низких уровнях концентрации.
Другие методы, такие как газовая хроматография с масс-спектрометрией (GC-MS), также применяются для определения каннабиэлзоина, но они менее чувствительны по сравнению с HPLC-MS, особенно при анализе биологических образцов с низкими концентрациями метаболитов. Однако метод GC-MS может быть полезен для уточнения структурных характеристик метаболитов благодаря своей способности к детальной масс-спектрометрии.
Дифференциация артефактов и конверсий в лабораторных условиях
Один из основных вызовов при использовании биоаналитических методов — это дифференциация реальных метаболитов от артефактов или продуктов конверсии, которые могут образовываться во время хранения или обработки биологических образцов. Каннабиноиды и их метаболиты подвержены химическим преобразованиям при изменении условий хранения (температуры, pH и т.д.), что может привести к образованию ложных или побочных продуктов. Это может исказить результаты и затруднить точное определение концентраций метаболитов.
Для минимизации риска артефактов важно использовать методы, способные выявлять специфические маркеры метаболитов, особенно при использовании масс-спектрометрии. Одним из подходов является выбор специфических фрагментов молекул (ионов), которые образуются во время ионизации метаболитов, что позволяет избежать ложных сигналов от побочных продуктов. Кроме того, исследование также предусматривает использование стабильных изотопов для внутренней калибровки, что позволяет корректировать ошибки, вызванные преобразованиями молекул в процессе хранения или обработки образцов.
Дифференциация артефактов и реальных метаболитов также может осуществляться путём сравнения результатов с использованием стандартных образцов или путём совместного применения различных методов анализа. Например, комбинация масс-спектрометрии с жидкостной хроматографией позволяет точно отличать каннабиэлзоин от потенциальных артефактов, таких как метаболиты с иными структурными характеристиками.
Перспективы дальнейших исследований
Поскольку каннабиэлзоин является относительно новым метаболитом каннабидиола, необходимо провести более детальные исследования его биологической активности и метаболических путей. Одним из перспективных направлений является изучение его взаимодействия с различными ферментами метаболизма, в частности через систему CYP450 и ферменты фазы II, способствующие глюкуронированию. Понимание этого процесса позволит создать новые терапевтические стратегии для использования каннабиноидов в лечении различных заболеваний.
Дополнительно значительный интерес вызывают исследования влияния каннабиэлзоина на окислительный стресс и нейропротекцию, особенно в контексте нейродегенеративных заболеваний. Эти исследования могут привести к разработке новых фармакологических средств для борьбы с болезнью Альцгеймера и Паркинсона.
С другой стороны, изучение фармакокинетики и фармакодинамики каннабиэлзоина в различных биологических матрицах поможет понять его эффективность и безопасность в терапевтических дозах. Необходимы более точные данные о различных вариантах метаболизма в зависимости от генетических факторов пациента, что позволит разработать индивидуализированные схемы лечения для пациентов в зависимости от их генетического профиля.
Использование в биоинформатике каннабиноидных метаболомов
Благодаря развитию биоинформатики, современные подходы позволяют создавать модели метаболических путей каннабиноидов, включая каннабиэлзоин, что позволяет прогнозировать их биологическую активность, фармакокинетику и потенциальные клинические эффекты. Изучение каннабиноидных метаболомов с помощью биоинформатических платформ позволяет создавать интегрированные модели метаболических путей, которые могут помочь в прогнозировании метаболических преобразований и взаимодействий с другими препаратами.
Это особенно важно для дальнейших исследований каннабиноидов в персонализированной медицине, поскольку позволяет учитывать индивидуальные особенности метаболизма и разрабатывать наиболее эффективные терапевтические стратегии для каждого пациента. Биоинформатика также может быть использована для создания инструментов для выявления потенциальных новых метаболитов каннабиэлзоина и их биологических эффектов.
Потребность в многоцентровых валидационных исследованиях
Поскольку исследования каннабиэлзоина все еще находятся на стадии активного развития, необходимо проведение многоцентровых валидационных исследований для оценки точности и надежности биоаналитических методов определения этого метаболита. Важность таких исследований заключается в том, что они позволяют обеспечить стандартизацию методов и установить международные критерии для определения концентраций каннабиэлзоина в биологических матрицах.
Валидационные исследования должны включать различные типы образцов (кровь, моча, слюна, ткани) и различные уровни концентрации метаболита, чтобы обеспечить точность измерений в широком диапазоне концентраций. Такие исследования также позволяют сравнивать эффективность различных биоаналитических методов и определить оптимальные подходы для их использования в медицинских и научных целях.
Заключение
Все вышеупомянутые аспекты изучения каннабиэлзоина (КБЭ) демонстрируют важность и сложность этого метаболита каннабидиола в контексте биоаналитических, фармакокинетических и фармакодинамических исследований. КБЭ, как один из активных компонентов каннабиноидов, обладает многочисленными потенциальными применениями в медицинской практике, в частности в области нейропротекции, регуляции окислительного стресса и персонализированной медицины. Однако для эффективного использования каннабиэлзоина в терапевтических целях необходимо тщательно изучить его механизмы действия, метаболизм, а также взаимодействие с другими препаратами и биологическими системами.
Фармакокинетика и метаболизм каннабиэлзоина продолжают оставаться ключевыми аспектами для оценки безопасности и эффективности его применения. Для этого необходимо разработать высокочувствительные биоаналитические методы, способные точно измерять низкие концентрации этого метаболита в биологических образцах. Современные методы, такие как высокоэффективная жидкостная хроматография с масс-спектрометрией, демонстрируют высокую точность и чувствительность, однако для получения достоверных результатов необходимо постоянное совершенствование процесса калибровки и минимизации артефактов.
Дифференциация артефактов и конверсий в лабораторных условиях является важной составляющей обеспечения точности биоаналитических методов. Это позволяет получить достоверные данные, которые служат основой для дальнейшего применения каннабиэлзоина в медицинских и клинических исследованиях.
Важной частью дальнейших исследований является биоинформатика каннабиноидных метаболомов, которая позволяет создавать модели метаболических путей, предсказывать биологическую активность и взаимодействие каннабиэлзоина с другими метаболитами и лекарственными средствами. Это открывает новые возможности для индивидуализации лечения и создания новых терапевтических стратегий для пациентов с различными генетическими и метаболическими профилями.
Перспективы дальнейших исследований заключаются в проведении многоцентровых валидационных исследований, которые позволят стандартизировать биоаналитические методы и определить оптимальные параметры для измерения каннабиэлзоина в различных биологических матрицах. Эти исследования также будут способствовать разработке международных критериев для оценки концентраций каннабиэлзоина и его метаболитов, что является важным этапом в медицинском использовании каннабиноидов.
Роль в персонализированной медицине и фармакогеномике каннабиэлзоина имеет большой потенциал благодаря способности учитывать индивидуальные профили метаболизма пациентов. Вариабельность активности ферментов CYP450, участвующих в метаболизме каннабиэлзоина, является важным фактором, который может влиять на эффективность и безопасность терапии каннабиноидами. Понимание этого процесса позволит создать более точные и безопасные стратегии лечения, основанные на генетических характеристиках каждого пациента.
Таким образом, для полного понимания потенциала каннабиэлзоина необходимо продолжать исследования, в частности в контексте фармакогенетики, метаболизма, биоаналитики и клинической практики. Применение новейших биоаналитических методов и биоинформатических платформ для анализа метаболомов каннабиноидов позволит осуществить более точное прогнозирование эффектов каннабиэлзоина, что обеспечит эффективное и безопасное применение этого метаболита в медицинских целях.
Источники:
- National Institutes of Health (NIH)
PubMed (https://pubmed.ncbi.nlm.nih.gov/) — база данных с рецензируемыми научными статьями в области медицины и биологии. Можно найти статьи, касающиеся метаболизма каннабиноидов, таких как каннабиэлзоин (КБЭ), фармакокинетики и взаимодействия с различными ферментами. - National Institute on Drug Abuse (NIDA)
NIDA — Cannabinoids (https://www.drugabuse.gov/drug-topics/marijuana) — Институт является частью NIH и специализируется на исследованиях, касающихся наркотиков и каннабиноидов, их фармакологии и биологии.
- U.S. National Library of Medicine (NLM)
Toxicology Data Network (TOXNET) (https://toxnet.nlm.nih.gov/) — база данных с информацией о токсикологических свойствах веществ, включая каннабиноиды, и их влиянии на организм. - Centers for Disease Control and Prevention (CDC)
CDC — Marijuana and Public Health (https://www.cdc.gov/marijuana/index.htm) — предоставляет данные и рекомендации относительно воздействия каннабиноидов на здоровье, включая исследования механизмов действия и метаболизма. - Journal of Pharmacology and Experimental Therapeutics
J Pharmacol Exp Ther (https://jpet.aspetjournals.org/) — научный журнал, публикующий исследования по фармакокинетике, метаболизму каннабиноидов и их фармакологическим эффектам. - The Journal of Clinical Investigation
J Clin Invest (https://www.jci.org/) — известный журнал, публикующий высококачественные исследования по биохимии и фармакологии, включая каннабиноидные соединения и их влияние на организм. - ScienceDirect
ScienceDirect — Cannabinoids (https://www.sciencedirect.com/topics/pharmacology-toxicology-and-pharmaceutical-science/cannabinoid) — платформа с доступом к статьям по фармакологии и биологии. Можно найти исследования о каннабиноидах и их метаболизме, включая роль ферментов CYP450.