Несмотря на быстрый рост интереса к каннабиноидам в фармакологии и нейробиологии, канабинол (CBN) долгое время оставался в тени более изученных соединений, таких как Δ9-тетрагидроканнабинол (THC) и каннабидиол (CBD). Его статус как вторичного метаболита, который образуется преимущественно в результате автоокисления Δ9-THC, часто приводил к ошибочному отождествлению с «неактивным» или даже «деградированным» продуктом. Такой подход игнорирует существенную биологическую специфику CBN, а также его уникальные физико-химические и фармакокинетические свойства, которые отличают его как от первичных фитоканнабиноидов, так и от синтетических каннабиноидных аналогов.
CBN — это не просто побочный продукт действия кислорода на THC. Он является отдельным каннабиноидом с полноценной фармакологической активностью, которая не сводится к подавленной активности на CB1-рецепторы. Его частичная агонистическая активность на CB2-рецепторах, а также аффинность к неглавным каннабиноидным и TRP-рецепторам (в частности, TRPA1) свидетельствует о потенциале этого соединения в изучении периферийных противовоспалительных путей, модуляции ноцицепции и нейровоспаления. Кроме того, в отличие от THC, CBN демонстрирует значительно меньший психоактивный профиль, что открывает возможности для терапевтического применения без ограничений, связанных с психотропностью THC.
Исторически CBN был первым каннабиноидом, изолированным в чистом виде и охарактеризованным с помощью методов классической органической химии: его структура была установлена в 1930-х годах, еще до идентификации THC. Именно с CBN связано зарождение систематического химического исследования конопель, хотя позднее его маргинализировали из-за низкой концентрации в свежем растении. Следует подчеркнуть, что изоляция CBN часто была косвенным показателем качества или «свежести» конопляного сырья, что вводило в заблуждение относительно его фармакологического потенциала.
Еще одной недооцененной особенностью CBN является его уникальная стабильность в условиях, при которых большинство каннабиноидов теряют активность или структуру. Например, CBN демонстрирует более высокую термическую стабильность по сравнению с THC, что делает его перспективным кандидатом для формулировок, которые требуют стерилизации, или для применения в условиях длительного хранения. Его химическая инертность также позволяет исследовать специфические взаимодействия с мембранными белками без побочного влияния на рецепторную динамику, что характерно для менее стабильных молекул.
В отличие от других каннабиноидов, CBN не продуцируется растением напрямую через энзиматический биосинтез из каннабигероловой кислоты (CBGA) — его возникновение полностью зависит от постбиосинтетических процессов, включая фотохимические и окислительно-восстановительные реакции. Это ставит CBN в концептуально отдельную категорию «вторичных» или «декандентных» каннабиноидов, чье количественное присутствие в образце служит индикатором возраста, способа хранения и степени окисления первичных компонентов. Такой подход открывает перспективу использования CBN как химического маркера деградации или фотодеградации каннабиноидной системы.
С учетом современных подходов к полифармакологии и модульному анализу эффекта энтуриджа (entourage effect), CBN начинает привлекать внимание как потенциально ко-активное соединение, способное влиять на фармакодинамику других компонентов фитоканнабиноидного спектра. Например, исследования показывают, что CBN может изменять транскрипционную активность микроглии или влиять на экспрессию провоспалительных цитокинов, модулируя тем самым активность CBD в периферической среде. В таких условиях CBN выходит за пределы роли «вторичного каннабиноида» и приобретает статус функционального элемента фитохимической композиции.
Не менее важным является тот факт, что CBN входит в круг каннабиноидов, которые чаще всего встречаются в переработанной или сохраненной конопле, что обусловило его активное изучение в контексте безопасности продуктов, вторичной переработки сырья и длительного воздействия на организм. Такие исследования позволяют рассматривать CBN не только как биологически активное соединение, но и как индикатор технологического процесса — в частности, в условиях стандартизации фармацевтических препаратов из конопли.
Биогенез и химическое происхождение CBN
Канабинол (CBN) не синтезируется в растении Cannabis sativa через классические энзиматические пути, характерные для основных фитоканнабиноидов, а возникает в результате постбиогенетических преобразований. Его появление является прямым следствием нестабильности Δ9-тетрагидроканнабинола (Δ9-THC), в частности его чувствительности к окислительным процессам. Это принципиально отличает CBN от каннабиноидов первичного биосинтеза, таких как каннабигерол (CBG), каннабидиол (CBD) или сам Δ9-THC, образование которых основывается на энзиматическом превращении общего предшественника, каннабигеролевой кислоты (CBGA), с участием специфических синтаз.
CBN формируется преимущественно путём некаталитического автоокисления Δ9-THC в присутствии атмосферного кислорода и света. Этот процесс не требует ферментов или специфических ко-факторов, что позволяет ему происходить в уже собранном, сушеном или хранимом растительном материале. С точки зрения органической химии, трансформация Δ9-THC в CBN включает дегидрогенизацию и ароматизацию части молекулы: в частности, циклогексановая часть основы Δ9-THC теряет две пары атомов водорода, что приводит к образованию ароматической бензеновой системы в структуре CBN. Этот ароматический кольцевой фрагмент является ключевым отличием — он стабилизирует молекулу, уменьшая её реактивность и склонность к дальнейшим деградационным процессам.
Хотя канабинол исторически идентифицировался как продукт действия времени и среды на конопляное сырьё, имеющиеся данные показывают, что процессы его образования могут быть контролируемыми и целенаправленно индуцированными в лабораторных условиях. Например, моделирование условий освещенности, влажности, температуры и доступа кислорода позволяет регулировать скорость превращения Δ9-THC в CBN с достаточно высокой селективностью. Известны также методы каталитической окислительной ароматизации с использованием агентов типа хлорхинона или марганцевых комплексов, которые позволяют ускорить процесс превращения без сопутствующего распада других структур. В рамках химико-технологического подхода подобные реакции можно реализовать даже в полупромышленных масштабах, что актуализирует вопрос о технологической валидности CBN как самостоятельного продукта.
Интересен также факт, что CBN, в отличие от большинства фитоканнабиноидов, имеет свою химическую историю, независимую от ферментативного происхождения. В 1940-х годах структура CBN была установлена на основе классических методов органической химии, в частности реакций нитрования, бромирования и соединения, без привлечения знаний о его биогенетической роли. Это означает, что CBN был выведен в химической плоскости раньше, чем THC — то есть ещё до открытия каннабиноидной биосинтетической системы в растениях. Позднее было доказано, что природное присутствие CBN в конопле является производной условий хранения, а не результатом непосредственного действия каннабиноидных синтаз.
Следует также отметить хемосистематическое значение CBN в фармакогностических исследованиях. Его накопление в образцах конопли позволяет реконструировать временную динамику химических преобразований в биомассе, в частности под воздействием ультрафиолетового излучения или длительного окислительного стресса. Это делает его маркером химического старения фитокомплексов и важным индикатором деградации других фитоканнабиноидов. В этом контексте роль CBN может быть сопоставима с оксидами терпеноидов в биомониторинге эфирных масел.
Отдельное внимание следует уделить его хиральным свойствам. Хотя CBN является ахиральной молекулой из-за наличия симметричного ароматического кольца, он образуется из хирального предшественника — Δ9-THC, который имеет несколько центров хиральности. При трансформации хиральная информация теряется, и это может служить ещё одним маркером химической деградации: потеря хиральности = потеря биосинтетической идентичности.
Наконец, следует упомянуть, что структура CBN имеет отношение к классу дифенольных тритерпенов, однако по ароматическому ядру он тяготеет к фенантреновой группе, характерной для многих лигандов рецепторов ЦНС. Этот структурный сдвиг от каннабиноидного типа к ароматическому контуру определяет уникальную рецепторную активность CBN, отличную от классических каннабиноидов, и заслуживает более глубокого изучения с точки зрения фармакофора.
Фитоканнабиноидный ландшафт: место CBN среди других соединений
Фитоканнабиноидный профиль Cannabis sativa включает более 120 идентифицированных соединений, которые классифицируются по структурному сходству с производными каннабигерола (CBG), каннабидиола (CBD), тетрагидроканнабинола (THC), канабихромена (CBC), а также их соответствующие карбоксилированные формы. На этом фоне CBN не входит в ни одну из основных синтетических линий, поскольку не происходит от CBGA по прямому энзиматическому пути, как это свойственно упомянутым классам. Вместо этого он формируется вторично через постсинтетические модификации, и потому его присутствие в химотипе не является предсказательной характеристикой генотипа растения.
С точки зрения хемотаксономии, CBN занимает нишу деградативных каннабиноидов. Его появление не является результатом энзимной активности, а следствием внешних условий, что отличает его от структурно связанных молекул, в частности Δ8-THC или канабицикла. Его молекулярная масса и распределение полярности влияют на фармакокинетику: сниженная липофильность по сравнению с THC способствует измененной способности к пересечению гематоэнцефалического барьера. В результате этого CBN можно рассматривать как пограничное соединение — между фитоканнабиноидами, активными в центральной нервной системе, и теми, которые действуют преимущественно периферийно.
CBN также интересен в контексте каннабиноидного спектра «второй волны» — группы соединений, которые формируются в процессе старения или техногенной обработки конопляного сырья. Вместе с такими компонентами, как канабиварин (CBV) или дегидроканнабиноиды, он позволяет реконструировать химическую эволюцию образца. Такой подход особенно ценен в фармакогностическом и токсикологическом анализе.
Окисление Δ9-THC: механизм образования канабинола
Автоокисление с участием кислорода
Механизм превращения Δ9-THC в CBN основан на радикальном автоокислении. Он начинается с абстрагирования атома водорода из алифатического цепочка Δ9-THC, преимущественно в положении C-11, с образованием стабилизированного алильного радикала. Этот промежуточный продукт реагирует с молекулярным кислородом (O₂), формируя пероксидный радикал, который через дальнейшие внутримолекулярные реорганизации трансформируется в ароматизированный хиноноидный каркас. Ключевым этапом является установление π-системы через окислительную дегидратацию.
Конечный продукт — CBN — является термодинамически стабильным благодаря полностью конъюгированной ароматической системе. Важно отметить, что этот путь не требует катализаторов и происходит даже при комнатной температуре, что подтверждено изотопно-маркерными исследованиями. В то же время процесс чрезвычайно чувствителен к присутствию воды, рН среды, а также уровню ультрафиолетового излучения, которое способно индуцировать альтернативные реакции фотопреобразования.
Светочувствительность и термолабильность ТГК
Δ9-THC является молекулой с выраженной фото- и термолабильностью из-за наличия двойных связей и хиральных центров в циклогексеновом фрагменте. Воздействие света, особенно в диапазоне 280–320 нм, способствует разрыву π-связей, образованию радикальных промежуточных продуктов и, в конечном итоге, реструктуризации в стабильный ароматический продукт.
Термическое разрушение Δ9-THC при температуре выше 70 °C активирует перегруппировку, что также ведет к образованию CBN. Этот путь особенно активируется в условиях ограниченного доступа к кислороду, где преобладают внутримолекулярные механизмы дегидрирования.
Исследования термокинетики показывают, что CBN образуется из Δ9-THC с конверсией до 90% за 72 часа при 100 °C в атмосфере воздуха. Напротив, при повышенном содержании влаги преобладает образование других деградационных продуктов, в частности хинонов или свободных альдегидов.
Альтернативные пути синтеза
Химический синтез CBN: история и современные подходы
Первые лабораторные синтезы CBN были проведены в 1940-х годах путем ароматизации структурно схожих прекурсоров. Например, реакция канабиолов с дихлордиметилхиноном или другими ароматизирующими агентами позволяла получить CBN с умеренной выходной способностью. Позднее использовались методы электрофильного замещения с последовательной дегидратацией для формирования ароматического ядра.
Современные подходы базируются на реакциях контролируемого окисления Δ9-THC в присутствии катализаторов на основе MnO₂, CrO₃, PCC (пиридин-хлорохромат), а также новейших органокатализаторов, таких как TEMPO. Каталитическое ароматизирование позволяет точно регулировать стехиометрию, что минимизирует образование побочных продуктов. Важным направлением также является селективное использование фотокатализа: введение фоточувствительных переносчиков электронов позволяет инициировать процессы дегидрирования с высокой эффективностью и без необходимости жестких температурных условий.
В области синтетической органической химии растет интерес к C-H функционализации как методу прямого преобразования аналогов Δ9-THC в CBN без необходимости предварительного получения THC. Такой подход может быть полезен для массового химического производства CBN из полусинтетических источников.
Биосинтетические модели: использование штаммов микроорганизмов
В отличие от традиционного биосинтеза канабиноидов через ферменты растительного происхождения (THCAS, CBDAS, CBCAS), CBN не имеет специфического фермента, который катализирует его образование. Однако современная биотехнология позволяет конструировать штаммы микроорганизмов (обычно Saccharomyces cerevisiae или Escherichia coli), способные продуцировать Δ9-THC, который затем подвергается индуцированному окислению до CBN в условиях in situ или ex vivo.
Исследовательские группы сосредоточены на создании штаммов, способных осуществлять контролируемое автоокисление или экспрессировать рекомбинантные пероксидазы, которые катализируют ароматизацию. Эксперименты с экспрессией бактериальных гидроксилаз в сочетании с окисляющими агентами показывают перспективы целевого синтеза CBN без необходимости выделения Δ9-THC как промежуточного продукта.
Отдельным направлением является использование генетически модифицированных культур Aspergillus niger, которые демонстрируют способность к ароматизации терпеноидов за счет эндогенных оксидаз. При определенных условиях культивации такие грибы могут быть использованы в качестве биокатализаторов для образования CBN из канабиноидных предшественников.
В отличие от классических химических методов, биосинтетические модели позволяют производить CBN с высоким уровнем чистоты без необходимости в жестких условиях или токсичных реагентах. Эти модели имеют преимущества в контексте «зеленой химии» и фармакологической стандартизации, что делает их привлекательными для будущего фармацевтического применения.
Методы получения и изоляции
Процессы получения и изоляции канабинола (CBN) из природных или синтетических источников представляют собой комплекс технологически сложных процедур, которые требуют точной регуляции условий, высокой химической специфичности и чувствительности к воздействию внешних факторов. Исторически CBN был первым изолированным каннабиноидом, и это обстоятельство обусловило раннее развитие методологий его получения, которые впоследствии были оптимизированы в соответствии с современными стандартами химической технологии, аналитики и фармацевтики. В то же время получение чистого CBN по-прежнему представляет собой значительную задачу как в лабораторных, так и в промышленных условиях из-за его вторичной природы, низкой концентрации в свежем растительном материале и структурной схожести с сопутствующими каннабиноидами.
Первичное сырьё для получения CBN чаще всего представлено высушенными цветками или экстрактами с высоким содержанием Δ9-тетрагидроканнабинола, поскольку CBN образуется в результате его окисления. Однако использование таких матриц связано с многочисленными аналитическими и процессуальными трудностями. Во-первых, значительное содержание липофильных веществ в натуральном экстракте усложняет специфическое выделение CBN без параллельного извлечения других компонентов. Во-вторых, CBN часто находится в экстрактах в форме нестабильных промежуточных продуктов или в связанном состоянии, что требует предварительной активации или трансформации матрицы.
По этой причине изоляция каннабинола почти всегда предполагает многоступенчатый подход, включающий предварительное фракционирование, селективное выделение, концентрирование и очистку. Экстракция обычно выполняется с использованием органических растворителей, которые демонстрируют высокую сродственность к фенольным и ароматическим структурам, таких как дихлорметан, этиловый ацетат или ацетонитрил. Отдается предпочтение условиям, которые не провоцируют дальнейшую деградацию термолабильных компонентов. В некоторых случаях используются сверхэкстрактивные технологии, в частности сверхкритическая CO₂-экстракция с модифицированными параметрами температуры и давления, адаптированными для обогащения фракций CBN.
Наиболее важным этапом в контексте высокой специфичности остаётся хроматографическое разделение. Традиционные методы, такие как флеш-хроматография на силикагелевой колонке, демонстрируют ограниченную разделительную способность при работе с каннабиноидными смесями, поэтому их обычно комбинируют с более современными подходами — препаративной ВЭЖХ, хроматографией с инверсией фаз или центрифужной распределительной хроматографией. Условия элюирования выбираются с учетом тонких различий в полярности и ароматичности между CBN и близкородственными структурами, в частности дегидрогенизированными производными ТГК и следами CBD.
Дополнительный уровень сложности возникает в случаях, когда CBN получают не из природных источников, а через синтетическую трансформацию прекурсоров. В таких случаях возникает потребность в тщательной очистке от побочных продуктов реакций, в частности полициклических ароматических углеводородов, которые могут образовываться в ходе окислительных или термических процессов. Методы очистки в таких контекстах включают молекулярную дистилляцию в вакууме, твердофазную экстракцию, а также использование микроколоночной электрофорезной сепарации, что позволяет разделять изомеры с минимальными потерями продукта.
Особого внимания требует контроль аналитической чистоты CBN, так как даже микроскопические примеси изомеров или частично окисленных остатков могут существенно повлиять на результаты дальнейших фармакологических или биохимических исследований. Поэтому процедуры очистки часто завершаются аналитическим контролем с помощью спектроскопии ядерного магнитного резонанса (ЯМР), масс-спектрометрии высокой разрешающей способности (HRMS), а также ультраэффективной жидкостной хроматографии с детекцией UV-Vis или DAD. Только после прохождения этих проверок материал считается пригодным для дальнейших экспериментов или фармацевтической разработки.
Химическое преобразование каннабиноидов в лабораторных условиях
Под воздействием контролируемых химических условий каннабиноиды, в частности Δ9-тетрагидроканнабинол (ТГК), могут быть преобразованы в каннабинол (CBN) с высокой выходной эффективностью. В лабораторной практике эти преобразования основываются на хорошо описанных механизмах ароматизации, дегидрогенизации и оксидативного разрыва связей в терпеновой части молекулы. Основным преимуществом такого подхода является воспроизводимость и возможность контроля над изомерационными процессами, которые часто осложняют природную деградацию ТГК.
Кислотные и основные среды
Использование кислотно-основного катализа позволяет ускорить или направить реакции преобразования ТГК в CBN в зависимости от выбранного реагента, концентрации и температуры. В кислой среде (например, с использованием хлористоводородной или серной кислоты) ТГК подвергается дегидратации, что способствует формированию стабильной ароматической системы, характерной для CBN. Особенно эффективным является использование мягких протонных кислот в неполярных растворителях при повышенной температуре (40–80°C), что обеспечивает контролируемую деградацию без излишней побочной полимеризации или образования хлорсодержащих артефактов.
В щелочной среде, особенно при использовании слабых оснований (например, бикарбоната натрия или органических аминов), основной реакцией является инициирование автокаталитической дегидрогенизации, при которой ТГК теряет два атома водорода и образует полностью конъюгированную ароматическую систему. Однако такой подход имеет более узкий диапазон рабочих условий, так как в щелочной среде могут образовываться нестабильные эпоксиды и пероксиды с потенциальной цитотоксической активностью.
Контролируемое старение ТГК
Моделирование условий старения ТГК в лаборатории позволяет смоделировать естественный путь образования CBN, но с гораздо большей эффективностью и управляемостью. Этот метод предполагает экспозицию раствора или полутвердого экстракта ТГК в присутствии кислорода, света или тепла в контролируемых режимах. Например, облучение ультрафиолетовым светом (λ = 254 нм) в атмосфере с ограниченным доступом влаги способствует селективному разрыву π-связей и образованию CBN с минимальным количеством побочных продуктов. Температурное старение (инкубация при 70°C в течение 2–5 дней) в сухом воздухе также показывает высокую эффективность, особенно когда процесс сочетается с периодическим перемешиванием в присутствии микроколичеств пероксидов или озона.
Методы экстракции CBN из растительного материала
Поскольку природное содержание CBN в свежих образцах Cannabis sativa обычно низкое, эффективная экстракция требует специализированных условий для сохранения целостности молекулы и минимизации потерь. Традиционные растворительные методы (этанол, гексан, хлороформ) позволяют получить только обогащенную фракцию, однако высокоселективные методики позволяют значительно повысить выход и чистоту CBN даже из материалов с низкой начальной концентрацией каннабинола.
Суперкритическая CO₂-экстракция с учетом деградации
Суперкритический диоксид углерода (CO₂) в сочетании с температурным или фотохимическим стимулом является мощным инструментом для выборочной экстракции каннабиноидов, в частности CBN. Ключевым параметром является регулирование давления и температуры так, чтобы активировать частичную деградацию ТГК в процессе экстракции — это позволяет не только получить CBN, но и повысить его концентрацию непосредственно в момент извлечения. В частности, условия при 31°C и 150–250 бар с добавлением модификатора (этанол 5–10%) способствуют обогащению экстракта CBN за счет термостимулированного образования. Преимущество этого метода заключается в чистоте полученного продукта, отсутствии остаточных токсичных растворителей и минимальном уровне термической деградации других соединений.
Хроматографическое разделение (HPLC, флеш-хроматография)
Для окончательного выделения CBN из экстракта применяются хроматографические методы с высокой разрешающей способностью. Высокоэффективная жидкостная хроматография (HPLC) с использованием C18-колонн в градиентном режиме позволяет разделять каннабиноиды, которые отличаются по ароматической насыщенности и гидрофобности. Модификаторы подвижной фазы — ацетонитрил, метанол с добавлением воды или уксусной кислоты — влияют на селективность, позволяя выделять CBN даже в присутствии большого количества ТГК-кислоты или других изомеров. В случае необходимости масштабного выделения применяется флеш-хроматография на силикагелях с постепенным повышением полярности элюента (гексан/этиловый ацетат), что позволяет эффективно отделить CBN от CBD, CBC и канабихромена без термического стресса.
Спектроскопическая идентификация
Из-за химической схожести каннабиноидов установление чистоты и подтверждение структуры CBN требует мультиспектрального подхода, который сочетает методы ЯМР, ИК и масс-спектрометрии. Особенно это актуально при работе с синтетическими аналогами или фракциями, где изомеры могут быть структурно неидентифицированы без детального анализа спектральных характеристик.
ЯМР (¹H, ¹³C), ИК-спектроскопия
Спектры ЯМР для CBN имеют четко выраженные сигналы, характерные для ароматических протонов (δ 6,2–7,1 ppm) и метильных групп (δ 1,2–1,6 ppm), которые отличаются от ТГК по сдвигам и мультиплетности. В ¹³C-ЯМР хорошо идентифицируются углеродные сигналы ароматического кольца (δ 120–160 ppm), что позволяет отличить CBN от CBD или CBC, даже при частичной деградации. ИК-спектры демонстрируют характерные поглощения в области 3400 см⁻¹ (–OH), 1600–1625 см⁻¹ (ароматическое ядро), а также 1260–1280 см⁻¹, что соответствует колебаниям C–O в фенольной части молекулы. Сопоставление этих спектров с библиотечными данными обеспечивает окончательную идентификацию.
Масс-спектрометрия (MS)
CBN демонстрирует характерный молекулярный ион с m/z 310 в спектрах EI-MS или GC-MS, что соответствует его молекулярной массе. Основными фрагментами являются ионы при m/z 295, 279 и 264, которые образуются в результате потери метильной, изопропильной или гидроксильной группы. В высокоразрешающей масс-спектрометрии (HRMS) фиксируются ионы с точностью до 4 десятичных знаков, что позволяет отличить CBN от его изомеров и потенциальных артефактов. Особое значение имеет применение тандемной масс-спектрометрии (MS/MS), которая позволяет идентифицировать внутримолекулярные фрагментации, включая потерю воды или CO-группы. Эти данные позволяют идентифицировать даже микродомешки в аналитических или фармацевтических препаратах на основе CBN.
Химические и физико-химические характеристики
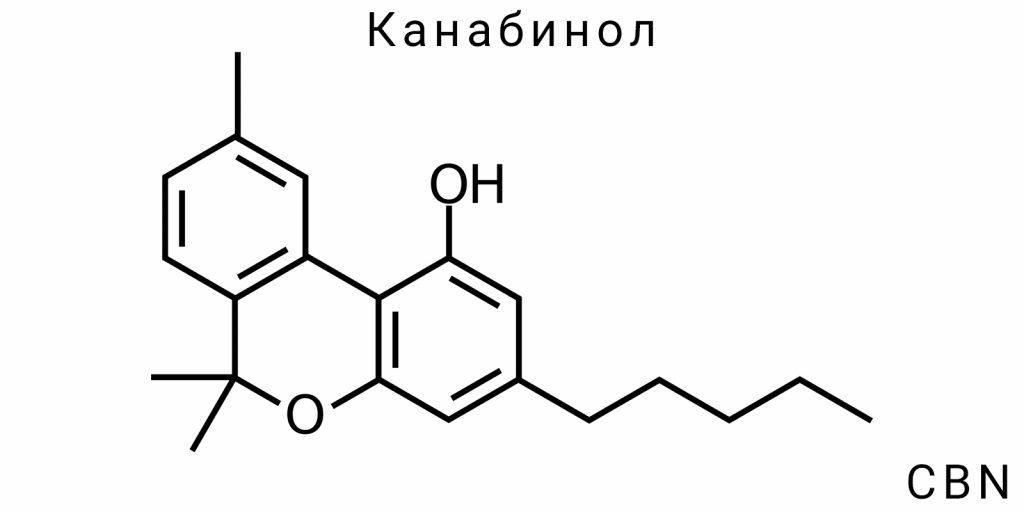
Каннабинол (CBN) относится к группе трициклических фенольных терпенофенолов и имеет уникальную ароматическую структуру, которая отличает его от других природных каннабиноидов не только с точки зрения биоактивности, но и химической поведения. Его молекулярная формула — C₂₁H₂₆O₂, а точная молекулярная масса — 310.43 г/моль. Структура CBN включает конъюгированную ароматическую систему, которая придает ему характерные электронные свойства и устойчивость к дальнейшему окислению по сравнению с менее ароматизированными каннабиноидами.
В отличие от Δ⁹-ТГК, структура CBN содержит полностью ароматизированное кольцо A, что приводит к усиленной плоскостности молекулы, увеличению электронной плотности в системе π-связей и потенциальной способности к межмолекулярному π–π-взаимодействию. Эти особенности являются решающими при кристаллизации, взаимодействии с носителями, мембранами или рецепторами, а также при изучении полимерных материалов на основе каннабиноидов.
CBN обычно кристаллизуется в виде бесцветных или светло-желтоватых игольчатых кристаллов с температурой плавления в пределах 76–77°C. Его растворимость сильно зависит от полярности растворителя: высокая в органических неполярных средах (гексан, хлороформ, диэтиловый эфир), ограничена в воде, но увеличивается в присутствии ПАВ или комплексообразующих веществ. Диэлектрическая постоянная молекулы находится в пределах, характерных для фенольных соединений, а значение logP — около 6.3, что указывает на высокий степень гидрофобности и преобладание накопления в липидных фазах.
Оптические свойства CBN определяются его конъюгированной системой, что проявляется в выраженном поглощении в ультрафиолетовой области спектра (λmax ≈ 282 нм). Этот максимум характерен для π→π* переходов в бензольных кольцах и используется для количественного анализа CBN с помощью УФ-детекции. В масс-спектрах и ЯМР-характеристиках каннабинол отличается четкой структурной сигнализацией, что позволяет отличить его от других изомеров, включая деградированные производные Δ⁹-ТГК.
CBN химически инертнее к реакциям гидратации, галогенирования или эпоксидирования на месте ароматического кольца, что усложняет его дальнейшую функционализацию без предварительного восстановления ароматической системы. В то же время активность фенольного гидроксила сохраняется, что позволяет осуществлять реакции этерификации, ацилирования, карбаматной защиты или образования простых и смешанных эфиров с полифункциональными молекулами.
Термодинамические параметры, такие как энтальпия плавления (~30 кДж/моль) и энтропия перехода в жидкое состояние, указывают на хорошо упорядоченную кристаллическую решетку и ограниченную способность к сублимации. При температуре выше 150°C CBN демонстрирует признаки термодеструкции, сопровождающейся декарбоксилированием, если присутствуют следы каннабиноловой кислоты или побочных продуктов с незавершенным ароматическим циклом. Его химическая стойкость увеличивается в анаэробной среде или в присутствии антиоксидантов, что позволяет прогнозируемо сохранять вещество в твердом состоянии без потери активности до 12 месяцев при температуре до 25°C.
Флуоресцентные свойства CBN еще не были полностью охарактеризованы, однако существуют сообщения о слабом излучении при возбуждении в диапазоне 290–310 нм, что открывает потенциал для применения в молекулярных трекинговых системах или биосенсорных платформах. По кислотно-основному поведению CBN действует как слабая кислота, pKa его фенольной гидроксильной группы составляет примерно 10.1, что аналогично крезолу и другим монофенолам. Это ограничивает его ионизацию при физиологическом pH и определяет низкую водорастворимость.
Химические взаимодействия с металлами, особенно с комплексообразующими центрами (Cu²⁺, Zn²⁺), могут приводить к образованию координационных комплексов с потенциальными биологическими функциями. Исследования таких комплексов являются актуальным направлением синтетической биоорганической химии каннабиноидов.
Молекулярная структура и стабильность
Молекулярная структура каннабинола (CBN) важна для определения его химических и физических свойств, которые, в свою очередь, влияют на стабильность этого соединения. CBN имеет молекулярную формулу C21H26O2, что указывает на 21 атом углерода, 26 атомов водорода и два атома кислорода. Как и другие каннабиноиды, CBN имеет циклическую структуру, включающую бензольное кольцо. Однако его отличие от других каннабиноидов, в частности от Δ9-THC, заключается в наличии гидроксильной группы (-OH), которая играет важную роль в определении его реакционной активности.
Одной из ключевых особенностей CBN является его термостабильность. Она выше, чем у Δ9-THC, что делает CBN более устойчивым к воздействиям внешней среды (высоким температурам, воздействию кислорода). Это означает, что CBN может быть более стабильным при хранении, по сравнению с Δ9-THC, который быстро распадается под воздействием света и температуры. Однако при длительном воздействии солнечного света или повышенных температурах CBN может деградировать до других метаболитов, таких как каннабидиол (CBD) или каннабихромен (CBC), которые также обладают различными фармакологическими эффектами.
С точки зрения химической стабильности, CBN подвержен окислению, поскольку его структура включает ароматическое кольцо, которое легко вступает в реакции с кислородом. Окисление CBN может привести к изменению его фармакологических свойств, таких как снижение анальгезирующего эффекта или изменение его взаимодействия с каннабиноидными рецепторами.
Сравнение с Δ9-THC и CBD
CBN, Δ9-THC и CBD — три ключевых каннабиноида, встречающихся в растениях каннабиса, однако их молекулярные структуры и фармакологические свойства существенно различаются. Δ9-THC является основным психоактивным компонентом, вызывающим изменения в сознании у пользователей каннабиса. В отличие от него, CBN имеет минимальные психоактивные свойства, так как его аффинность к рецептору CB1 значительно ниже. Это делает CBN перспективным кандидатом для терапевтического применения, где отсутствие психоактивных эффектов является важным.
CBD, с другой стороны, также является каннабиноидом, не обладающим психоактивной активностью, но имеющим значительный терапевтический потенциал. CBD обладает мощными противовоспалительными и анксиолитическими свойствами, а также проявляет антиоксидантную активность. В сравнении с CBN, CBD может иметь более широкий спектр применения, в частности при лечении тревожных расстройств, эпилепсии и хронической боли.
Хотя CBN не является психоактивным каннабиноидом, он имеет значительный потенциал для лечения ряда заболеваний, включая бессонницу, хроническую боль и воспалительные процессы. Одной из его основных особенностей является способность к стимуляции сна, что делает его потенциально полезным средством для людей, страдающих бессонницей.
Липофильность, растворимость, термостабильность
Липофильность CBN является важной характеристикой, так как она определяет его способность растворяться в жирорастворимых растворителях. CBN обладает высокой липофильностью, что делает его более доступным для экстракции с помощью органических растворителей, таких как этанол или гексан. Этот аспект позволяет получать высококонцентрированные экстракты каннабиноидов, которые могут использоваться в терапевтических целях.
Поскольку CBN является жирорастворимым, его растворимость в воде ограничена, что может повлиять на его биоактивность при пероральном введении. Для улучшения биоактивности CBN часто используют специальные методы доставки, такие как липосомальные системы, которые могут помочь каннабиноиду преодолеть водорастворимые барьеры и попасть в кровоток. Кроме того, наличие липофильных свойств позволяет использовать CBN для производства различных продуктов, таких как масла, настойки и кремы.
Что касается термостабильности, CBN может выдерживать температуры до 150°C без значительной деградации. Однако при длительном воздействии температуры выше 150°C, как в процессах декарбоксилирования или изготовлении экстрактов, часть CBN может превращаться в другие каннабиноиды или метаболиты. Это следует учитывать при разработке технологий обработки растительных экстрактов, чтобы сохранить максимально возможное количество активных компонентов.
Взаимодействие с кислотной средой (желудочно-кишечный тракт)
Пероральный прием CBN сопровождается сложными процессами его абсорбции и метаболизма в желудочно-кишечном тракте. Важным аспектом является то, что CBN, как и другие каннабиноиды, имеет ограниченную растворимость в воде, что затрудняет его абсорбцию в желудке. Кислотная среда желудка может влиять на молекулярную структуру CBN, в частности, на его способность образовывать водородные связи с другими молекулами.
Кислотность желудка может привести к частичному расщеплению или превращению CBN, что, в свою очередь, может изменить его биологическую активность. По этой причине большинство каннабиноидов, включая CBN, обладают низкой биоактивностью при пероральном приеме. Для улучшения абсорбции каннабиноидов обычно используют специальные формулы, которые стабилизируют их перед абсорбцией, такие как капсулы с контролируемым высвобождением или липосомальные системы.
Поскольку CBN не особенно стабилен в кислой среде, его фармакокинетика при пероральном приеме требует внимательного изучения. Это важно для разработки эффективных методов доставки, которые могут максимизировать его терапевтический эффект.
Фармакологический профиль CBN
Каннабинол (CBN) является одним из каннабиноидов, который, хотя и не вызывает выраженного психоактивного эффекта, обладает целым рядом важных фармакологических свойств, которые делают его интересным объектом для научных исследований и клинического применения. Взаимодействие CBN с каннабиноидными рецепторами CB1 и CB2 является основной причиной его фармакологической активности. При этом его способность вызывать менее выраженную психоактивность по сравнению с Δ9-THC делает его перспективным кандидатом для использования в медицинских целях, где требуется минимальное влияние на сознание и психику пациента.
CBN имеет слабую афинность к рецепторам CB1 по сравнению с THC, что означает, что он не вызывает сильных психотропных эффектов, таких как изменение сознания или эйфория. Однако он способен взаимодействовать с рецепторами CB2, которые в основном расположены в периферических тканях, таких как иммунные клетки, что придаёт CBN мощные противовоспалительные и обезболивающие свойства. Это позволяет использовать CBN в терапии хронических воспалительных заболеваний, таких как артрит, кожные заболевания или даже некоторые аутоиммунные болезни. Кроме того, CBN обладает умеренной анксиолитической активностью, что позволяет использовать его в лечении стресса и тревожных расстройств. Его способность снижать уровень тревожности может быть особенно полезной для пациентов с психоэмоциональными расстройствами, но без сильной медикаментозной зависимости, которая может возникнуть при применении традиционных антидепрессантов или успокаивающих средств.
Одним из наиболее изученных свойств CBN является его способность улучшать качество сна, хотя этот эффект менее выражен, чем у Δ9-THC. CBN обладает мягкими седативными свойствами, что может быть полезно для пациентов, страдающих бессонницей. Каннабинол может способствовать лучшему засыпанию, не вызывая при этом сильного опьянения, что характерно для THC. Однако исследования в этой области всё ещё продолжаются, и более точные данные о его влиянии на фазы сна требуют дальнейших клинических испытаний.
Противовоспалительные свойства CBN являются ещё одним важным аспектом его фармакологического профиля. Как каннабиноид, он способен снижать выработку воспалительных цитокинов, таких как интерлейкины, что может способствовать уменьшению воспаления в организме. Это особенно важно для лечения таких заболеваний, как хроническая боль, артрит, псориаз или другие дерматологические расстройства, а также для поддержания здоровья нервной системы при нейродегенеративных заболеваниях, таких как болезнь Альцгеймера или Паркинсона. Способность CBN модулировать иммунный ответ также делает его перспективным средством для лечения аутоиммунных заболеваний и хронических воспалительных процессов.
Ещё одной важной характеристикой CBN является его антиоксидантная активность. Благодаря своей способности нейтрализовать свободные радикалы, он может помочь снизить уровень окислительного стресса в организме, что является основной причиной развития многих хронических заболеваний, таких как сердечно-сосудистые болезни, рак, а также нейродегенеративные заболевания. Это делает CBN потенциально полезным как средство для профилактики и лечения таких заболеваний, хотя для более точного подтверждения этой способности необходимы дальнейшие исследования.
CBN также проявляет перспективы в лечении инфекций, его антибактериальные и антивирусные свойства могут быть полезными для борьбы с некоторыми бактериями и вирусами. Некоторые исследования показывают, что каннабинол может быть эффективным при лечении инфекций дыхательных путей или кожных инфекций, что делает его полезным для создания новых терапевтических стратегий, особенно в условиях, когда традиционные препараты не дают ожидаемого результата или имеют значительные побочные эффекты.
Особенностью фармакологического профиля CBN является то, что он взаимодействует с другими каннабиноидами, усиливая или изменяя их эффекты. Например, в комбинации с THC он может снижать интенсивность некоторых побочных эффектов, таких как тревожность или психоактивное влияние. Эта синергия между каннабиноидами является одним из важных направлений для дальнейших исследований, особенно в контексте разработки многокомпонентных терапевтических средств, которые обеспечивают баланс между эффективностью и безопасностью лечения.
Каннабинол также демонстрирует минимальные побочные эффекты по сравнению с более мощными каннабиноидами, такими как Δ9-THC, что делает его более безопасным для применения в терапевтических целях. Однако, как и все каннабиноиды, он может вызвать некоторые побочные эффекты, такие как вялость, сухость во рту или лёгкие изменения в когнитивных функциях, но эти эффекты обычно незначительны и исчезают после прекращения применения.
Взаимодействие CBN с другими лекарствами является важным аспектом, который требует более детального изучения. Поскольку он может влиять на метаболизм других препаратов путём ингибирования определённых ферментов печени, это может привести к изменению их концентрации в организме. Это важно учитывать при применении CBN у пациентов, которые принимают другие медикаменты, в том числе для лечения хронических заболеваний.
Аффинность к каннабиноидным рецепторам (CB1/CB2)
Каннабинол (CBN) обладает специфическими свойствами взаимодействия с каннабиноидными рецепторами CB1 и CB2, что определяет его фармакологическую активность и потенциальное клиническое применение. Основная характеристика CBN заключается в том, что он является частичным агонистом для CB2-рецепторов с довольно слабой активностью относительно CB1-рецепторов. Эти различия в взаимодействии с рецепторами указывают на значительные отличия в эффектах каннабиноида на центральную и периферическую нервную систему, а также на его потенциал в лечении различных патологических состояний.
- Взаимодействие с CB2-рецепторами
CB2-рецепторы в основном локализуются в периферических тканях, особенно в иммунных клетках, таких как макрофаги, лимфоциты и нейтрофилы. Они также присутствуют в некоторых органах, таких как печень, почки и кожа, а также в нервной системе, преимущественно в её периферических отделах. Афинность CBN к CB2-рецепторам относительно высокая, что позволяет ему эффективно модулировать различные иммунные и воспалительные процессы. Благодаря этому CBN способен реализовывать свои противовоспалительные и анальгезирующие эффекты. Взаимодействие с CB2 также обуславливает антиоксидантную активность CBN, что способствует снижению окислительного стресса и улучшению клеточной регенерации при хронических воспалительных заболеваниях.
В контексте терапевтического применения это имеет важное значение, поскольку активация CB2-рецепторов не вызывает выраженного психоактивного эффекта, характерного для CB1-рецепторов, поэтому CBN может быть полезным в лечении воспалительных заболеваний без риска для психического состояния пациента. Это особенно важно при лечении хронических болей, аутоиммунных заболеваний, таких как артрит, псориаз, или нейродегенеративных расстройств, таких как болезнь Альцгеймера, где воспаление играет ключевую роль в развитии патологии.
- Взаимодействие с CB1-рецепторами
Хотя CBN имеет относительно низкую активность к CB1-рецепторам, его способность взаимодействовать с этими рецепторами всё же имеет значение для его фармакологического профиля. CB1-рецепторы сосредоточены в центральной нервной системе, в частности в мозге и спинном мозге, где они регулируют множество функций, таких как восприятие боли, память, аппетит, эмоции и координация движений. Поскольку CBN имеет слабую афинность к CB1-рецепторам по сравнению с Δ9-THC, его влияние на центральную нервную систему намного менее выражено.
Таким образом, CBN не вызывает сильного психоактивного эффекта, что делает его более безопасным для использования в терапевтических целях, когда важно избежать любых нежелательных изменений в сознании или поведении пациента. Однако его способность взаимодействовать с CB1-рецепторами может объяснить его некоторые седативные эффекты, которые могут быть полезны при лечении бессонницы или тревожных расстройств. В то же время, CBN может помочь уменьшить некоторые побочные эффекты, связанные с высокими дозами THC, такие как тревожность или психоз, благодаря своему модулирующему воздействию на CB1-рецепторы.
- Механизм частичной агонистической активности
Каннабинол является частичным агонистом как для CB1, так и для CB2-рецепторов, однако его активность к этим рецепторам значительно различается. Частичный агонизм означает, что CBN, взаимодействуя с каннабиноидными рецепторами, вызывает субоптимальный эффект по сравнению с полным агонистом, таким как THC. Это позволяет CBN модулировать активность каннабиноидных рецепторов без чрезмерной активации, что снижает риск развития психоактивных или негативных эффектов, характерных для более мощных каннабиноидов.
Такое частичное агонистическое воздействие может быть полезным в контексте клинического использования, где контролируемое и сбалансированное воздействие на каннабиноидные рецепторы необходимо для достижения терапевтического эффекта без сильных побочных реакций. Например, его противовоспалительные эффекты могут быть достигнуты благодаря активации CB2-рецепторов, при этом минимизируя нежелательную психоактивность через слабое взаимодействие с CB1-рецепторами.
- Перспективы терапевтического применения
Слабая активность CBN на CB1-рецепторах, наряду с его значительной афинностью к CB2-рецепторам, делает его интересным кандидатом для лечения воспалительных и аутоиммунных заболеваний без риска для психического состояния пациентов. Кроме того, CBN может стать частью комбинированных терапий с другими каннабиноидами или фармакологическими агентами для достижения более эффективного результата без риска развития зависимости или психоза. Поэтому изучение афинности и активности CBN к каннабиноидным рецепторам CB1 и CB2 имеет значительный потенциал для создания новых терапевтических стратегий, особенно для пациентов с хроническими воспалительными заболеваниями, болью, нейродегенерацией и расстройствами сна.
Нейрофармакологические эффекты
Каннабинол (CBN) по своей природе обладает специфическими нейрофармакологическими свойствами, что делает его предметом многочисленных исследований, направленных на изучение его потенциальных терапевтических возможностей. Однако в научной среде существует ряд споров относительно того, вызывает ли CBN выраженный седативный эффект, а также насколько обоснованы его нейропротекторные свойства.
Седация: миф или обоснованный эффект?
Седация является одним из эффектов, на который многие обращают внимание при исследовании каннабиноидов, и хотя на первый взгляд эффект CBN на центральную нервную систему может выглядеть очевидным, его седативная природа не является такой явной, как у других каннабиноидов, в частности Δ9-THC. CBN способен влиять на состояние пациента через свою частичную активацию CB1-рецепторов, однако его воздействие на эти рецепторы значительно слабее по сравнению с Δ9-THC, поэтому его седативный эффект часто описывается как умеренный и менее выраженный.
Слабая активность CBN на CB1-рецепторах является важным аспектом, поскольку именно этот тип рецепторов связан с психоактивными и седативными свойствами каннабиноидов. Вместо того чтобы сильно активировать эти рецепторы, CBN, вероятно, действует как частичный агонист, что может снижать уровень стресса и тревожности без значительных изменений в эмоциональном состоянии или когнитивных функциях. Научные исследования показывают, что CBN может иметь умеренные успокаивающие свойства, что делает его полезным в контексте лечения тревожных расстройств или бессонницы, однако он, вероятно, не способен вызвать мощное седативное воздействие, как это может быть с THC.
В то же время, некоторые исследования указывают, что при более высоких дозах CBN может проявлять более выраженный седативный эффект. Однако эти данные требуют дальнейшего изучения для лучшего понимания механизмов его действия на центральную нервную систему. Поэтому, хотя седация является частью его нейрофармакологического профиля, эффект CBN нельзя характеризовать как основную или выраженную особенность, и его следует воспринимать в контексте умеренного действия.
Потенциальные нейропротекторные свойства
Одной из основных сфер исследований в контексте CBN является изучение его нейропротекторных свойств. Нейропротекция относится к способности вещества снижать повреждения нейронов и нейропротекторных тканей, сохраняя нормальную функцию нервной системы. CBN продемонстрировал потенциал в снижении оксидативного стресса, который является одним из основных факторов развития нейродегенеративных заболеваний, таких как болезнь Альцгеймера и Паркинсона.
Механизм нейропротекции CBN предполагает его антиоксидантные свойства, которые позволяют ему эффективно нейтрализовать свободные радикалы и снижать уровень оксидативного стресса, который может быть причиной повреждения нейронов. Как частичный агоніст CB2-рецепторов, CBN может иметь противовоспалительный эффект, снижая воспаление в нервной системе. Воспаление играет ключевую роль в развитии многих нейродегенеративных заболеваний, поэтому способность CBN модулировать активность иммунных клеток может помочь замедлить прогрессирование этих заболеваний.
Нейропротекторное действие CBN также может быть результатом его воздействия на клеточную стрессовую реакцию. Исследования показали, что CBN способен способствовать восстановлению функций нейронов после повреждений, вызванных токсинами или инфекциями, что также придает ему потенциал в лечении травм головного и спинного мозга. Его влияние на нейропластичность может быть особенно полезным при лечении расстройств, связанных с потерей или повреждением нейронов.
Нейропротекция CBN может также быть связана с его способностью снижать уровень нейротоксичных соединений в нейронах. Он может помочь уменьшить риск апоптоза (программируемой гибели клеток), что имеет важное значение для восстановления функций после нейродегенерации. Кроме того, его способность к активации антиоксидантных путей, таких как активация системы глутатиона, может способствовать уменьшению повреждений, вызванных оксидативным стрессом.
Влияние на иммунный ответ и воспаление
Канабинол (CBN) является одним из канабиноидов, который проявляет значительное влияние на иммунную систему. Его способность модулировать иммунный ответ делает его интересным объектом для исследований, направленных на терапевтическое использование в контексте хронических воспалительных заболеваний, аутоиммунных болезней и других нарушений, связанных с дисфункцией иммунной системы.
CBN имеет особую способность активировать CB2-рецепторы, которые являются основными рецепторами, влияющими на иммунные клетки. Этот механизм важен, так как активация CB2-рецепторов обычно ведет к снижению воспалительных процессов. В результате CBN способен снижать активность иммунных клеток, таких как Т-лимфоциты и макрофаги, которые обычно играют ключевую роль в развитии воспаления. Таким образом, CBN может иметь противовоспалительные свойства, которые потенциально могут быть полезными при лечении заболеваний, таких как артрит, болезни кишечника, ревматоидный артрит и даже некоторые кожные болезни, связанные с хроническими воспалениями.
Кроме того, CBN способен снижать уровень прозапальных цитокинов, таких как TNF-α, интерлейкин-6 и другие молекулы, способствующие активации иммунных клеток и ведующие к усилению воспалительного процесса. Это указывает на то, что CBN может выступать как ингибитор воспалительных механизмов, снижая уровень хронического воспаления и связанных с ним симптомов. Однако для подтверждения этих эффектов необходимо провести дополнительные клинические исследования, так как текущие данные ограничены результатами исследований на животных и лабораторными испытаниями.
Метаболизм и биодоступность
Метаболизм CBN является сложным процессом, включающим многочисленные этапы трансформации в организме, включая метаболизм в печени и участие различных ферментов. Основными механизмами метаболизма CBN являются окисление, конъюгация с глюкуроновой кислотой и сульфатами. Канабиноиды, включая CBN, активно метаболизируются в печени через систему ферментов, известную как CYP450 (цитохром P450). Эти ферменты играют важную роль в метаболизме практически всех канабиноидов, поскольку они осуществляют окисление молекул до активных метаболитов, которые могут иметь различные фармакологические эффекты.
CBN метаболизируется преимущественно через ферменты CYP2C9 и CYP3A4, хотя и другие ферменты также могут участвовать в этом процессе. Это имеет важное значение для клинического применения CBN, так как взаимодействие с другими лекарствами, которые метаболизируются через эти же ферменты, может привести к изменениям в эффективности и токсичности препарата. Например, прием CBN вместе с другими препаратами, которые ингибируют CYP2C9 или CYP3A4, может увеличить уровень CBN в организме, что может привести к повышению его эффектов или побочных реакций. С другой стороны, стимуляция этих ферментов может ускорить метаболизм CBN и снизить его эффективность.
Что касается биодоступности, канабиноиды обычно имеют низкую биодоступность при пероральном приеме из-за эффекта «первого прохождения» через печень, когда значительная часть активного соединения метаболизируется еще до того, как попадет в системный кровоток. Биодоступность CBN при пероральном введении может быть еще ниже из-за низкой растворимости в воде и большой молекулярной массы, что ограничивает его проникновение через клеточные мембраны. Это делает применение CBN в форме масляных или липофильных препаратов более эффективным способом доставки в организм.
Кроме того, биодоступность CBN может варьировать в зависимости от способа введения. Например, при ингаляционном введении (через курение или выпаривание) биодоступность значительно выше, поскольку CBN попадает непосредственно в кровоток через легкие, минуя эффект первого прохождения через печень. Это позволяет достичь более быстрого и сильного эффекта, что делает ингаляцию одним из наиболее эффективных способов введения канабиноидов, включая CBN. Тем не менее, ингаляционное введение имеет свои риски, связанные с воздействием на легкие и дыхательные пути, что требует осторожности при использовании этого метода.
Сравнение перорального и ингаляционного введения CBN показывает значительные различия в их биодоступности и фармакокинетике. Пероральное введение CBN обычно имеет более продолжительный срок начала действия, так как активные метаболиты должны пройти через печень перед тем, как попасть в кровь. Ингаляция, в свою очередь, обеспечивает более быстрый эффект и большую биодоступность, но эффект может быть короче по продолжительности, поскольку канабиноид быстро метаболизируется.
Потенциальные области применения
Предклинические исследования
Предклинические исследования каннабиноидов, включая каннабиниол (CBN), проводятся на различных животных моделях, что позволяет оценить возможные терапевтические эффекты и безопасность этого каннабиноида до перехода к клиническим испытаниям на людях. Для исследований CBN часто используют модели мышей, так как эти животные играют важную роль в изучении фармакологических свойств и механизмов действия каннабиноидов благодаря их генетическому сходству с людьми и установленным методам тестирования.
Одним из основных направлений исследований является оценка воздействия CBN на нейрофармакологические эффекты, включая потенциал для седативного действия и изменения аппетита. Так, в ряде исследований было показано, что CBN способен вызывать седативный эффект, который, хотя и менее выражен по сравнению с Δ9-THC, тем не менее, проявляется заметно при определенных дозах. Животные, получавшие CBN, демонстрировали снижение активности, что позволяет предположить, что этот каннабиноид может иметь потенциал для применения в условиях, связанных с нарушениями сна или повышенной тревожностью.
Кроме того, CBN стал объектом исследований, направленных на изучение его воздействия на аппетит. Известно, что некоторые каннабиноиды, в частности Δ9-THC, обладают выраженным аппетитогенным действием, но относительно CBN данные ограничены. Тем не менее, зафиксировано, что CBN способен модулировать поведение, связанное с приемом пищи у животных, хотя этот эффект по сравнению с другими каннабиноидами не является столь выраженным.
Противовоспалительные свойства CBN являются еще одним направлением, активно изучаемым в рамках предклинических исследований. Множество исследований показали, что CBN способен снижать уровень прозапальных цитокинов и молекул, таких как TNF-α и интерлейкин-6, что подтверждает потенциал этого каннабиноида для использования при лечении воспалительных заболеваний, таких как артрит, заболевания кишечника и кожные патологии, сопровождающиеся хроническим воспалением.
Клинические перспективы
Переход от предклинических исследований к клиническим испытаниям является важным этапом в разработке новых лекарственных средств, и CBN не является исключением. Однако существует ряд барьеров для трансляционной медицины, которые усложняют применение CBN в клинической практике. Одним из таких барьеров является недостаточно исследованная безопасность и эффективность CBN для человеческого организма. Поскольку исследования, касающиеся каннабидиола, часто ограничены животными, многие аспекты фармакокинетики и фармакодинамики каннабиноида, такие как оптимальные дозы, способы введения и возможные побочные эффекты, остаются недостаточно изученными.
Нормативное регулирование является еще одним существенным барьером для клинического использования CBN. Во многих странах каннабиноиды находятся под строгим контролем, и их использование ограничивается определенными условиями. Этот аспект особенно касается регулирования наркотических средств и их лекарственных форм, где существуют юридические ограничения относительно их применения в медицинских целях. Кроме того, специфика регулирования может значительно различаться в зависимости от страны, что усложняет процесс получения разрешений на проведение клинических исследований или продажу каннабиноидов в качестве лекарственных средств.
Еще одной проблемой является недостаточное количество клинических испытаний, изучающих эффекты CBN на людях. Имеющиеся данные в основном являются результатами исследований на животных или случайных наблюдений. Это означает, что необходимо провести широкие, рандомизированные клинические исследования для подтверждения эффективности и безопасности этого каннабиноида для лечения конкретных заболеваний или симптомов. Только после получения доказательств эффективности и безопасности, а также после определения оптимальных доз и способов введения, CBN может стать доступным для широкого клинического применения.
Роль CBN в полифармакологии каннабиноидов
Полифармакология каннабиноидов, в частности эффект «энтourage» (эффект «сопровождения»), является важным аспектом, который требует более детального изучения в контексте применения CBN. Эффект «сопровождения» предполагает, что взаимодействие различных каннабиноидов, терпенов и других молекул в каннабисе может усиливать или модулировать терапевтические эффекты этих соединений, обеспечивая более эффективное лечение. В случае CBN этот эффект может проявляться в комбинации с другими каннабиноидами, такими как Δ9-THC, CBD или даже с другими фитохимическими веществами, содержащимися в каннабисе.
Например, некоторые исследования показывают, что сочетание CBN с другими каннабиноидами может усилить его противовоспалительную или нейропротекторную активность, а также снижать потенциально негативные эффекты, связанные с приемом Δ9-THC, такие как параноидные реакции или тревожность. Это позволяет утверждать, что использование комбинаций каннабиноидов в лечении может быть более эффективным по сравнению с применением отдельных молекул.
Кроме того, изучение синергизма между различными каннабиноидами имеет важное значение для оптимизации терапевтических схем. Роль CBN в таких комбинациях может быть различной в зависимости от терапевтической цели: он может выступать как основное активное вещество или как вспомогательный агент для усиления эффекта других каннабиноидов.
Этические, экологические и правовые аспекты производства каннабиноидов
Производство CBN как продукта деградации: утилизация или ценный ресурс?
Каннабидиол (CBN) традиционно считается продуктом деградации Δ9-THC (тетрагидроканнабинола), основного психоактивного компонента каннабиса. Его образование в результате окисления и старения THC под воздействием кислорода и света открывает новые возможности для изучения CBN как потенциального продукта с терапевтическими свойствами. Однако вопрос, является ли CBN лишь побочным продуктом с ограниченным применением или его можно рассматривать как полноценный ресурс, вызывает интерес у ученых, производителей и законодателей.
Использование CBN как ценного ресурса требует оценки его экономической целесообразности, а также этических аспектов. Поиск путей эффективной утилизации CBN из растительного материала, не соответствующего стандартам для производства более известных каннабиноидов, таких как Δ9-THC или CBD (каннабидиола), становится важным направлением исследований. Учитывая высокий спрос на каннабиноиды и их производные, в будущем может стать возможной технология переработки «стареющих» каннабисных растений для получения CBN, что позволит снизить экологический след каннабисной промышленности.
Однако этот вопрос поднимает также экологические и этические вопросы. С одной стороны, каннабиноиды, образующиеся в результате деградации, могут иметь меньший влияние на окружающую среду по сравнению с другими методами синтеза. Но с другой стороны, необходимость большого объема сырья для образования таких соединений может создать экологические проблемы, связанные с выращиванием и обработкой растений. Превышение уровня экологического воздействия, вызванного масштабным использованием природных ресурсов, может привести к снижению устойчивости производственных цепочек.
Что касается этической стороны, важно учитывать правомерность и ответственность при использовании биологических ресурсов. Переход к широкомасштабному использованию CBN как продукта деградации может создать новые этические дилеммы в отношении прав на ресурсы и контроля за использованием генетических данных каннабиса. Производители должны учитывать возможные риски монополизации на рынке каннабиноидов, а также обеспечить равный доступ к этим ресурсам для малых и средних производителей.
Биоэтика синтетических каннабиноидов
Синтетические каннабиноиды, к которым относится также синтетический CBN, становятся важной частью современной фармакологии и медицины. Однако использование синтетических каннабиноидов вызывает ряд этических вопросов, касающихся не только их безопасности, но и моральных аспектов применения новейших технологий для создания молекул, имитирующих природные соединения каннабиса. Синтетические каннабиноиды позволяют контролировать молекулярные структуры с большей точностью, однако с их появлением возникает угроза несанкционированного использования и потенциального вреда для здоровья потребителей из-за несоответствия необходимым стандартам качества или приема в дозах, значительно превышающих безопасные уровни.
Кроме того, синтетические каннабиноиды могут иметь значительно большую аффинность к каннабиноидным рецепторам по сравнению с природными соединениями, что может привести к усилению или развитию нежелательных эффектов, таких как психотические реакции или тяжелые кардиоваскулярные расстройства. Это требует тщательного контроля за исследованиями и регулированием, чтобы обеспечить как безопасность, так и этическую ответственность при использовании синтетических каннабиноидов в медицинских и промышленных целях.
Этические вопросы также возникают в контексте использования синтетических каннабиноидов для создания новых фармацевтических продуктов, поскольку синтетические аналоги могут снижать природное разнообразие биоресурсов и заменять традиционные методы лечения. Согласно биоэтическим принципам, важно сохранять природные ресурсы и избегать замены их синтетическими веществами без должных оснований или доказательств эффективности.
Правовые коллизии относительно «непсихоактивных» производных
Правовой статус каннабиноидов и их производных, включая CBN, является одной из самых сложных и противоречивых тем в области наркополитики и медицины. Особенно важным является вопрос правового определения «непсихоактивных» производных каннабиноидов. Учитывая, что CBN не обладает выраженной психоактивной активностью, он иногда попадает в категории веществ, разрешенных к использованию в медицинских целях. Однако в некоторых странах существуют законодательные ограничения относительно каннабиноидов, даже если они не обладают психоактивным действием, что может создавать правовые трудности для их производства и распространения на рынке.
Поскольку CBN является продуктом деградации Δ9-THC, это дополнительно усложняет правовую ситуацию, так как в некоторых юрисдикциях все каннабиноиды, даже те, которые не вызывают наркотических эффектов, подлежат строгому контролю. Это приводит к необходимости детального рассмотрения правовых норм, определяющих, какие именно каннабиноиды можно использовать для медицинских и промышленных целей. Возможно, будущие законодательные инициативы должны быть направлены на уточнение критериев для классификации каннабиноидов и их производных в зависимости от их воздействия на центральную нервную систему, а также на определение четких границ для разрешенного использования таких соединений.
Правовые коллизии могут возникать и в случае, когда каннабиноиды, не подпадая под определение психоактивных веществ, все равно подлежат регулированию с учетом их происхождения от растения каннабис. Учитывая эти правовые барьеры, многие производители, стремящиеся коммерциализировать CBN и другие каннабиноиды, сталкиваются с проблемами получения лицензий или разрешений на выпуск продукции на рынок. Это подчеркивает необходимость унификации правовых норм на международном уровне для облегчения процесса исследований и разработки новых медицинских и фармацевтических продуктов.
Вывод
В данной статье был проведен детальный анализ различных аспектов каннабидиола (CBN), начиная от его химического происхождения и синтетических путей до фармакологических свойств и возможных направлений применения. Отмечено, что CBN, как один из каннабиноидов, активно исследуется не только в контексте его терапевтического потенциала, но и с точки зрения экологической и правовой регламентации. Возможности его использования в медицинских целях, в частности для снижения воспаления, облегчения боли и нейропротекции, открывают новые горизонты в контексте лечения различных патологий, хотя и требуют дальнейших исследований для подтверждения эффективности и безопасности.
Одной из ключевых тем, обсуждавшихся в статье, стало сравнение CBN с другими каннабиноидами, такими как Δ9-THC и CBD. Выявлено, что хотя CBN имеет слабую психоактивную активность и отличается от этих соединений, его био-фармакологический профиль демонстрирует интересные преимущества, в частности в контексте взаимодействия с каннабиноидными рецепторами и потенциально полезных эффектов для нервной и иммунной системы.
Не менее важным аспектом является анализ методов получения CBN, который включает как биосинтетические, так и химические подходы. Деградация THC в процессе старения и окисления, а также инновационные методы экстракции и хроматографии открывают новые возможности для извлечения и очистки CBN из растительного материала, что способствует его коммерциализации и применению в фармацевтике.
Вместе с тем, ряд этических, экологических и правовых вопросов, возникающих в контексте производства и использования CBN, требуют тщательного регулирования. Законодательные ограничения относительно каннабиноидов и производных каннабиса, а также неполный правовой статус CBN как «непсихоактивного» компонента, являются значительным барьером для его широкого внедрения в медицинскую практику и коммерциализацию.
Несмотря на прогресс в понимании биологических и фармакологических свойств CBN, существует необходимость проведения дополнительных исследований на уровне доклинических и клинических испытаний, чтобы подтвердить его безопасность, эффективность и возможные побочные эффекты. Отсутствие масштабных клинических исследований делает понимание реальных возможностей этого каннабиноида еще недостаточно определенным.
Источники:
- National Center for Biotechnology Information (NCBI) https://www.ncbi.nlm.nih.gov/
Официальный сайт, который содержит множество научных статей и исследований, в том числе по каннабиноидам, таким как CBN. - PubMed Central https://www.ncbi.nlm.nih.gov/pmc/
Платформа с открытым доступом к научным публикациям по медицине, биологии и химии. Для конкретных статей о каннабиноидах и CBN можно найти ссылки через ключевые слова. - The Journal of Pharmacology and Experimental Therapeutics https://jpet.aspetjournals.org/
Известный научный журнал, публикующий исследования по фармакологии, включая каннабиноиды и их влияние на рецепторы CB1 и CB2. - Nature Reviews Drug Discovery https://www.nature.com/nrd/
Журнал, который содержит обзоры и статьи о фармакологических свойствах каннабиноидов, их биосинтезе и влиянии на различные органы. - Frontiers in Pharmacology https://www.frontiersin.org/journals/pharmacology
Это открытый доступ к статьям и исследованиям на тему фармакологии, где можно найти исследования по терапевтическим эффектам каннабиноидов. - The Lancet Psychiatry https://www.thelancet.com/journals/lanpsy
Журнал с открытым доступом, который публикует исследования о психиатрических эффектах каннабиноидов и их роли в лечении неврологических и психических заболеваний. - Cannabis and Cannabinoid Research https://www.liebertpub.com/can
Известный журнал, который публикует оригинальные исследования, связанные с каннабисом и каннабиноидами, включая CBN. - Harvard University — Department of Neurobiology https://neuro.hms.harvard.edu/
Известный научный институт с ресурсами и исследованиями в области нейробиологии, где проводятся исследования, связанные с каннабиноидами. - U.S. National Institute on Drug Abuse (NIDA) https://nida.nih.gov/
Официальный сайт, публикующий материалы и исследования о каннабиноидах, их эффектах на человеческий организм и психику. - American Chemical Society (ACS) https://www.acs.org/
Организация, которая публикует научные исследования в области химии, в том числе в области каннабиноидов и химических свойств CBN.