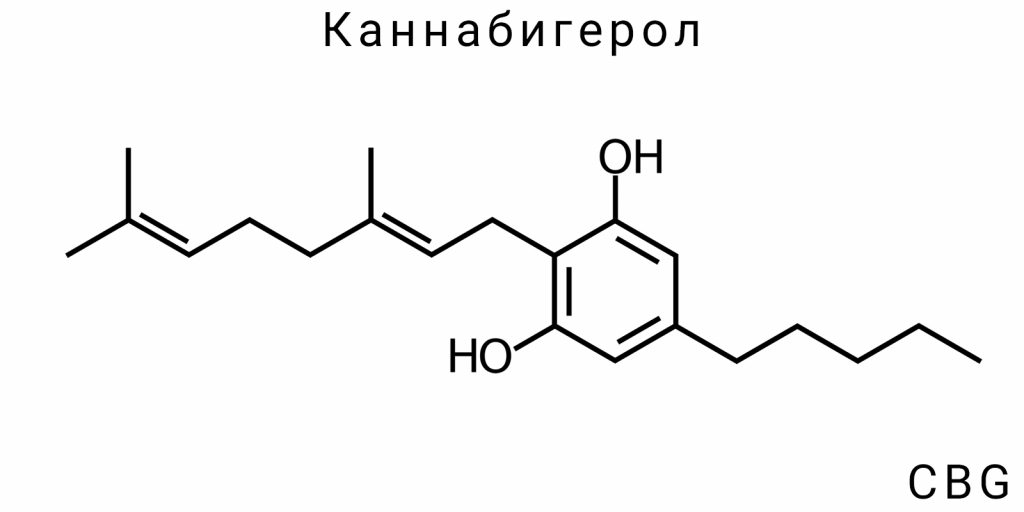
На протяжении последних десятилетий каннабиноиды, биологически активные соединения, которые естественным образом содержатся в Cannabis sativa L., стали объектом масштабных научных исследований. Основное внимание было сосредоточено на Δ⁹-тетрагидроканнабиноле (THC) и каннабидиоле (CBD), обладающих хорошо изученным фармакологическим профилем. Однако в растении присутствуют и другие, менее распространённые каннабиноиды, демонстрирующие уникальные биологические свойства. Одним из таких соединений является каннабигерол (CBG) — непсихоактивное вещество, служащее метаболическим предшественником THC, CBD и CBC в биосинтетическом каскаде каннабиноидов.
CBG синтезируется в виде кислотного предшественника — каннабигероловой кислоты (CBGA), которая с участием ферментов циклизуется в другие основные каннабиноиды. Из-за этого в зрелых растениях концентрация свободного CBG, как правило, не превышает 1%, что исторически затрудняло его изучение. Однако современные биотехнологические подходы позволяют получать CBG в достаточных количествах, открывая новые перспективы для исследования его противовоспалительного, нейропротекторного, антибактериального и потенциально противоопухолевого действия.
В настоящее время интерес к CBG обусловлен не только его уникальным фармакологическим профилем, но и низкой психоактивностью, что делает его перспективным кандидатом для клинического применения в сферах, где традиционные каннабиноиды имеют ограничения.
Происхождение и химическая характеристика каннабигерола (CBG)
Каннабигерол (CBG) является одним из первичных каннабиноидов, встречающихся в растениях Cannabis sativa. Это молекула, являющаяся частью сложного биохимического пути в метаболизме каннабиса, в котором каннабигерол играет роль предшественника большинства других каннабиноидов, таких как Δ⁹-THC и CBD. Важной особенностью CBG является его способность служить матрицей для дальнейших превращений, происходящих в растении. Это придаёт CBG ключевое значение для понимания того, как каннабиноиды с важными терапевтическими свойствами образуются в растении.
Что касается его химической структуры, CBG имеет молекулу с 21 атомом углерода, 30 атомами водорода и одним атомом кислорода, что позволяет отнести его к классу фитоканнабиноидов, которые обычно включают фенольное кольцо и гидрофобную алкильную цепь. Отличительной чертой CBG является наличие гидроксильной группы (-OH) в определённой позиции молекулы, что делает его более полярным по сравнению с другими каннабиноидами, такими как THC или CBD. Это имеет важное значение для его биологической активности и взаимодействия с различными рецепторами в организме.
Одной из важных характеристик CBG является его биологическая активность на молекулярном уровне, что позволяет ему обладать потенциалом для лечения широкого спектра заболеваний — от нейродегенеративных расстройств до воспалительных процессов. Однако его содержание в растениях каннабиса, как правило, очень низкое, что ограничивает возможности для массового использования. Для повышения концентрации CBG в растениях применяются специальные методы селекции и генной инженерии.
Биосинтез CBG: переход от CBGA к CBG
Биосинтез CBG в растениях каннабиса начинается с образования каннабигероловой кислоты (CBGA), которая является предшественником всех основных каннабиноидов, таких как THC, CBD и CBC. CBGA синтезируется путём соединения двух молекул: оливитоловой кислоты и геранилдифосфата (GPP), которые служат предшественниками каннабиноидной структуры. Этот этап происходит под действием фермента каннабигероловой синтазы, катализирующего их соединение.
После образования CBGA он далее превращается в CBG. Это происходит через процесс декарбоксилирования, при котором от молекулы CBGA отщепляется карбоксильная группа (-COOH). Для этого необходим фермент каннабигероловой кислоты декарбоксилаза (CBGA-DC). Результатом этого процесса становится нейтральный каннабиноид CBG, играющий важную роль в фармакологии.
Стоит отметить, что после образования CBG этот каннабиноид может трансформироваться в THC или CBD в зависимости от действия других специфических ферментов, таких как Δ⁹-THC-синтаза или CBD-синтаза. Это делает CBG уникальным по своей роли, поскольку через него осуществляется синтез основных каннабиноидов. Однако CBG также может действовать независимо от превращения в другие каннабиноиды, обладая собственными терапевтическими свойствами.
Структурные особенности CBG
Молекула каннабигерола включает фенольное кольцо, которое является общей структурной единицей для всех каннабиноидов. Это кольцо обеспечивает способность молекулы взаимодействовать с каннабиноидными рецепторами в организме, в частности с рецепторами CB1 и CB2, являющимися частью эндоканнабиноидной системы. Ещё одной характерной особенностью является наличие длинной углеродной цепи, позволяющей молекуле проникать через биологические мембраны и взаимодействовать с клетками.
Молекула CBG содержит гидроксильную группу (-OH), придающую молекуле полярность. Это позволяет CBG быть менее гидрофобным по сравнению с другими каннабиноидами, такими как THC, что важно для его способности растворяться в водных средах и взаимодействовать с водными компонентами клеток. Гидроксильная группа также может способствовать стабильности молекулы и влиять на её реакции с другими биологическими молекулами.
Каннабигерол не является полностью стабильным в растении. Он может разлагаться или превращаться в другие каннабиноиды под воздействием температуры, света или определённых ферментов. Это важно для его потенциального медицинского использования, поскольку условия хранения и производства CBG могут существенно влиять на его эффективность.
Сравнение с другими фитоканнабиноидами
Сравнение CBG с другими каннабиноидами, такими как THC и CBD, важно для понимания его уникальных свойств и терапевтического потенциала. CBG отличается от THC тем, что является непсихоактивным каннабиноидом. Это означает, что он не вызывает характерного для THC эффекта «эйфории», а потому может быть более безопасным для широкого медицинского применения, особенно при лечении хронических воспалительных заболеваний, нейродегенеративных расстройств, а также некоторых видов рака.
CBD, хотя и не является психоактивным, имеет иные механизмы действия по сравнению с CBG. Например, CBD взаимодействует с серотониновыми рецепторами, что придаёт ему успокаивающие свойства, тогда как CBG оказывает более непосредственное воздействие на каннабиноидные рецепторы CB1 и CB2, что позволяет ему обладать более выраженными противовоспалительными и антиоксидантными свойствами.
CBG также обладает большим потенциалом в лечении инфекций, поскольку проявляет эффективность в борьбе с бактериями, в частности с некоторыми штаммами, устойчивыми к антибиотикам. Это делает его перспективным для использования в терапии инфекционных заболеваний, особенно в условиях роста устойчивости к антибиотикам.
Методы получения CBG
Получение каннабигерола (CBG) является критически важным этапом в фармацевтическом, биотехнологическом и аграрном секторах, поскольку это соединение демонстрирует широкий спектр потенциальных биологических активностей. Несмотря на сравнительно невысокую популярность по сравнению с тетрагидроканнабинолом (THC) или каннабидиолом (CBD), CBG рассматривается как перспективный терапевтический агент, а также важное сырьё для дальнейшего химического синтеза каннабиноидов. Его низкая концентрация в природных источниках требует применения высокотехнологичных подходов к извлечению или синтезу. В данном разделе будут рассмотрены и проанализированы основные методы получения CBG: природная экстракция, синтетические технологии, ферментативные методы, а также биоинженерные подходы, включая сравнительную эффективность, качество конечного продукта, затраты и экологическое воздействие.
Природная экстракция
Наиболее традиционным и одновременно технологически сложным методом получения CBG является его извлечение из растительного сырья. Важной особенностью здесь является выбор культуры: для получения CBG предпочтение отдаётся специально выведенным сортам Cannabis sativa с повышенным содержанием каннабигероловой кислоты (CBGA), которые затем подвергаются биохимической или термической декарбоксиляции для образования активной формы — CBG. Это предполагает тщательный подход к культивации, сбору и хранению растений.
Одним из наиболее эффективных способов натуральной экстракции CBG является метод сверхкритической флюидной экстракции с использованием углекислого газа. Этот метод обеспечивает исключительную селективность в отношении неполярных молекул, таких как каннабиноиды, и позволяет извлекать CBG без остатка органических растворителей. Сверхкритический CO₂ в состоянии между жидкостью и газом проникает в матрицу растения, растворяя целевые компоненты. Результатом этого процесса является экстракт высокой чистоты, пригодный для последующей очистки и фракционирования. Однако этот метод требует использования дорогостоящего оборудования, в частности экстракторов высокого давления, работающих при температуре 35–45 °C и давлении до 350 бар.
Другим способом является экстракция с использованием органических растворителей, в частности этанола, гексана или изопропилового спирта. Этанол как растворитель обладает высокой полярностью, что позволяет эффективно извлекать каннабиноиды, но при этом вызывает извлечение нежелательных компонентов, таких как хлорофилл. Для минимизации примесей применяется низкотемпературная экстракция с последующим зимованием (winterization), которая позволяет осадить воски, липиды и другие высокомолекулярные вещества. Следующий этап — дистилляция или хроматография — обеспечивает высокую степень очистки CBG. Однако эти процедуры существенно влияют на себестоимость конечного продукта.
В ряде исследований описано применение фракционной перегонки в условиях вакуума, что позволяет сохранять термолабильные каннабиноиды и повысить концентрацию CBG без потери активности. Этот подход, однако, редко применяется в промышленных масштабах из-за сложности масштабирования и необходимости высокой точности температурного контроля. Дополнительные методы, в частности ультразвуковая экстракция, применяются преимущественно в лабораторных условиях и позволяют снизить температуру процесса, однако их эффективность в отношении CBG остаётся предметом дискуссий в научном сообществе.
Биотехнологические и синтетические подходы
В свете проблем масштабируемости природной экстракции всё большее внимание привлекают синтетические и биоинженерные подходы. Особое значение имеет биосинтез CBG с использованием микроорганизмов, способных продуцировать каннабиноиды с помощью встроенных метаболических путей. Наиболее распространёнными объектами для этого являются дрожжи (Saccharomyces cerevisiae) и кишечная палочка (E. coli), генетически модифицированные для синтеза предшественников каннабиноидов — геранилпирофосфата (GPP) и оливитола, которые далее ферментируются в CBGA, а затем превращаются в CBG путём термической или ферментативной декарбоксиляции.
Инновационные исследования в этой области продемонстрировали возможность получения до 100 мг/л CBG в ферментативных культурах, что свидетельствует о реалистичности масштабирования этих процессов. Например, согласно публикациям в журналах Nature Biotechnology и ACS Synthetic Biology, применение модульных синтетических каскадов позволило оптимизировать продуктивность и повысить стабильность микроорганизмов до уровня, достаточного для промышленной реализации. Основное преимущество этого подхода заключается в отсутствии зависимости от условий культивации растений, сезонности и фитосанитарных угроз. Кроме того, микробные биофабрики значительно снижают экологическую нагрузку благодаря замкнутым циклам производства.
Ферментативные методы, применяемые ex vivo, также демонстрируют значительный потенциал. По этой технологии используются очищенные ферменты, такие как каннабигероловая синтаза, в реакциях с изолированными предшественниками (оливитолом и геранилпирофосфатом). Ферментативные реакции проводятся в буферных средах с регулируемыми параметрами pH и температуры, что обеспечивает высокую селективность и выход. Одним из вызовов здесь является стабильность ферментов и их стоимость, однако синтетическая биология и протеомика активно работают над получением более стабильных и дешёвых вариантов каталитических белков.
Что касается полностью химического синтеза, он основан на реакции алкилирования оливитола геранилом или его производными в присутствии кислотных или щелочных катализаторов с последующей циклизацией и стабилизацией полученной структуры. Проблемой этого подхода является низкая химическая селективность и наличие значительного количества побочных продуктов. Кроме того, синтетический CBG может иметь неидентичную стереохимию по сравнению с природной молекулой, что потенциально влияет на его биоактивность.
Сравнительная оценка технологий
При выборе метода получения CBG критически важно учитывать конечную цель использования соединения. Если речь идёт о фармацевтическом применении, ключевыми факторами являются чистота, воспроизводимость и соответствие стандартам GMP. В таком случае биотехнологические и ферментативные подходы имеют преимущество благодаря возможности контроля на молекулярном уровне и снижению риска контаминации посторонними веществами.
Для промышленных целей, в частности в косметической или пищевой промышленности, экстракция из растительного сырья остаётся экономически целесообразной, особенно при использовании специализированных сортов с высоким содержанием CBGA. С другой стороны, методы химического синтеза могут применяться для получения исследовательских образцов или в случаях, когда доступ к сырью ограничен из-за регуляторных или логистических барьеров.
Фармакологические свойства каннабигерола (CBG)
Взаимодействие с рецепторами: CB1, CB2, TRPV1, PPARγ и другие молекулярные мишени
CBG, как непсихоактивный фитоканнабиноид, демонстрирует широкий спектр фармакологических свойств благодаря способности взаимодействовать с многочисленными молекулярными мишенями в организме человека и животных. Наиболее изученными среди них являются каннабиноидные рецепторы первого (CB1) и второго (CB2) типов, транзиторный рецептор потенциала ванилоидного типа 1 (TRPV1), а также ядерный рецептор активатора пролиферации пероксисом γ (PPARγ).
В отличие от ТГК, CBG обладает относительно низким сродством к CB1-рецепторам, что объясняет отсутствие психоактивного действия. Однако он действует как частичный агонист CB1 и CB2, демонстрируя модулирующий эффект, который может иметь значение при регуляции нейротрансмиссии, в частности в случае нейродегенеративных нарушений. В экспериментальных моделях было показано, что CBG ингибирует обратный захват анандамида — эндогенного каннабиноида — тем самым усиливая тонус эндоканнабиноидной системы.
TRPV1, кальцийзависимый ионный канал, также известный как капсаициновый рецептор, модулируется CBG с активационным эффектом. Это открывает потенциальные пути для анальгезирующего действия, уменьшения невропатической боли, а также регуляции воспалительных реакций. Перспективным является и влияние на PPARγ — транскрипционный фактор, участвующий в регуляции углеводного обмена, воспаления и клеточной дифференцировки. CBG активирует этот рецептор, что может объяснить его антидиабетический и нейропротекторный потенциал.
CBG также демонстрирует способность ингибировать активность фермента 5-альфа-редуктазы, что имеет значение в терапии гиперплазии предстательной железы и андрогенетической алопеции. Другими мишенями являются адренергические, серотонинергические и простагландиновые рецепторы, однако эти взаимодействия на данный момент остаются предметом активных исследований.
Противовоспалительное, нейропротекторное и антибактериальное действие
CBG проявляет выраженные противовоспалительные свойства, что подтверждено как in vitro, так и in vivo. В экспериментах на клеточных культурах макрофагов и микроглии CBG снижает экспрессию провоспалительных цитокинов — интерлейкина-6 (IL-6), фактора некроза опухолей альфа (TNF-α) и интерлейкина-1β (IL-1β). Подобные эффекты наблюдались также в животных моделях колита, что свидетельствует о потенциале CBG в лечении воспалительных заболеваний кишечника.
Нейропротекторные свойства CBG изучались в контексте болезни Хантингтона, Паркинсона и Альцгеймера. В моделях нейродегенерации было показано, что CBG снижает окислительный стресс, ингибирует апоптоз и способствует выживанию нейронов, предположительно за счёт воздействия на PPARγ и подавления активации микроглии. Интересно, что CBG проявил эффективность в уменьшении утраты моторики и воспаления в коре головного мозга у мышей с моделью болезни Хантингтона.
Антибактериальные свойства CBG становятся объектом растущего внимания, особенно в контексте антибиотикорезистентных инфекций. CBG эффективно ингибирует рост метициллин-резистентного золотистого стафилококка (MRSA), а также разрушает биоплёнки — структуры, обеспечивающие бактериям защиту от действия антибиотиков. Предполагается, что механизм заключается в нарушении функционирования клеточной мембраны микроорганизмов.
Перспективы применения в онкологии и гастроэнтерологии
CBG демонстрирует значительный потенциал в качестве сопутствующего или адъювантного средства в терапии некоторых форм рака. Его цитотоксическое действие в отношении раковых клеток, в частности колоректального, молочного и предстательного рака, подтверждено в нескольких доклинических исследованиях. В работе, опубликованной в Carcinogenesis (2014), было показано, что CBG ингибирует пролиферацию колоректальных клеток человека, индуцирует апоптоз и снижает ангиогенез в опухолях у мышей.
Ключевым механизмом противоопухолевого действия CBG является ингибирование сигнальных путей, связанных с клеточным ростом, в частности ERK/MAPK и PI3K/AKT, а также модуляция экспрессии генов, участвующих в регуляции клеточного цикла. Кроме того, CBG снижает уровень VEGF (фактора роста эндотелия сосудов), что ограничивает кровоснабжение опухолей.
В сфере гастроэнтерологии особый интерес представляет потенциал CBG при лечении воспалительных заболеваний кишечника (ВЗК), включая болезнь Крона и язвенный колит. CBG снижает инфильтрацию нейтрофилов в слизистую оболочку кишечника, нормализует барьерную функцию эпителия, а также уменьшает оксидативный стресс. В животных моделях наблюдалось восстановление морфологии кишечника после введения CBG в дозах 5–10 мг/кг.
Потенциально CBG может использоваться также в терапии функциональных нарушений ЖКТ, таких как синдром раздражённого кишечника (СРК), благодаря своим спазмолитическим, противовоспалительным и анальгезирующим свойствам. Однако необходимы дополнительные клинические исследования для подтверждения эффективности и безопасности этих применений у людей.
Фармакокинетика и безопасность каннабигерола (CBG)
Биодоступность, метаболизм и выведение каннабигерола
Каннабигерол (CBG), несмотря на свою низкую аффинность к основным каннабиноидным рецепторам (CB1 и CB2), обладает значительным терапевтическим потенциалом благодаря своей способности взаимодействовать с другими рецепторами и сигнальными путями в организме. Для понимания потенциала каннабигерола важным аспектом является изучение его фармакокинетики, которая включает биодоступность, метаболизм и выведение.
- Биодоступность
Биодоступность каннабигерола определяется путем, которым препарат попадает в общий кровоток после введения. При пероральном применении каннабигерола биодоступность является относительно низкой, что обусловлено высоким уровнем метаболизма при первом прохождении через печень. Этот эффект может снижать количество активной молекулы, достигающей кровотока. Существуют данные о том, что при пероральном введении биодоступность может составлять лишь 6–10%, что значительно ограничивает эффективность применения каннабигерола через рот.
Однако при других способах введения, таких как ингаляция или сублингвальное введение, биодоступность повышается, поскольку вещество не подвергается метаболическим изменениям в печени на первом этапе. Это позволяет более эффективно доставлять CBG в организм, достигать высоких концентраций в крови и обеспечивать более быстрый терапевтический эффект.
- Метаболизм каннабигерола
Каннабигерол метаболизируется в печени с помощью ферментов цитохрома P450, в частности CYP3A4 и CYP2C9. Эти ферменты катализируют процессы гидроксилирования молекулы каннабигерола, что приводит к образованию активных и неактивных метаболитов. Известно, что основной метаболит CBG — это 7-гидроксиканнабигерол, обладающий значительно меньшей фармакологической активностью по сравнению с материнской молекулой, однако он может иметь определённый терапевтический потенциал, особенно во взаимодействии с другими молекулярными мишенями в организме.
Поскольку метаболизм CBG осуществляется через систему цитохрома P450, существует потенциал для фармакокинетических взаимодействий с другими лекарственными средствами, использующими те же ферменты. Например, одновременное применение каннабигерола с препаратами, ингибирующими CYP3A4, может привести к повышению концентраций CBG в крови, что, в свою очередь, может изменить эффективность и безопасность его применения. Такие взаимодействия имеют значение при составлении терапевтических схем для пациентов, использующих комбинации препаратов.
- Выведение каннабигерола из организма
Выведение каннабигерола происходит преимущественно через почки, поскольку большинство метаболитов выводится с мочой. Однако часть каннабигерола и его метаболитов может выводиться через желчь, а значит — с калом. Это важно при разработке схем дозирования и оценке потенциала накопления каннабигерола в организме при длительном применении. Как и в случае многих других каннабиноидов, у лиц с нарушениями функции почек или печени могут наблюдаться изменения в метаболизме и выведении каннабигерола, что требует корректировки дозировок.
Начальные данные токсикологии каннабигерола
- Оценка острой токсичности
Каннабигерол демонстрирует низкую острую токсичность. Животные модели показывают, что даже при введении высоких доз CBG не наблюдается серьёзных летальных последствий. Повышение дозы в сотни раз выше терапевтической не приводит к тяжёлым нарушениям в функционировании организма. Исследования острой токсичности показали, что даже в случае передозировки CBG не наблюдаются тяжёлые расстройства сердечно-сосудистой или нервной систем. Однако возможны незначительные побочные эффекты, такие как временная дезориентация, сонливость, незначительное снижение моторной активности.
- Хроническая токсичность
На сегодняшний день отсутствуют значимые данные, свидетельствующие о хронической токсичности CBG. Важно отметить, что при длительном применении каннабигерола в терапевтических дозах у животных не было выявлено серьёзных побочных эффектов. Результаты исследований показывают, что CBG не оказывает токсического влияния на печень, почки или сердце в долгосрочной перспективе. Однако, поскольку клинические исследования на людях длились более короткий период, полная картина возможных долгосрочных побочных эффектов пока не сформирована.
Одним из главных вызовов является то, что каннабигерол может вызывать изменения в функциях органов, связанных с метаболизмом, таких как печень и почки, в случае значительного превышения доз. Это требует тщательного контроля дозировок в клинических испытаниях и при применении CBG в медицинской практике.
- Воздействие на органы
Каннабигерол может оказывать влияние на различные органы, включая печень, почки и сердечно-сосудистую систему. Однако на сегодняшний день не выявлено серьёзных токсических эффектов при использовании каннабигерола в рекомендуемых дозах. Случаи токсичности ограничиваются лишь лёгкими симптомами на уровне желудочно-кишечного тракта, такими как диспепсия или незначительное снижение аппетита. Однако в случае передозировки может возникнуть временное снижение функции почек или печени, что обязательно требует корректировки дозировки или временной приостановки приёма препарата.
Переносимость каннабигерола при различных формах введения
- Пероральное введение
Пероральное введение каннабигерола обеспечивает стабильный эффект при длительном применении, но низкая биодоступность делает его менее эффективным. Этот метод введения является наиболее удобным, поскольку позволяет удобно дозировать каннабигерол в виде капсул или масла, а также позволяет пациентам сохранять контроль над дозировкой. Однако необходимо учитывать, что пероральное введение сопровождается эффектом первого прохождения через печень, что снижает количество активной молекулы в крови.
- Ингаляция
Ингаляция каннабигерола через пар или специальные устройства позволяет быстро достичь высоких концентраций в крови, поскольку вещество не подвергается метаболическим изменениям в печени. Этот метод также позволяет минимизировать влияние на пищеварительную систему, что делает его более эффективным при быстром лечении симптомов. Однако из-за отсутствия долгосрочных исследований по воздействию ингаляции каннабигерола этот метод требует дополнительных научных данных.
- Сублингвальное введение
Сублингвальное введение каннабигерола обеспечивает быстрое всасывание и высокие концентрации в крови. Каннабигерол, попадая непосредственно в кровоток через слизистую оболочку полости рта, минует печень, что позволяет обеспечить высокую биодоступность и быстрый эффект. Этот метод является удобным для пациентов, нуждающихся в быстрой терапевтической реакции, но также требует точного дозирования для избежания передозировки.
Текущие исследования и клинический потенциал каннабигерола (CBG)
Каннабигерол (CBG), как один из основных каннабиноидов, привлекает всё больше внимания в контексте его медицинского потенциала. Благодаря своим фармакологическим свойствам, таким как противовоспалительное, нейропротекторное, антибактериальное и антидиабетическое действие, CBG демонстрирует возможности в лечении широкого спектра заболеваний. Растущее количество научных исследований обосновывает необходимость дальнейших клинических испытаний, направленных на подтверждение безопасности и эффективности данного каннабиноида в медицинской практике.
Результаты доклинических моделей
Доклинические исследования каннабигерола показали его значительный терапевтический потенциал в различных модельных системах. Испытания на животных и клеточных культурах позволили выявить многообещающие результаты в отношении лечения ряда заболеваний, в частности неврологических, воспалительных, онкологических и бактериальных.
Одним из основных направлений исследований является изучение влияния CBG на нейродегенеративные заболевания, такие как болезнь Хантингтона, Паркинсона и Альцгеймера. В доклинических моделях показано, что CBG способен снижать уровень окислительного стресса, уменьшать активацию микроглии (клеток, отвечающих за воспаление в мозге), а также способствовать сохранению нейронов, что даёт основания для дальнейшего изучения CBG как потенциального нейропротектора.
Кроме того, CBG продемонстрировал обнадёживающие результаты в борьбе с инфекциями, особенно бактериальными. Исследования показали его способность ингибировать рост метициллин-резистентного золотистого стафилококка (MRSA), а также эффективность против других патогенных микроорганизмов, таких как Escherichia coli и Pseudomonas aeruginosa. Также были зафиксированы положительные эффекты CBG в борьбе с бактериальными биоплёнками, что является значительным достижением в контексте антибиотикорезистентности.
Ещё одной перспективной областью является использование каннабигерола для лечения воспалительных заболеваний кишечника, таких как болезнь Крона и язвенный колит. Исследования на животных показали, что CBG способен снижать уровень провоспалительных цитокинов, улучшать барьерную функцию кишечника и уменьшать инфильтрацию нейтрофилов в слизистую оболочку кишки. Это открывает новые возможности для применения каннабигерола в терапии воспалительных заболеваний ЖКТ.
Доклинические модели также продемонстрировали, что CBG обладает анальгезирующими свойствами, что открывает перспективы для его использования в лечении хронической боли, в частности нейропатической и воспалительной. В экспериментах на животных было показано, что CBG может снижать уровень боли путём активации рецепторов TRPV1, отвечающих за восприятие боли и температуры.
Одним из наиболее интересных направлений исследований является использование CBG в борьбе с онкологическими заболеваниями. Ряд доклинических исследований показал, что CBG обладает потенциалом для ингибирования пролиферации раковых клеток, в частности при колоректальном, молочном и простатическом раке. Механизм противоопухолевого действия CBG включает блокировку сигнальных путей, способствующих росту и развитию опухолей, таких как ERK/MAPK и PI3K/AKT. Это делает CBG многообещающим кандидатом для дальнейшего изучения как дополнения к стандартной терапии рака.
Клинические испытания: краткий обзор
Клинические испытания каннабигерола находятся на ранних этапах, но уже имеются предварительные данные, подтверждающие его безопасность и эффективность в лечении некоторых заболеваний. Важно отметить, что большинство клинических исследований каннабигерола по-прежнему являются маломасштабными и относятся к фазам 1 и 2, что делает выводы о его терапевтическом потенциале предварительными.
Одно из первых клинических исследований CBG касалось его применения у пациентов с хронической болью, в частности нейропатической. Результаты показали, что применение CBG оказывает положительное влияние на снижение интенсивности боли и улучшение качества жизни пациентов. Однако, несмотря на обнадёживающие результаты, исследование не выявило значительных отличий по сравнению с плацебо, что указывает на необходимость дополнительных клинических испытаний для подтверждения этих результатов.
Другое клиническое исследование изучало использование CBG у пациентов с воспалительными заболеваниями кишечника. Применение CBG показало снижение уровня воспаления и улучшение симптомов у пациентов с болезнью Крона. Однако и эти результаты требуют дальнейшей проверки на большей популяции пациентов и при длительном применении.
Ещё одно направление клинических исследований связано с потенциальным использованием CBG для лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона и Альцгеймера. На данный момент проведено несколько небольших клинических исследований, которые указывают на улучшение моторных функций у пациентов с Паркинсоном после применения CBG, однако эффективность и безопасность требуют дальнейших масштабных исследований.
В то же время, клинические исследования в области онкологии, изучающие влияние CBG на раковые клетки, находятся на стадии первичных испытаний. По предварительным данным, CBG может быть полезен как дополнительное лечение для некоторых видов рака, таких как колоректальный рак. Однако, как и в других направлениях, необходимо больше клинических испытаний для подтверждения этой гипотезы.
Барьеры для внедрения CBG в медицинскую практику
Существует несколько существенных барьеров для внедрения каннабигерола в медицинскую практику, в том числе правовые, экономические и научные. Несмотря на значительный терапевтический потенциал каннабигерола, некоторые из этих барьеров могут замедлить или усложнить его широкое применение.
- Правовые барьеры
Один из крупнейших барьеров на пути к внедрению CBG в медицинскую практику — это правовые ограничения, связанные с каннабиноидами в целом. Во многих странах каннабиноиды, даже в непсихоактивных формах, таких как CBG, до сих пор классифицируются как контролируемые вещества. Это затрудняет проведение клинических испытаний, а также ограничивает возможность широкого применения CBG в медицинской практике.
Пока что лишь в отдельных странах каннабигерол имеет статус разрешённого препарата, что значительно ограничивает возможности для исследований и клинического применения. Однако с постепенным смягчением законодательства в отношении каннабиноидов во всём мире, ситуация может измениться в пользу большего признания CBG как терапевтического средства.
- Экономические барьеры
Создание и производство лекарственных средств на основе CBG требует значительных инвестиций в научные исследования и клинические испытания. Терапевтические препараты на основе каннабигерола предполагают высокие затраты на разработку, тестирование и получение необходимых лицензий для коммерческого производства. Кроме того, на производство таких препаратов могут быть наложены налоги и ограничения, что увеличивает их стоимость для конечных потребителей.
- Научные барьеры
Хотя исследования CBG выявили его перспективы в лечении различных заболеваний, существует необходимость в дальнейших клинических испытаниях для более точного понимания механизмов его действия, оптимальных доз и продолжительности лечения. Только после проведения крупных, многократных и длительных исследований можно будет окончательно оценить, действительно ли CBG может стать эффективным и безопасным лекарством для широкой аудитории пациентов.
Вывод
Каннабигерол (CBG) представляет собой один из наиболее перспективных каннабиноидов, который привлекает значительное внимание в контексте современных медицинских исследований благодаря своим широким фармакологическим свойствам. Его потенциал в лечении различных заболеваний, таких как нейродегенеративные болезни, инфекционные заболевания, воспалительные процессы и онкологические заболевания, на основе доклинических исследований выглядит обнадеживающим. Однако, несмотря на многообещающие предварительные результаты, каннабигерол всё ещё требует проведения дополнительных клинических испытаний для подтверждения его эффективности и безопасности в реальных условиях.
Важной проблемой остаётся правовое регулирование и экономические барьеры, сдерживающие широкое внедрение CBG в медицинскую практику. Однако с учётом изменений в законодательной сфере в отношении каннабиноидов и постепенного расширения научных исследований существует реальная возможность для более широкого признания данного каннабиноида в качестве терапевтического средства в ближайшем будущем.
На основе текущих исследований можно сделать вывод, что каннабигерол обладает большим клиническим потенциалом, но для его полноценного применения в медицине необходимо решить ещё ряд проблем, связанных с правовым статусом, экономическими аспектами производства и расширением научных исследований. Поэтому для того чтобы каннабигерол смог реализовать свой полный медицинский потенциал, следует продолжать научные исследования, преодолевать барьеры для его внедрения и внимательно отслеживать результаты клинических испытаний, что поможет сделать этот каннабиноид важным компонентом современной терапии.
Источники:
- PubMed (NCBI) — научные исследования, рецензируемые статьи, клинические испытания: https://pubmed.ncbi.nlm.nih.gov/
Одна из крупнейших баз данных, содержащая статьи и исследования по медицинской, биологической и фармакологической тематике. - Google Scholar — научные статьи, рецензируемые журналы и диссертации: https://scholar.google.com/
Платформа, на которой можно найти научные публикации и исследования из различных областей, включая фармакологию и химию каннабиноидов. - Frontiers in Pharmacology — открытые научные журналы по фармакологии: https://www.frontiersin.org/journals/pharmacology
Журнал предоставляет доступ к статьям по различным направлениям фармакологии, в том числе каннабиноидов и их терапевтических свойств. - Cannabis and Cannabinoid Research — журнал, публикующий статьи и исследования о каннабисе и каннабиноидах: https://www.liebertpub.com/can
Специализированный журнал, сосредоточенный на научных и клинических исследованиях каннабиноидов. - National Institute on Drug Abuse (NIDA) — официальный ресурс, публикующий исследования о каннабисе и его компонентах: https://www.drugabuse.gov/
Научные статьи и исследования по каннабиноидам и их влиянию на здоровье. - World Health Organization (WHO) — отчёты и обзоры по каннабиноидам: https://www.who.int/
Официальный сайт ВОЗ, на котором публикуются отчёты и научные обзоры, в том числе о медицинском применении каннабиноидов. - ScienceDirect — научные статьи и обзоры на тему фармакологии каннабиноидов: https://www.sciencedirect.com/
Платформа для доступа к научным статьям и рецензируемым журналам, охватывающим различные