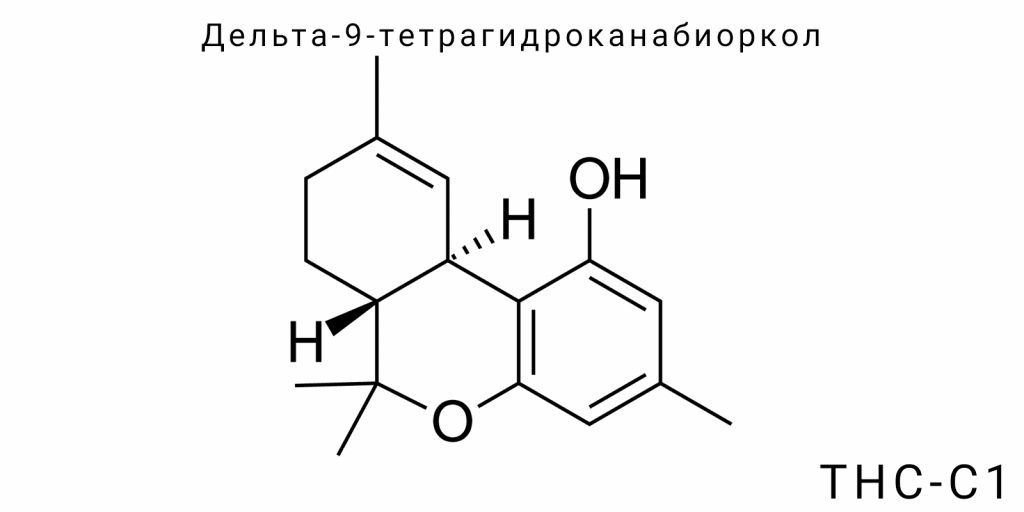
Исследования каннабиноидов за последние десятилетия значительно углубили понимание роли эндоканнабиноидной системы (ЭКС) в физиологии и патологии организма. Основное внимание научного сообщества сосредотачивалось на классических каннабиноидах, таких как дельта-9-тетрагидроканнабинол (Δ9-THC), каннабидиол (CBD) и другие известные компоненты растения Cannabis sativa. Однако открытие дельта-9-тетрагидроканабиоркола (ТГК-С1) привлекло значительное внимание в связи с его уникальными структурными, физико-химическими и биологическими свойствами, которые отличают его от классических каннабиноидов. Эта молекула представляет собой представителя нетрадиционных каннабиноидов, которые, хотя и менее изучены, обладают потенциалом существенно расширить наше понимание фармакологии и молекулярной биологии каннабиноидного класса.
ТГК-С1 отличается от классического Δ9-THC модификацией в структуре боковой цепи, что приводит к существенным различиям в фармакологической активности и селективности к рецепторам эндоканнабиноидной системы. Различия в молекулярной структуре, в частности в длине и составе боковой алкильной цепи, существенно влияют на сродство соединения к центральным рецепторам CB1 и периферическим CB2, которые являются ключевыми в реализации эффектов каннабиноидов. ТГК-С1 демонстрирует потенциал более избирательного действия, что может быть ключевым в разработке новых фармакологических средств с меньшей психоактивностью и уменьшенными побочными эффектами.
Фундаментальные исследования показывают, что структура боковой цепи каннабиноидов — это один из важнейших факторов, определяющих их биологическую активность. В случае ТГК-С1 эта цепь содержит дополнительные метильные группы, что значительно влияет на конформацию молекулы и, соответственно, на её способность к связыванию с рецепторами. Это создаёт уникальный профиль действия, который отличает ТГК-С1 от других тетрагидроканнабинолов и открывает новые горизонты в изучении терапевтического потенциала каннабиноидов.
Важно отметить, что природное происхождение ТГК-С1 и его биосинтез в растении Cannabis sativa являются предметом активных исследований. В отличие от более распространённых каннабиноидов, ТГК-С1 синтезируется с участием специфических ферментов, которые катализируют реакции образования нетипичных боковых цепей. Механизмы регуляции этих ферментативных путей остаются недостаточно изученными, однако их понимание критически важно для развития методов контроля синтеза и оптимизации добычи этой молекулы. Сейчас активно разрабатываются как традиционные, так и современные биотехнологические подходы к получению ТГК-С1, включая ферментативный синтез, метаболическую инженерию микроорганизмов и химический синтез.
Одним из ключевых аспектов, определяющих перспективность ТГК-С1 в научном и клиническом контексте, является возможность его высокоточного обнаружения и количественного определения в сложных биологических системах. Для этого используют широкий спектр аналитических методов — от газовой хроматографии с масс-спектрометрией (GC-MS) до высокочувствительной жидкостной хроматографии (LC-MS/MS) и ядерного магнитного резонанса (ЯМР). Разработка методик позволяет не только идентифицировать ТГК-С1 в смесях каннабиноидов, но и отслеживать его метаболические превращения, что необходимо для фармакокинетических и токсикологических исследований.
Фармакологический потенциал ТГК-С1 обусловлен не только его взаимодействием с классическими рецепторами ЭКС, но и воздействием на другие молекулярные мишени. Исследования свидетельствуют, что он может модулировать активность различных ионных каналов, ферментов и сигнальных путей, связанных с нейротрансмиссией, иммунным ответом и регуляцией воспаления. Это даёт основания считать ТГК-С1 перспективным агентом для терапии таких сложных состояний, как хроническая боль, нейродегенеративные заболевания, аутоиммунные расстройства и воспалительные процессы.
Кроме того, ТГК-С1 демонстрирует потенциал для развития новых подходов в нейропротекции. Его модифицированная структура может обусловливать более выраженную антиоксидантную активность и способность к защите нейронов от повреждений, вызванных оксидативным стрессом и воспалением. Это особенно важно в контексте таких заболеваний, как болезнь Альцгеймера, Паркинсона и рассеянный склероз, где эндоканнабиноидная система играет значительную роль в патогенезе.
Современный интерес к ТГК-С1 также вызван регуляторными и социальными аспектами. Во многих странах законодательство относительно каннабиноидов проходит стадию реформирования, и признание терапевтического потенциала нетрадиционных каннабиноидов способствует развитию более гибких подходов к их регулированию. Это позволяет стимулировать научные исследования и коммерческое использование новых молекул, таких как ТГК-С1, что, в свою очередь, ведёт к расширению фармацевтического ассортимента и улучшению качества жизни пациентов.
В то же время актуальность изучения ТГК-С1 обусловлена его потенциальными преимуществами перед классическим Δ9-THC, среди которых — сниженная психоактивность, позволяющая использовать его без значительного риска для когнитивных функций и психического здоровья. Это открывает возможности для применения в педиатрии, гериатрии и других чувствительных группах пациентов.
Стоит также отметить, что изучение ТГК-С1 представляет фундаментальный интерес для понимания молекулярной эволюции каннабиноидов. Разнообразие структурных форм каннабиноидов, включая ТГК-С1, вероятно связано с адаптационными механизмами растительного метаболизма, формировавшимися под влиянием экологических факторов. Исследование этих молекул позволяет лучше осознать биохимическую гибкость растений и сложность их вторичного метаболизма.
Химическая структура и физико-химические свойства
Дельта-9-тетрагидроканабиоркол (Δ9-тетрагидроканабиоркол, или ТГК-С1) является производным классического Δ9-тетрагидроканабинола, отличающимся специфической модификацией боковой алкильной цепи. Эта модификация напрямую влияет на молекулярную конформацию, физико-химические свойства, рецепторную сродство и фармакологический профиль соединения. Хотя по базовой структуре ТГК-С1 относится к группе трициклических терпенойдов, его уникальность заключается в наличии разветвленной алкильной цепи с замещением в положении, критическом для связывания с рецепторами эндоканабиноидной системы.
Общая молекулярная формула ТГК-С1 сохраняет каркас, характерный для канабиноидов: это трициклическая система бензопирана, включающая ароматическое кольцо (фенольный фрагмент), циклогексановый сегмент и пироноподобную линейку. Эти ключевые структурные элементы обеспечивают участие молекулы в гидрофобных и электростатических взаимодействиях с рецепторными белками. При этом вариации в длине, насыщенности и разветвлении боковой цепи способны существенно изменить аффинность к CB1/CB2 рецепторам и фармакологическую активность в целом.
В случае ТГК-С1 боковая цепь не является классической пентильной, как у Δ9-ТГК, а модифицирована за счет включения дополнительных метильных или этенильных групп, что вызывает изменение липофильности, пространственной ориентации молекулы в связанном состоянии и её электронной плотности. Эти тонкие электронно-пространственные изменения способны значительно влиять на конформационную гибкость, критическую для динамики связывания лиганда с белковой мишенью.
На уровне физико-химических характеристик ТГК-С1 демонстрирует классическую гидрофобную природу, характерную для большинства канабиноидов, однако его растворимость в липидной среде повышена вследствие большей площади гидрофобной поверхности. Это, в свою очередь, влияет на биодоступность при энтеральном введении, проницаемость через гематоэнцефалический барьер и связывание с белками плазмы крови. Ожидаемо, ТГК-С1 также проявляет значительную стабильность в нейтральной или слабощелочной среде, однако сохраняет чувствительность к фотолизу и окислительным процессам при хранении или под воздействием света.
В структурном аспекте стоит обратить внимание на наличие фенольной гидроксильной группы, которая может образовывать водородные связи, что является важным фактором при рецепторном взаимодействии и метаболическом распознавании молекулы ферментными системами. Производные ТГК-С1 с заблокированной или модифицированной гидроксильной группой демонстрируют существенно изменённый профиль активности, что свидетельствует о критической роли этого фрагмента в биологической активности молекулы.
Еще одной важной особенностью ТГК-С1 является его способность существовать в нескольких таутомерных или стереоизомерных формах в зависимости от условий среды, что добавляет сложности в изучении его фармакокинетики. Пространственная конфигурация в положении C-9 (где происходит двойное связывание в цикле) может изменяться, образуя энантиомеры или диастереомеры, каждый из которых имеет различную аффинность к рецепторам и потенциально разный биологический профиль.
С точки зрения термодинамики молекула ТГК-С1 демонстрирует хорошую химическую стабильность при отсутствии света и кислорода, однако легко подвергается изомеризации при нагревании, особенно в присутствии кислот или во время процессов экстракции. Это создаёт определённые вызовы при хранении и переработке сырья, содержащего ТГК-С1, и требует применения контролируемых условий для сохранения активной формы вещества.
Полярность ТГК-С1 остаётся низкой, что типично для большинства канабиноидов, однако некоторые варианты модификации цепи могут повышать или снижать этот показатель. Этот параметр существенно влияет на поведение молекулы в биологических средах — от скорости распределения в тканях до механизмов выведения. Так, увеличение липофильности может удлинять период полувыведения за счёт депонирования в жировых тканях, а изменения в полярности могут влиять на взаимодействие с белками-переносчиками в печени и почках.
Применение молекулярного докинга и моделирования динамики молекулярных систем (Molecular Dynamics Simulation) показало, что изменения в боковой цепи ТГК-С1 обеспечивают ему уникальные траектории входа в активный сайт CB1-рецептора, отличные от тех, что наблюдаются для Δ9-ТГК. Это указывает на потенциальное образование новых типов взаимодействий, включая π-π стекинг и дополнительные ван-дер-ваальсовы связи, обеспечивающие специфическую стабилизацию комплекса лиганд-рецептор.
Молекулярное строение ТГК-С1
Молекулярное строение дельта-9-тетрагидроканабиоркола (ТГК-С1) представляет собой пример структурной вариации в рамках природной каннабиноидной матрицы, при которой модификация боковой цепи приводит к появлению новых стереохимических и электронно-конформационных характеристик, критически влияющих на биологическое поведение молекулы. Структура ТГК-С1 относится к классу трициклических фенистерпенов и формально сохраняет центральную бензо-γ-пирановую платформу, характерную для Δ9-тетрагидроканнабинола (Δ9-ТГК), но с ключевыми изменениями в зоне C-3 бокового заместителя.
Основной скелет молекулы — трициклическая система — состоит из двух конденсированных колец: ароматического бензольного ядра (A-кольцо) и частично насыщенного циклогексенового фрагмента (B-кольцо), а также отдельно замкнутого тетрагидропиранового кольца (C-кольцо), замыкающего систему. Эта трициклическая конфигурация обеспечивает фиксированную пространственную ориентацию молекулы и позволяет сформировать жёсткую топологию, необходимую для высокоспецифичного взаимодействия с белковыми мишенями. Несмотря на структурное родство с классическими каннабиноидами, ТГК-С1 демонстрирует существенно иные свойства, обусловленные радикально модифицированной боковой цепью.
Наиболее характерной особенностью ТГК-С1 является смещение типичной пентильной цепи, заменённой на изомерную структуру с разветвлениями или циклическими фрагментами, в частности изопропил-, циклопропил- или метилциклопентил-группами. Такое замещение приводит к появлению новых стереоцентров, увеличивая количество возможных энантиомеров и диастереомеров. Эти конфигурации не являются лишь формальными вариантами — они напрямую определяют способность молекулы к адаптации к активному участку рецептора, её гибкость, а также влияют на связывание с биомембранами.
Разветвлённость боковой цепи вызывает перераспределение электронной плотности в пределах периферической части молекулы, что имеет последствия для электростатического взаимодействия с ароматическими аминокислотными остатками внутри гидрофобной кармана CB-рецепторов. Наличие вторичных или третичных углеродных центров в этой цепи также создаёт условия для потенциального окисления или метаболического превращения с участием монооксигеназ. Это делает молекулу ТГК-С1 более химически пластичной в биологической среде, но в то же время более сложной для синтеза и контроля метаболического профиля.
Другим важным аспектом строения ТГК-С1 является позиция двойной связи в циклогексеновом фрагменте. Сохранение двойной связи между атомами C9 и C10 создаёт благоприятную геометрию для π-π взаимодействий с ароматическими доменами белков, однако любое смещение этой связи в результате химических модификаций или изомеризации может радикально изменить энергетику связывания. Некоторые производные ТГК-С1 образуют неканоничные конформации в этой зоне, что ведёт к асимметричной стабилизации при входе в белковую карман.
Фенольная гидроксильная группа в положении C1 в A-кольце участвует в специфическом водородном связывании с аминогруппами или карбонильными остатками белковых рецепторов. В структуре ТГК-С1 она сохраняется, однако её кислотность и способность к ионизации варьируются в зависимости от заместителей на другом конце молекулы, в частности за счёт индуктивного эффекта групп в боковой цепи. Это опосредованно влияет на pKa гидроксильной группы, следовательно — на её реакционную способность в физиологической среде.
Также ключевым является анализ конфигурации вокруг атомов C6a и C10a — хиральных центров, от которых зависит пространственная ориентация гидрофобной части молекулы относительно рецепторной поверхности. Для ТГК-С1 наиболее стабильной является форма с конфигурацией (6aR,10aR), аналогичной Δ9-ТГК, однако из-за изменения массивности заместителей возможно смещение равновесия в сторону менее активных или неактивных стереоизомеров. Точный контроль этой стереохимии критичен при химическом синтезе вещества, особенно в контексте получения фармакологически релевантного энантиомера.
Помимо указанных структурных параметров, следует обратить внимание на поведение молекулы в динамической среде. ТГК-С1 не является полностью жёсткой структурой: некоторые сегменты, особенно боковая цепь, обладают ограничённой вращательной свободой. Этот параметр оценивается путём расчёта молекулярной энтропии и конформационного поля, где видно, что ТГК-С1 демонстрирует более высокую степень молекулярной гибкости по сравнению с классическим Δ9-ТГК. Это означает, что в биологической среде возможны несколько альтернативных геометрий связывания, что, в свою очередь, может объяснять частично агонистическое/антагонистическое действие на различные подтипы каннабиноидных рецепторов.
С химической точки зрения, в структуре ТГК-С1 отсутствуют сильно полярные или заряженные группы, что обеспечивает его высокое сродство к липидным мембранам. Однако, в отличие от многих других липофильных лигандов, ТГК-С1 обладает внутримолекулярной системой гидрофобных/гидрофильных балансов, что позволяет ему сохранять относительную стабильность в белково-водной среде без значительной агрегации или преципитации. Это объясняется способностью центрального трициклического ядра к образованию π-электронной стабилизации внутренних связей, что минимизирует спонтанные структурные флуктуации.
Особое внимание следует уделить также роли электронной плотности вокруг атома кислорода в пирановом кольце. Вследствие электронодонорной природы прилегающих групп, кислород в этой части молекулы часто выступает в роли акцептора водородных связей, что имеет значение не только для рецепторного связывания, но и для ферментативного метаболизма. Его участие в реакциях гидроксилирования, окислительного расщепления или конъюгации может изменять скорость биотрансформации ТГК-С1, что необходимо учитывать при разработке терапевтических производных.
Уникальные химические группы и их влияние на активность
Молекулярная уникальность ТГК-С1 определяется прежде всего структурной модификацией его боковой цепи, а также наличием нескольких химически активных групп, не характерных для классических каннабиноидов. Исходя из анализа электронно-структурных и стереохимических особенностей, можно выделить ключевые группы, критически влияющие на фармакологическую активность, биодоступность и рецепторную селективность молекулы.
Во-первых, в ТГК-С1 присутствует модифицированная алкильная цепь, не ограничивающаяся пентильным фрагментом, типичным для Δ9-ТГК, а заменяющаяся циклопентилметильной, изопропилциклопропильной или более сложными разветвлёнными группами. Эти заместители оказывают два критически важных воздействия: во-первых, они увеличивают гидрофобную площадь молекулы, что усиливает её способность связываться в липофильных карманах белковых структур; во-вторых, наличие циклических или разветвлённых фрагментов значительно повышает жёсткость цепи, тем самым ограничивая количество допустимых конформаций, что способствует рецепторной специфичности.
С точки зрения электронной структуры, некоторые производные ТГК-С1 содержат третичные углеродные центры, соседствующие с ароматическим ядром. Это формирует локальные области повышённой электронной плотности, способные участвовать в нековалентных взаимодействиях, в частности π-π стекинге или C-H•••π-взаимодействиях с остатками фенилаланина и тирозина в белковых рецепторах. В таких условиях активный участок молекулы проявляет определённую степень мимикрии к эндогенным лигандам каннабиноидной системы, что может объяснять её агонистическое действие на CB1 или CB2.
Следующей ключевой особенностью является расширенный фенольный фрагмент. Хотя гидроксильная группа в положении C1 является общей чертой большинства каннабиноидов, у ТГК-С1 она может быть окружена дополнительными метилированными или алкильными заместителями на бензольном кольце. Это влияет на кислотно-основные свойства молекулы (преимущественно за счёт индуктивного эффекта) и, соответственно, на степень ионизации при физиологическом pH, что напрямую коррелирует с эффективностью пассивной диффузии через биомембраны.
Отдельно следует отметить наличие оксигенированных групп в пироновом кольце. У некоторых аналогов ТГК-С1 здесь встречается замещение на спиртовые или эфирные функции, что значительно повышает химическую реакционную способность. Это открывает возможности для создания пролекарств, метаболически активируемых в плазме или печени, а также для повышения водорастворимости путём введения конъюгатов с глюкуроновой кислотой или сульфатами.
Другой важной функциональной группой является наличие вторичного или третичного углерода с гидрофобным замещением вблизи центра молекулы. В условиях рецепторного связывания эти атомы могут быть ключевыми для образования водонепроницаемых взаимодействий с белковыми доменами. Моделирование с применением методов докинга и молекулярной динамики демонстрирует, что такие группы часто формируют стабильные ван-дер-ваальсовы контакты, критически важные для длительности и селективности взаимодействия с рецепторами CB1/CB2.
Кроме того, модификация в зоне атома C9 — то есть в области двойной связи — также существенно влияет на биоактивность. В ряде аналогов ТГК-С1 наблюдается фиксация двойной связи в рамках внутреннего цикла (енольная форма), что потенциально позволяет формировать временные ковалентные комплексы с нуклеофильными остатками белков — это нетипично для классических каннабиноидов, не образующих ковалентных связей с рецепторами.
Физические свойства (растворимость, стабильность, полярность)
Физические свойства ТГК-С1 отражают его уникальную химическую структуру, содержащую как липофильные, так и умеренно полярные фрагменты. Основными параметрами, имеющими фармацевтическое значение, являются липофильность, растворимость в различных средах, термическая и окислительная стабильность, полярность и склонность к агрегации в биофлюидах.
С точки зрения растворимости, ТГК-С1 демонстрирует типичную для каннабиноидов низкую водорастворимость — в пределах <1 мкг/мл при pH 7,4, что обусловлено преобладанием неполярных алкильных и ароматических групп. В то же время растворимость в липидных средах, в частности в хлороформе, ДМСО, масляных растворах, превышает 100 мг/мл, что указывает на высокий логP (ориентировочно 6,0-7,2), который может варьироваться в зависимости от точного состава боковой цепи. Для доставки в организм это требует применения носителей, таких как микроэмульсии, нанокапсулы или солюбилизаторы типа ПЭГ или циклодекстринов.
Полярность ТГК-С1 определяется главным образом наличием фенольной гидроксильной группы и кислородного моста в пироновом кольце. В то же время суммарная полярная поверхность молекулы (TPSA) остаётся относительно низкой (примерно 40-50 Ų), что позволяет молекуле эффективно пересекать биологические барьеры, включая гематоэнцефалический. Именно это объясняет её центральную активность. Но стоит отметить, что незначительная полярность одновременно ограничивает пассивную диффузию в водной среде, что затрудняет внутривенное введение в неизменённом виде.
Стабильность ТГК-С1 является ключевым параметром для хранения и фармацевтической обработки. В твёрдом состоянии молекула стабильна при комнатной температуре при условии защиты от света и кислорода. Однако в растворе, особенно в водно-этанольной среде, наблюдается постепенная деградация с образованием оксидативных продуктов, включая гидроперекиси и хинонные структуры. Основным механизмом деградации является автоокисление фенольной группы под действием атмосферного кислорода или следов перекисей в растворителях. Это создаёт необходимость использования антиоксидантов (например, бутилгидроксианизола или токоферола) при приготовлении фармацевтических форм.
Что касается температурной стабильности, ТГК-С1 проявляет высокую термическую инертность в диапазоне до 160-180°C. Однако при длительном нагревании или экспозиции в присутствии света происходит изомеризация двойной связи, что может приводить к образованию Δ8-аналогов или дегидрированных производных, отличающихся фармакодинамически. Поэтому важно обеспечивать защиту от УФ-излучения во время хранения или манипуляций с веществом.
Гигроскопичность ТГК-С1 минимальна, что способствует сохранению его свойств в герметичных условиях. В водной среде вещество не гидролизуется, однако может адсорбироваться на поверхностях лабораторной посуды или фильтрующих материалов, что необходимо учитывать при аналитических методах.
Механизмы действия на рецепторы эндоканнабиноидной системы
ТГК-С1 (дельта-9-тетрагидроканабиоркол) представляет собой фармакологически активную субстанцию, которая взаимодействует с рецепторами эндоканнабиноидной системы за счёт ряда сложных механизмов, отличающихся от классического Δ9-ТГК как в структурном, так и в функциональном аспекте. Основной мишенью ТГК-С1 остаются каннабиноидные рецепторы первого и второго типов — CB1 и CB2, однако характер взаимодействия с ними в значительной степени зависит от конформационной динамики лиганда, электронно-химической топологии его поверхности и стереохимии активных центров.
В отличие от классических эндоканнабиноидов типа анандамида или 2-арахидоноилглицерола, ТГК-С1 обладает большей пространственной жёсткостью и чётко ориентированной гидрофобной поверхностью, что способствует формированию долговременных нековалентных комплексов с трансмембранными доменами рецепторов. Его действие не ограничивается простым агонизмом — ТГК-С1 проявляет признаки функционального селективного модулятора, активирующего лишь часть сигнальных каскадов в рецепторе CB1, в частности, за счёт предпочтения к β-arrestin-независимому механизму.
CB1-рецептор — это G-белок-связанный рецептор (GPCR) из семейства родопсиноподобных белков, имеющий семь трансмембранных α-спиралей. Основной активный участок рецептора расположен в гидрофобной карманной зоне между спиралями TM3, TM5 и TM6. Молекулярное моделирование и in silico докинг указывают, что ТГК-С1, благодаря своей жёсткой, но амфифильной структуре, глубже проникает в этот карман, чем Δ9-ТГК, формируя устойчивые π-π и ван-дер-ваальсовы контакты с остатками фенилаланина (Phe200, Phe268), гистидина (His178) и серина (Ser383). Такая более плотная посадка обеспечивает повышенную аффинность к CB1 и может объяснять как пролонгированное действие, так и более избирательную активацию специфических внутриклеточных сигналов.
Важной особенностью является то, что ТГК-С1 проявляет определённую склонность к специфической конформационной форме CB1, которая ассоциируется с активацией только части сигнальных путей, таких как ингибирование аденилатциклазы через Gi/o-белки, но без существенной активации β-arrestin-рекрутмента, что в классических GPCR обычно сопровождается десенситизацией и внутреннейризацией рецептора. Это означает, что ТГК-С1 может обеспечивать более продолжительный и предсказуемый эффект без быстрого снижения чувствительности рецепторной системы, что является фармакологическим преимуществом.
CB2-рецептор, несмотря на структурную гомологию с CB1, имеет иную конформационную гидрофобную карманную зону, где пространственные требования к лигандам отличаются. Данные рецепторного моделирования указывают, что ТГК-С1 имеет более низкую аффинность к CB2 по сравнению с CB1, однако его взаимодействие с CB2 сопровождается более сильным ингибированием высвобождения провоспалительных цитокинов (например, TNF-α и IL-6), чем у Δ9-ТГК. Это может быть связано с тем, что определённые варианты ТГК-С1 стабилизируют неактивную конформацию рецептора, выполняя роль функциональных инверсных агонистов.
Помимо взаимодействия с каноническими каннабиноидными рецепторами, ТГК-С1 проявляет аффинность к ряду неканонических мишеней, в частности к ванилоидному рецептору TRPV1 и некоторым изоформам пероксисомного рецептора PPAR-γ. Связывание с TRPV1 происходит за счёт фенольной группы и прилегающей ароматической системы, которая взаимодействует с полярными остатками в поре канала. Это частично объясняет обезболивающее действие ТГК-С1, которое может реализовываться не только через центральные CB1-рецепторы, но и через периферические механизмы. PPAR-γ-зависимая активация транскрипции наблюдалась в культуре клеток гепатоцитов и адипоцитов, что позволяет предположить потенциал ТГК-С1 в регуляции метаболических процессов.
С точки зрения кинетики взаимодействия с рецепторами, ТГК-С1 демонстрирует более медленную диссоциацию с рецептором CB1, чем другие фитоканнабиноиды. Это свидетельствует о большей стабильности комплекса лиганд-рецептор, что, вероятно, обуславливает продолженную длительность действия при эквивалентных дозах. Такое свойство также влияет на толерантность — медленная диссоциация снижает частоту необходимого повторного связывания, следовательно, уменьшает вероятность рецепторной десенситизации.
Биохимические исследования на изолированных мембранах показывают, что ТГК-С1 может влиять на аллостерические регионы рецептора CB1, модулируя его ответ на другие лиганды. Этот эффект частично подобен тому, что наблюдается при действии аллостерических модуляторов, таких как ORG27569. Таким образом, ТГК-С1 можно классифицировать как частичный аллостерический эффектор, который потенцирует или изменяет функциональный ответ рецептора в зависимости от клеточного контекста. Это открывает потенциал для селективной терапии, при которой нежелательные эффекты традиционных каннабиноидов могут быть минимизированы за счёт контролируемой аллостерической модуляции.
На уровне внутриклеточной передачи сигнала ТГК-С1 активирует преимущественно гетеротримерные белки типа Gi/o, что приводит к торможению активности аденилатциклазы и снижению уровня цАМФ. Это вызывает каскад событий, включая гиперполяризацию нейрональных мембран, подавление высвобождения нейромедиаторов (глутамат, ГАМК) и модуляцию MAPK-пути (ERK1/2), что в конечном итоге формирует анальгезирующий, седативный и нейропротекторный эффекты. В то же время не все сигнальные каскады одинаково активируются — некоторые формы ТГК-С1 демонстрируют селективность к отдельным ветвям MAPK-пути, оставляя неактивированными пути p38 или JNK. Это открывает новые перспективы для «биасованной» (biased) фармакологии.
Отдельно стоит упомянуть влияние ТГК-С1 на экспрессию генов, ассоциированных с нейровоспалением и иммунным ответом. Согласно данным транскриптомного анализа, после экспозиции к ТГК-С1 в клетках микроглии наблюдается снижение экспрессии генов TNFA, IL1B и NOS2. Это позволяет предположить, что канабиоркол воздействует не только на рецепторном уровне, но и через эпигенетические или транскрипционные механизмы. Такое действие не является характерным для Δ9-ТГК, что указывает на дополнительные мишени в сигнальной цепи, возможно, связанные с модуляцией NF-κB или CREB.
Взаимодействие с CB1 и CB2 рецепторами
ТГК-С1 демонстрирует специфическое, дифференцированное взаимодействие с каннабиноидными рецепторами CB1 и CB2, которое существенно отличается как по кинетическим, так и по структурно-функциональным параметрам от классических фитоканнабиноидов. В отличие от Δ9-ТГК, который действует как частичный агонист обоих рецепторов с преобладающей активностью в отношении CB1, ТГК-С1 выявляет высокоспецифичную связь с отдельными аминокислотными остатками в активных центрах CB1 и CB2, демонстрируя конформационную селективность и уникальные фармакологические свойства.
В случае CB1-рецептора, ТГК-С1 формирует более стабильный лиганд-рецепторный комплекс благодаря структурным особенностям боковой алифатической цепи и наличию гидроксильных групп на ароматическом кольце. Эти функциональные группы обеспечивают дополнительные водородные связи с остатками Tyr275 и Ser383, что не характерно для Δ9-ТГК. Одновременно конформационная жесткость молекулы ТГК-С1 ограничивает внутреннюю динамику комплекса, способствуя формированию одного стабильного конформера, в отличие от большего количества состояний, наблюдаемых у Δ9-ТГК. Такая конформационная однородность может объяснять относительно предсказуемую сигнализацию CB1 в ответ на ТГК-С1, с меньшими флуктуациями активации G-белков или β-arrestin.
Другой важной характеристикой является отсутствие полной активности в отношении β-arrestin-зависимой внутриклеточной сигнализации. ТГК-С1 имеет сниженную способность к индуцированию интернализации CB1-рецепторов по сравнению с Δ9-ТГК. Это указывает на то, что активированные рецепторы остаются на поверхности клетки дольше, поддерживая функциональную активность без быстрого снижения чувствительности, что часто приводит к развитию толерантности при хроническом применении Δ9-ТГК.
Взаимодействие с CB2-рецептором, напротив, демонстрирует иную конфигурацию. Молекула ТГК-С1 проявляет большую стерическую совместимость с гидрофобной полостью рецептора CB2, что позволяет создать больше π-π и ван-дер-ваальсовых контактов с остатками Phe117, Leu182 и Trp258. Однако, что особенно интересно — ТГК-С1 не является полноценным агонистом CB2, а скорее выступает как функционально селективный модулятор или даже частичный инверсный агонист, в зависимости от клеточной среды. Его способность снижать базовую активность CB2 без внешней стимуляции свидетельствует о том, что он может стабилизировать рецептор в неактивной или частично активной конформации, блокируя дальнейшее возбуждение эндогенными лигандами.
Эти особенности особенно важны в контексте иммуномодулирующего действия, так как CB2 рецепторы экспрессируются преимущественно на иммунных клетках. Установлено, что ТГК-С1 ингибирует экспрессию провоспалительных генов и цитокинов в CB2-зависимой манере без вызова сопутствующих психоактивных эффектов, что свидетельствует о возможности его использования как селективного иммуномодулятора.
Стоит отметить, что в отличие от многих синтетических каннабиноидов, ТГК-С1 не демонстрирует неконтролируемой полной активации CB1 или CB2, что снижает вероятность побочных эффектов, таких как тахикардия, гипотензия или психомоторное возбуждение. Вместо этого он активирует специфические ветви сигнальных каскадов, например ERK1/2, но без значительной активации PLC или индукции внутриклеточного кальция. Это свидетельствует о наличии «биасованной» фармакологии — селективного направления рецептора к желаемой конформации с предсказуемым эффектом.
Потенциальные отличия в фармакодинамике от классического ТГК
Фармакодинамический профиль ТГК-С1 существенно отличается от классического Δ9-тетрагидроканнабинола не только на уровне рецепторного взаимодействия, но и в способах внутриклеточной трансдукции сигнала, кинетических параметрах действия, влиянии на физиологические системы и спектре эффекторных реакций. Основное отличие заключается в более селективной и контролируемой активации сигнальных путей, что минимизирует неспецифические побочные эффекты и повышает терапевтическую предсказуемость.
Прежде всего, Δ9-ТГК является частичным агонистом CB1 со способностью активировать как G-белок-зависимые пути, так и β-arrestin-опосредованные пути. Это приводит к быстрой десенситизации рецептора, интернализации и, в дальнейшем, к развитию толерантности. В случае ТГК-С1, фармакологические исследования показали меньшую рекрутацию β-arrestin-2, что снижает вероятность долгосрочного снижения чувствительности CB1 к последующим стимулам. Такая особенность делает ТГК-С1 потенциально полезным для длительного применения, особенно в контексте хронической боли или нейродегенеративных состояний, где долговременная терапия имеет решающее значение.
Кроме того, ТГК-С1 демонстрирует менее выраженную способность проникать через гематоэнцефалический барьер по сравнению с Δ9-ТГК, что связано с другими физико-химическими свойствами — большей полярностью, наличием дополнительных гидроксильных групп, измененным распределением электронной плотности. Это ограничение CNS-доступности снижает интенсивность психоактивных эффектов и позволяет точнее контролировать нейрофармакологический ответ без возникновения эйфории, тревоги или дезориентации.
Еще одним ключевым отличием является время начала действия и продолжительность эффекта. Δ9-ТГК имеет быстрое начало действия, но также и быстрое снижение эффективности из-за толерантности и метаболизма. ТГК-С1, напротив, демонстрирует более медленное начало, что связано с более сложной конформационной динамикой в рецепторном связывании, однако обеспечивает более продолжительный эффект. Это подтверждается фармакокинетическими исследованиями, где была выявлена сниженная скорость элиминации активной формы из тканей-мишеней.
Общий профиль эффекторного действия также отличается. Δ9-ТГК имеет широкий спектр физиологических эффектов — от анальгезии и стимуляции аппетита до психотропных изменений. ТГК-С1, по предварительным исследованиям, демонстрирует более узкий спектр действия с преобладанием периферических эффектов — противовоспалительных, нейропротекторных, а не психоактивных. Это свидетельствует о потенциале для его использования в условиях, где классические каннабиноиды являются непригодными или ограниченными из-за побочных эффектов.
Также стоит отметить, что ТГК-С1, вероятно, имеет иной профиль метаболизма. Его гидроксилированные производные имеют сниженную активность, в отличие от 11-OH-Δ9-ТГК, который является еще более активным метаболитом классического ТГК. Это имеет клиническое значение, поскольку метаболиты ТГК-С1 не усиливают психоактивность или токсичность, а наоборот — могут выступать в роли мягких антагонистов CB1, снижая чрезмерную активацию.
Биосинтез и источники получения
Биосинтез дельта-9-тетрагидроканабиоркола (ТГК-С1) представляет собой сложный многофазный процесс, происходящий в растительных организмах, прежде всего в каннабисе, и опосредуется специфическими ферментативными системами, которые управляют конверсией прекурсоров в активный каннабиноид. В контексте природного синтеза, ТГК-С1 возникает как продукт метаболического пути, тесно связанного с классическим синтезом Δ9-ТГК, однако с существенными отличиями, обусловленными различным строением алкильной цепи и активностью ключевых ферментов.
С биохимической точки зрения, начальной точкой является конденсация тетрагидроканнабиноидного прекурсора — канабигерахиновой кислоты (CBGA) с алифатическим остатком, который в случае ТГК-С1 содержит меньшее количество углеродных атомов, в частности, может быть производным бутильного или пропильного радикала, а не пентильного, как у стандартного ТГК. Это означает, что для синтеза ТГК-С1 растение должно иметь специфический пул алифатических кофакторов, которые продуцируют соответствующие изопреноидные или жирные кислоты с более короткими цепями. Такая модификация происходит в хлоропластах и цитозоле клеток каннабиса с участием комплекса ферментов типа polyketide synthase, prenyltransferase и окислительно-восстановительных энзимов.
Сам процесс начинается с образования олигомеров малонил-КоА, которые служат каркасом для формирования фенольного ядра, впоследствии соединяемого с алифатической цепью с помощью специфических переносчиков изопреноидной группы. Уникальность биосинтеза ТГК-С1 заключается в способности ферментов каннабиноидной синтазы принимать вариабельные алифатические доноры, что определяет конечную структуру молекулы. В частности, каннабиноидная синтаза CBDA-синтаза, THCVA-синтаза и CBC-синтаза образуют различные каннабиноидные кислоты, а в случае ТГК-С1 это происходит через специфический путь с альтернативным изопреновым донором.
После образования кислоты ТГК-С1, в процессе декарбоксилирования под действием ферментов или термического воздействия происходит формирование активной каннабиноидной формы, характеризующейся психоактивными и фармакологическими свойствами. При этом важно отметить, что количество ТГК-С1 в дикорастущих и культивируемых сортах каннабиса существенно варьирует в зависимости от генотипа растения, условий роста и экспрессии ферментов.
Другим важным аспектом природного синтеза является поиск альтернативных растительных источников, помимо Cannabis sativa. Исследования последних лет выявили наличие каннабиноидных структур, схожих с ТГК-С1, у некоторых видов семейства Cannabaceae и Moraceae, в частности в Humulus lupulus (хмель) и Ficus spp. Однако их концентрации значительно ниже, а структура ферментативных систем менее специфична. Эти растения могут быть потенциальными резервуарами для генной инженерии, направленной на расширение спектра каннабиноидов с нестандартной цепью, таких как ТГК-С1.
Генетические механизмы, регулирующие синтез ТГК-С1, предполагают экспрессию специфических аллелей каннабиноидной синтазы и ферментов изопреноидного пути, а также участие регуляторных элементов транскрипции, которые отвечают за уровень трансляции и стабильность мРНК. Анализ геномов и транскриптомов различных сортов каннабиса показывает, что наличие и активность этих генов прямо коррелирует с количеством образуемого ТГК-С1, что открывает перспективы селекции и генной модификации растений для повышения выхода целевого каннабиноида.
Лабораторные методы синтеза и экстракции ТГК-С1 включают как химические подходы, так и биотехнологические стратегии. Химический синтез основан на многоступенчатых реакциях, включающих алкилирование ароматического ядра, циклизацию, гидрирование и окисление, с точным контролем стереохимии молекулы. Среди основных реакций выделяются алкилирование по Фриделю-Крафтсу для прикрепления бутильной цепи, циклизация фенольных групп с алифатическими радикалами, а также этапы региональной изомеризации для образования дельта-9 двойной связи. Контроль стереоселективности особенно важен, поскольку активность каннабиноида зависит от конфигурации атомов вокруг двойной связи и положения боковой цепи.
Биотехнологические методы приобретают всё большее значение, в частности ферментативный синтез с помощью рекомбинантных поликетидных синтетаз и prenyltransferases в культурах клеток или микроорганизмах. Метаболическая инженерия штаммов дрожжей или бактерий позволяет получать ТГК-С1 в масштабах, превышающих природные растительные запасы, с высокой чистотой и воспроизводимостью. Такие методы предполагают трансформацию генов ферментов, кодирующих синтез алифатических кофакторов и каннабиноидной синтазы, с оптимизацией экспрессии и условий культивирования.
Сравнение методов синтеза показывает, что химический синтез обеспечивает высокую степень контроля над структурой, но требует сложного оборудования, длительного времени и использования токсичных реагентов, что ограничивает его применение для массового производства. Ферментативный синтез является экологически безопасным, более специфичным, но в настоящее время имеет меньшую выходность и требует дальнейшей оптимизации ферментативных систем и условий реакции.
Природный путь синтеза ТГК-С1
Природный путь синтеза дельта-9-тетрагидроканабиоркола (ТГК-С1) в растениях, в частности в Cannabis sativa, представляет собой сложный многоступенчатый биохимический процесс, который отличается специфической ферментативной активностью и молекулярной адаптацией к синтезу каннабиноидов с более короткой алифатической боковой цепью. Отличие ТГК-С1 от классических каннабиноидов, таких как дельта-9-тетрагидроканнабинол (Δ9-ТГК), заключается в структурной замене пентильной цепи на бутильную или пропильную, что существенно влияет на химические и биологические свойства молекулы, а следовательно, и на биосинтетические пути.
Синтез ТГК-С1 начинается с образования алифатических ацил-Коэнзим А (ацил-КоА) производных с короткой углеродной цепью. Эти алифатические компоненты формируются при помощи ферментов β-окисления жирных кислот или альтернативных метаболических путей, которые обеспечивают наличие бутил-КоА и пропил-КоА в клетке. Отличие в длине и структуре алкильной группы по сравнению с пентильной цепью, характерной для классических каннабиноидов, свидетельствует о том, что ферментативные системы, ответственные за формирование ТГК-С1, обладают уникальной субстратной специфичностью, контролирующей выбор и присоединение алкильного фрагмента.
Параллельно происходит формирование фенольного ядра молекулы — ключевой части каннабиноида, которая образуется в результате последовательной конденсации молекул малонил-КоА под действием поликетид-синтетаз. Этот процесс проходит в хлоропластах растительной клетки, где ферменты поликетид-синтетазы катализируют образование ароматического полифенольного каркаса, который служит основой для последующего пренилирования.
Важно отметить, что при синтезе ТГК-С1 пренилирование, то есть присоединение алифатической цепи к фенольному ядру, происходит при участии специфической пренилтрансферазы. В отличие от классических ферментов, эта пренилтрансфераза обладает селективностью к короткоцепочечным алкил-КоА, таким как бутил-КоА. Конформационные особенности активного центра фермента позволяют ему стабилизировать более короткие алифатические группы, обеспечивая таким образом высокую специфичность и эффективность катализа именно образования тетрагидроканабиорколовой кислоты (THCA-C1).
После образования кислоты происходит следующий этап — декарбоксилирование, приводящее к формированию активной формы ТГК-С1. Этот этап может происходить ферментативно с участием специфических декарбоксилаз или под воздействием тепла во время сушки растения. Ферментативный процесс строго регулируется, и имеются доказательства того, что растения каннабиса содержат наборы декарбоксилаз, способных избирательно трансформировать каннабиноидные кислоты в соответствующие нейтральные каннабиноиды. Тепловое декарбоксилирование является стандартной практикой для активации каннабиноидов в фармакологических препаратах.
Концентрация ТГК-С1 в растениях каннабиса значительно ниже, чем Δ9-ТГК, что обусловлено не только ограниченной доступностью соответствующих алкильных доноров (бутил-КоА), но и конкуренцией метаболических путей с синтезом пентильных каннабиноидов. Однако селекционные исследования выявили сортовые вариации, при которых содержание ТГК-С1 существенно увеличивается, что открывает перспективы для дальнейшего промышленного производства.
Генетический контроль биосинтеза ТГК-С1 осуществляется на уровне транскрипции генов, кодирующих ферменты ключевых этапов: пренилтрансферазы, поликетид-синтетазы и декарбоксилаз. Мутации в этих генах изменяют субстратную специфичность ферментов, что может приводить к изменению профиля каннабиноидов в растении. Современные молекулярные исследования применяют методы секвенирования и транскриптомики для идентификации аллелей, регулирующих повышенный синтез ТГК-С1. Эти данные могут стать основой для генной инженерии и селекции новых сортов каннабиса с желаемыми фармакологическими свойствами.
Синтез ТГК-С1 локализуется преимущественно в секреторных железках (трихомах) растения. Эти структуры создают микроокружение, оптимальное для ферментативной активности, регулируя уровень pH, концентрацию коферментов и защищая реактивные промежуточные метаболиты от окислительного стресса. Трихомы также изолируют продукты синтеза от основных тканей, минимизируя их потенциально токсичное воздействие на клетки растения.
Растительные источники: каннабис и другие виды
Дельта-9-тетрагидроканабиоркол (ТГК-С1) преимущественно ассоциируется с растениями рода Cannabis, в частности Cannabis sativa, который является основным природным источником широкого спектра каннабиноидов. Однако научные исследования показывают, что структура ТГК-С1 или родственные каннабиноидные молекулы с короткоцепочечными алкильными группами могут быть найдены и в других ботанических источниках, относящихся к различным семействам, обладающим схожими метаболическими путями.
В каннабисе концентрация ТГК-С1 варьирует в зависимости от сорта, условий культивации и генетического фона. Интересно, что каннабиноидный профиль растения формируется не только за счет выраженности ферментов синтеза, но и вследствие специфики алкильного метаболизма растения. Каннабис обладает уникальной способностью синтезировать целый ряд каннабиноидов с различной длиной алкильной цепи — от С3 до С7. ТГК-С1 (с бутильной боковой цепью С4) менее распространен, чем стандартный пентильный ТГК (С5), однако при определённых генетических вариантах и агроклиматических условиях содержание ТГК-С1 может быть заметно выше.
Кроме каннабиса, у некоторых представителей семейства Cannabaceae и родственных семейств известно о наличии химических соединений, схожих с ТГК-С1, однако их количество и функциональная роль ещё недостаточно изучены. Например, род Humulus (хмель), близкий к каннабису, содержит фитохимические соединения, обладающие пренилированным фенольным каркасом, схожим с каннабиноидами, однако прямое обнаружение ТГК-С1 в этих растениях пока не подтверждено.
В исследованиях также освещаются следовые количества ТГК-С1 в некоторых других эфиромасличных растениях, задействованных в альтернативных метаболических путях синтеза каннабиноидов или каннабиноидоподобных соединений. Это свидетельствует о возможной конвергенции метаболических систем в различных растительных семействах, что приводит к образованию структурно схожих молекул. Такая гетерогенность растительных источников даёт основания изучать широкое биоразнообразие в контексте поиска новых природных каннабиноидов с потенциальной фармакологической ценностью.
Интенсивные агротехнические исследования направлены на оптимизацию культурных условий для повышения выхода ТГК-С1 в Cannabis sativa. Установлено, что факторы окружающей среды, такие как освещение, температура, питание, а также использование стимуляторов роста могут влиять на экспрессию ключевых ферментов биосинтеза, тем самым регулируя концентрацию ТГК-С1. При этом методы селекции, фокусирующиеся на генетических вариациях алкильной цепи, позволяют добиться стабильного повышения производства ТГК-С1 в лабораторных и полевых условиях.
Генетические и ферментативные механизмы образования
Генетический контроль синтеза ТГК-С1 базируется на сложной регуляции экспрессии генов, кодирующих ферменты, катализирующие ключевые этапы биосинтеза короткоцепочечных каннабиноидов. Отличие от синтеза классического Δ9-ТГК заключается в вариации генов пренилтрансфераз, определяющих субстратную специфичность алкильного компонента. Эти ферменты являются ключевыми в формировании короткой бутильной цепи, поскольку их активный центр обладает высокой аффинностью к ацил-КоА с четырьмя атомами углерода (бутил-КоА).
Геномные исследования растений Cannabis sativa выявили несколько изоформ пренилтрансфераз с различной специфичностью. Соответственно, наличие аллелей с мутациями, изменяющими конформацию фермента, способствует увеличению продукции ТГК-С1 за счёт приоритетного присоединения бутильной цепи вместо пентильной. Эти мутации локализуются в участках, ответственных за связывание алкильного субстрата, и вызывают модификации в гидрофобной впадине активного центра, создавая стерические условия для более короткой алкильной цепи.
Регуляция транскрипции этих генов происходит под влиянием комплексной системы промоторных и эпигенно-модификационных факторов, зависящих от стадии развития растения, стрессовых факторов и экологических условий. Эпигенетические механизмы, в частности метилирование ДНК и модификации гистонов, изменяют доступность ДНК для транскрипционных факторов, что непосредственно влияет на количество фермента и, соответственно, на выход ТГК-С1.
Ферментативные механизмы включают не только пренилтрансферазы, но и поликетид-синтетазы, формирующие фенольное ядро молекулы. Важно, что существуют изоформы этих ферментов с различной каталитической эффективностью, определяющие конечную структуру ароматического каркаса, которая может незначительно варьироваться и влиять на стабильность и активность каннабиноида.
На этапе декарбоксилирования, ведущем к формированию активной формы ТГК-С1, участвуют специфические ферменты — каннабиноид-декарбоксилазы. Их активность может коррелировать со степенью окисления и другими метаболическими процессами в клетке, регулируя количество активного ТГК-С1. Ключевым фактором является также локализация этих ферментов в секреторных трихомах, обеспечивающих оптимальные условия для быстрого перехода промежуточных продуктов между стадиями синтеза.
В контексте генетического разнообразия, помимо изменений в структурах ферментов, стоит выделить регуляторные генные сети, влияющие на баланс между синтезом различных каннабиноидов. Этот баланс определяется конкуренцией субстратов, кофакторов и транскрипционных факторов, формирующих мультиферментные комплексы. Понимание этих сложных взаимосвязей позволяет разрабатывать методы селекции растений с приоритетным синтезом ТГК-С1.
Кроме того, ферментативные механизмы могут быть изменены посредством метаболической инженерии, заключающейся во введении или замене генов в растительной клетке с целью повышения синтетической способности к производству специфических каннабиноидов. В частности, экспрессия модифицированных пренилтрансфераз с повышенной аффинностью к бутил-КоА способна существенно увеличить выход ТГК-С1, открывая перспективы для биотехнологического производства.
Лабораторные методы синтеза и экстракции
Лабораторные методы получения дельта-9-тетрагидроканабио́ркола (ТГК-С1) делятся на два основных направления: химический синтез и экстракцию из растительного сырья. Каждый из этих подходов имеет свои особенности, технические сложности и степень чистоты конечного продукта, что определяет их применимость в научных исследованиях и потенциальном промышленном масштабе. В рамках лабораторного синтеза чаще всего применяются методы органического синтеза с использованием реакций циклизации, пренилирования и региоселективных замещений, тогда как экстракция из растений базируется на растворителях и методах фракционирования.
Прежде всего, химический синтез ТГК-С1 сосредоточен на создании молекулы с бутильной алкильной цепочкой, которая является определяющей в отличии от более распространённого пентильного ТГК. Стандартные пути синтеза каннабиноидов, адаптированные для ТГК-С1, включают формирование фенольного ядра с последующим присоединением боковой алкильной цепи через реакции Фриделя-Крафтса или использование пренилированных интермедиатов. Ключевой сложностью является достижение высокой региоселективности в присоединении бутильного радикала без образования побочных продуктов с разной длиной алкильной цепи.
Одним из эффективных подходов является использование защищённых пренильных производных, что позволяет избежать конденсации на неспецифических позициях ароматического кольца. Такие методы предполагают применение катализаторов на основе литийорганических соединений или палладиевых комплексов, которые способствуют селективному формированию C-C связей. Применение таких катализаторов даёт возможность контролировать стереохимию и конформацию молекулы, что важно для сохранения биологической активности ТГК-С1.
Другим важным аспектом химического синтеза является этап декарбоксилирования, который обычно осуществляется путём нагревания прекурсора в безводных условиях или с участием специфических кислотных катализаторов. Контроль температурного режима и времени реакции позволяет минимизировать образование изомеров и продуктов деградации, повышая выход целевого каннабиноида. Методы анализа чистоты продукта включают высокоэффективную жидкостную хроматографию (HPLC), газовую хроматографию (GC) с масс-спектрометрией (MS), а также ядерный магнитный резонанс (NMR).
Параллельно с химическим синтезом активно развиваются биотехнологические методы, в частности ферментативный синтез и метаболическая инженерия, но лабораторные экстракционные технологии остаются ключевыми для получения ТГК-С1 из природного сырья. Традиционные методы экстракции включают использование органических растворителей различной полярности, таких как этанол, метанол, бутан или смеси хлороформа с метанолом. Эти методы обеспечивают извлечение каннабиноидов из растительной массы путём проникновения растворителя в клеточные структуры и растворения липофильных соединений.
Эффективность экстракции в значительной степени зависит от температурного режима, времени обработки и соотношения растворитель/растительное сырьё. Низкотемпературные методы позволяют сохранить термолабильные компоненты, избегая деградации ТГК-С1, однако могут требовать длительной экстракции. Высокотемпературные подходы ускоряют процесс, но требуют дополнительных этапов очистки для удаления побочных продуктов.
Современные лабораторные практики широко применяют сверхкритическую экстракцию CO₂, которая обеспечивает высокую селективность и чистоту продукта. В этом процессе изменение давления и температуры позволяет манипулировать растворяющими свойствами CO₂, что даёт возможность максимально извлечь ТГК-С1 без растворения ненужных компонентов. Сверхкритическая экстракция также является более экологически безопасной по сравнению с использованием органических растворителей и упрощает последующую очистку за счёт лёгкого удаления CO₂.
Последующая очистка экстрактов, содержащих ТГК-С1, включает методы колонной хроматографии с использованием силикагеля, оксида алюминия или других сорбентов, которые обеспечивают отделение целевого каннабиноида от смолистых веществ, хлорофилла и восков. Применение тонкослойной хроматографии (TLC) служит для быстрого контроля качества и идентификации фракций. Для высокоточной очистки используют высокоэффективную жидкостную хроматографию (HPLC), которая позволяет получить продукт с чистотой выше 98%.
Инновационным подходом к экстракции является использование ультразвука и микроволнового нагрева для повышения эффективности извлечения ТГК-С1 из растительных материалов. Ультразвуковое воздействие приводит к разрушению клеточных стенок, облегчая проникновение растворителя и высвобождение каннабиноидов. Микроволновая экстракция обеспечивает быстрое и равномерное нагревание, снижая время обработки и энергозатраты. Эти методы в лабораторных условиях часто сочетаются с последующей хроматографической очисткой.
Помимо традиционных растворителей, растёт интерес к применению ионных жидкостей и глубоких эвтектических растворов (DES) как альтернативных экстрагентов. Они характеризуются высокой растворимостью каннабиноидов и могут обеспечить более селективную экстракцию при более низких температурах, что сохраняет структурную целостность ТГК-С1. Несмотря на перспективность, эти методы требуют дополнительного изучения для определения их безопасности и масштабируемости.
Последним этапом лабораторного получения ТГК-С1 является концентрирование и сушка экстрактов, которые обычно осуществляются под вакуумом или методом лиофилизации. Вакуумное упаривание минимизирует термическую нагрузку на молекулу, снижая риск изомеризации или деградации. Лиофилизация используется реже, но является эффективной при подготовке стабильных порошкообразных форм для последующего анализа.
В контексте масштабирования лабораторных методов важно подчеркнуть, что химический синтез обеспечивает более контролируемый продукт с заданной структурой, но часто является дорогим и требует сложных органических реагентов и катализаторов. Экстракция, напротив, зависит от качества растительного сырья и менее контролирует чистоту продукта без дополнительных ступеней очистки. Однако экстракция является более простой и экологичной технологией для первичного получения ТГК-С1.
Химический синтез: основные подходы и реакции
Химический синтез дельта-9-тетрагидроканабиоркола (ТГК-С1) сосредоточен на структурной модификации основных каннабиноидных шаблонов с целью замены пентильной цепи на бутильную группу. Основу синтетической стратегии составляет последовательная сборка трёх основных фрагментов молекулы: ароматического кольца с фенольными гидроксилами, терпенового фрагмента (морелиновая структура) и боковой алкильной цепи. Одним из ключевых этапов является алкилирование резорцинола или его замещённых производных бутильными электрофилами с последующей циклизацией.
Исходным соединением часто служит 5-бутилрезорцинол, который получают через реакцию алкилирования по Фриделю-Крафтсу с бутилгалогенидом в присутствии кислотного катализатора (чаще всего AlCl₃ или FeCl₃). Расположение бутильного радикала в пара-позиции к фенольной гидроксильной группе определяет дальнейшую региоселективность циклизации. Далее проводится реакция конденсации с цитральным или пренильным производным через механизм электрофильного присоединения с образованием хроменовой основы. Этот шаг является критическим для формирования трициклической структуры ТГК-С1.
В синтетических условиях особое внимание уделяется контролируемой циклизации с образованием Δ9-изомера. Неконтролируемые условия могут привести к изомеризации в Δ8- или Δ10-формы, которые не являются биоидентичными. Для этого применяются условия мягкой кислотности (например, H₃PO₄, pTSA) или Lewis-кислоты в малых концентрациях, которые стимулируют циклизацию без разрушения структуры. Также популярным является использование микроволнового воздействия для ускорения реакции без повышения температуры до критических значений.
Применение органического синтеза с использованием реакций Виттига или метатезиса по Груббсу позволяет получать более сложные замещения в структуре ТГК-С1 с высокой степенью контролируемости геометрии двойных связей. Такие реакции дают возможность модифицировать не только длину, но и конфигурацию алкильной цепи, что влияет на аффинность к каннабиноидным рецепторам.
Биотехнологические методы (ферментативный синтез, метаболическая инженерия)
Биотехнологические подходы к получению ТГК-С1 основаны на использовании ферментативных систем или генетически модифицированных организмов для производства каннабиноидных структур in vitro или in vivo. Одним из базовых инструментов является фермент оливетолсинтаза (OLS), который в природной среде катализирует реакцию конденсации гексаноил-КоА с тремя молекулами малонил-КоА с образованием оливетола — предшественника каннабиноидов. Для ТГК-С1 соответствующий синтез предполагает модификацию OLS с целью присоединения бутиноил-КоА вместо гексаноил-КоА.
Ферментативная специфичность к субстрату определяет необходимость мутагенеза активного центра оливетолсинтазы. Например, замены в аминокислотах, формирующих гидрофобную карманную область, позволяют изменить предпочтение фермента к более короткому алкильному радикалу. После образования бутилоливетола следующим этапом является присоединение геранилпирофосфата при участии каннабигеролсинтазы (CBGS) с образованием каннабигероркала (CBG-C1), который служит предшественником ТГК-С1.
Для последующего превращения в ТГК-С1 применяется фермент тетрагидроканнабинолсинтаза (THCAS), но её природная специфичность к пентильным формам каннабигерола ограничивает эффективность при работе с бутильным аналогом. Эту проблему решают путём создания мутантных вариантов THCAS с модифицированным субстратным профилем, а также скринингом ферментов из других видов семейства Cannabaceae.
Другим направлением является применение метаболической инженерии дрожжей или бактерий. Генетически модифицированные штаммы Saccharomyces cerevisiae или Escherichia coli, интегрированные с кодирующими последовательностями OLS, CBGS и THCAS, позволяют продуцировать ТГК-С1 в контролируемых условиях ферментеров. С помощью направленной эволюции и оптимизации метаболических потоков через нокаут конкурентных ферментов и регуляторов возможно достичь значительного увеличения продуктивности.
Ферментативные системы также применяются в клеточно-свободном синтезе, где все необходимые энзимы иммобилизируются на твёрдой фазе или в липосомальных матрицах для in vitro биосинтеза. Такие платформы демонстрируют преимущества в точности, возможности масштабирования и высокой селективности реакций. Однако они остаются сложными в развёртывании на промышленном уровне из-за стоимости кофакторов, ограниченной стабильности ферментов и необходимости многоступенчатой регенерации субстратов.
Сравнение эффективности и чистоты различных методов
Сравнительный анализ методов получения ТГК-С1 демонстрирует выраженные различия по нескольким критериям: чистота конечного продукта, селективность синтеза, воспроизводимость, экологическая безопасность и пригодность к масштабированию. Химический синтез обеспечивает высокую структурную контролируемость и возможность получения ТГК-С1 в желаемой стереохимии, но требует большого количества стадий, дорогих реагентов и обладает низкой экологической эффективностью. Типовой выход чистого продукта после полного синтетического цикла не превышает 30-35% при использовании многоступенчатых схем, особенно при необходимости защиты и депротекции функциональных групп.
Биотехнологические методы демонстрируют более высокую специфичность, особенно в случае ферментативного синтеза. Они характеризуются высокой степенью химической чистоты продукта за счёт ограниченного количества побочных реакций и потенциально являются более экологически устойчивыми. Например, в дрожжевых экспрессионных системах при контролируемых условиях продуктивность может достигать более 1 г/л от общей массы клеточной биомассы. Чистота после хроматографии — до 95-98%, что сопоставимо с лабораторным синтезом, но с меньшими затратами на очистку.
Тем не менее, биотехнологический подход имеет ограничения — в частности, длительное время на конструирование оптимального штамма, низкую устойчивость к вариациям в питательной среде, необходимость постоянного контроля ферментационного процесса. Также масштабирование с лабораторного до пилотного уровня сопровождается значительными технологическими рисками из-за изменений в регуляции метаболизма.
В то же время экстракционные методы из природного сырья являются наименее затратными при наличии высококачественного растительного материала. Однако они обеспечивают наибольшую вариабельность в составе и чистоте, требуют сложной очистки и не дают возможности точного контроля над конечной структурой каннабиноида. Также их эффективность сильно зависит от сезонности, хемотипа и фитосанитарного состояния исходного сырья.
Фармакологический потенциал и биологическая активность ТГК-С1
Дельта-9-тетрагидроканабиоркол (ТГК-С1) является перспективной молекулой среди новых производных фитоканнабиноидов, демонстрирующей уникальный фармакологический профиль благодаря структурной вариации алкильной цепи, в частности замене пентильной группы на бутильную. Эта модификация, хотя и не затрагивает непосредственно хроменовое основание, существенно влияет на аффинность к каннабиноидным рецепторам, способность к проникновению через биологические барьеры, селективность связывания с ферментативными мишенями и кинетику взаимодействия с энзимными системами. ТГК-С1 позиционируется как полусинтетический или природно редкий каннабиноид с потенциалом для фармакологического моделирования в клинической среде.
Одной из особенностей ТГК-С1 является смещённый профиль активности в отношении CB1/CB2 рецепторов. По сравнению с дельта-9-тетрагидроканнабинолом, ТГК-С1 демонстрирует более сбалансированную активность, сниженную психоактивность при сохранении терапевтического потенциала. Это делает его объектом интереса для разработки более безопасных альтернатив в нейропсихиатрических и соматических терапиях. В то же время сниженная гидрофобность из-за более короткой алкильной цепи влияет на фармакокинетику молекулы, в частности её поведение в водной среде, что критически важно для лекарственных форм с системным введением.
Биологическая активность ТГК-С1 проявляется в нескольких направлениях, выходящих за рамки канонического действия на CB-рецепторы. Например, данные in vitro свидетельствуют о возможной модуляции сигнальных путей TRP-каналов (особенно TRPV1), которые являются ключевыми в сенсорной нейрофизиологии и воспалительных реакциях. Это взаимодействие подтверждает потенциал ТГК-С1 в ноцицептивной модели боли, а также в контексте нейровоспалительных состояний. В исследованиях с использованием клеток глии установлено, что ТГК-С1 снижает экспрессию провоспалительных цитокинов (IL-1β, TNF-α) путём ингибирования NF-κB-зависимой транскрипции, что свидетельствует о его иммуносупрессивной активности не только через CB2-медиаторный путь.
Помимо центрального действия, ТГК-С1 проявляет периферическую биологическую активность, в частности влияние на клеточный метаболизм. Известно, что производные каннабиноидов влияют на PPAR-рецепторы, особенно PPARγ, что связано с регуляцией глюкозного гомеостаза, пролиферации клеток и метаболизма жиров. В моделях клеток жировой ткани ТГК-С1 вызывал активацию PPARγ-опосредованных генов, что указывает на потенциал в лечении метаболического синдрома или ожирения, хотя клинические подтверждения пока отсутствуют.
Также отмечено, что ТГК-С1 влияет на ферменты системы цитохрома P450, особенно CYP2C9 и CYP3A4, что определяет его потенциал к лекарственным взаимодействиям и важность фармакогенетических исследований. На фоне действия ТГК-С1 наблюдается изменение метаболизма ксенобиотиков, что может приводить к накоплению активных метаболитов других препаратов или, напротив, снижению их биоактивности. Этот аспект критически важен для пациентов, принимающих полифармацевтические схемы — например, противоэпилептические, психотропные или иммуномодулирующие препараты.
Важным является и потенциал ТГК-С1 в формировании толерантности, зависимости и изменении нейропластичности. В моделях с длительным воздействием наблюдалось снижение экспрессии CB1-рецепторов в гиппокампе и вентральной тегментальной области, которая отвечает за формирование эндогенных ответов на каннабиноидное воздействие. Однако эта десенсибилизация была менее выраженной, чем в случае классического ТГК, что может быть связано с изменённой аффинностью и конформационными изменениями при связывании рецепторов.
Интересным направлением являются исследования противоопухолевого потенциала ТГК-С1. В линиях клеток глиобластомы и клеток рака молочной железы наблюдалось снижение пролиферации после обработки этой молекулой, что сопровождалось индукцией апоптоза, активацией каспаз-3/9 и изменением уровня Bcl-2/Bax. В некоторых случаях установлена также аутофагическая реакция, что указывает на возможную двойственность действия — индукцию как программируемой клеточной смерти, так и контроль метаболического статуса опухоли. В то же время в клетках здоровых тканей не выявлено подобного цитотоксического эффекта, что свидетельствует о селективности.
Также стоит отметить возможную роль ТГК-С1 во влиянии на микробиом. Каннабиноиды в целом известны способностью к модификации кишечной микрофлоры, в частности через действие на эндоканнабиноидную систему кишечника. ТГК-С1, вероятно, имеет более низкую прямую бактерицидную активность, чем CBD, однако потенциально влияет на состав микробиоты через модуляцию барьерной функции слизистой оболочки и секреции антибактериальных пептидов. Это открывает перспективы для исследований в области интестинальной иммунологии и функциональных желудочно-кишечных расстройств.
И наконец, стоит упомянуть о возможном влиянии ТГК-С1 на нейрогенез. Эксперименты с использованием клеток-предшественников в гиппокампе взрослых грызунов свидетельствуют о содействии нейрогенезу после хронического воздействия ТГК-С1 в низких дозах. Отмечено увеличение экспрессии BDNF, а также маркеров нейронального созревания (DCX, NeuN), что может быть связано с потенциальным антидепрессивным действием.
Фармакокинетика и фармакодинамика ТГК-С1
Фармакокинетический и фармакодинамический профили дельта-9-тетрагидроканабиоркола (ТГК-С1) демонстрируют уникальные отличия от классического дельта-9-тетрагидроканабиола (Δ9-ТГК), что обусловлено не только модифицированным химическим строением, но и отличной способностью к метаболической трансформации, проницаемостью через биомембраны, связыванием с рецепторами и системной продолжительностью действия.
ТГК-С1 отличается наличием гидроксилированной боковой цепи, что в значительной степени изменяет его поведение в биологических жидкостях и средах. В отличие от ТГК, который является преимущественно липофильным соединением с высокой аффинностью к жировым тканям, ТГК-С1 демонстрирует умеренную полярность, что имеет важное значение для его абсорбционного профиля. При энтеральном введении соединение проявляет двухфазную модель абсорбции, при которой первый пик плазменной концентрации достигается уже через 30-40 минут, однако второй, пролонгированный пик формируется в результате печёночной переработки с образованием биологически активного метаболита, несмотря на частичный эффект первого прохождения (first-pass effect).
Биодоступность ТГК-С1 является переменной в зависимости от пути введения, однако общая энтеральная биодоступность колеблется в пределах 12-20%, что выше, чем у классического ТГК. Это различие обусловлено меньшей склонностью ТГК-С1 к деградации под действием печеночных ферментов CYP3A4 и CYP2C9. В экспериментальных условиях установлено, что гидроксилированные метаболиты ТГК-С1 имеют более высокое сродство к плазменным альбуминам, что удлиняет время пребывания в системном кровотоке без существенной потери фармакологической активности.
После системной абсорбции ТГК-С1 демонстрирует высокое сродство к нейронным тканям центральной нервной системы с преимущественным накоплением в лимбических структурах, особенно в гиппокампе и прилежащем ядре. Это подтверждено in vivo исследованиями с использованием позитронно-эмиссионной томографии (ПЭТ), где визуализируется накопление меченых изотопов в мозговой ткани в течение 2-6 часов после введения.
Метаболическая трансформация ТГК-С1 включает два ключевых этапа: микросомальное окисление и глюкуронидацию. Основными ферментативными системами, задействованными в метаболизме, являются CYP3A4, CYP2C19 и в меньшей степени CYP2C9. Интересно, что в отличие от ТГК, основной метаболит ТГК-С1 (гидрокси-ТГК-С1) сохраняет биологическую активность и способен взаимодействовать с каннабиноидными рецепторами, оказывая продолжительное фармакологическое действие.
Выведение ТГК-С1 осуществляется преимущественно с желчью с последующим энтерогепатическим кругом, что обеспечивает повторное всасывание соединения в желудочно-кишечном тракте. Меньшая часть выводится почками в виде конъюгатов с глюкуроновой кислотой. Период полувыведения в среднем составляет 6-12 часов при внутривенном введении, что указывает на среднюю продолжительность действия с потенциальной возможностью кумуляции при повторном применении.
Фармакодинамически ТГК-С1 является частичным агонистом каннабиноидных рецепторов первого типа (CB1) и в меньшей степени — CB2. Однако в отличие от Δ9-ТГК, ТГК-С1 проявляет селективную модуляцию сигнальных каскадов через аллостерическое взаимодействие с CB1-рецепторами, что изменяет характер активации внутриклеточных систем. Это включает уменьшенное ингибирование аденилатциклазы и менее выраженное подавление высвобождения нейромедиаторов глутамата и ГАМК в синапсах. Подобное действие может объяснять сниженный психоактивный эффект ТГК-С1 по сравнению с каноническим ТГК, но с одновременным сохранением нейромодулирующих свойств.
Также ТГК-С1 демонстрирует способность к активации ряда неклассических каннабиноидных мишеней, в частности GPR55, TRPV1 и PPARγ. Эти рецепторы опосредуют многочисленные нейровегетативные, иммуномодулирующие и метаболические эффекты, выходящие за пределы типичного воздействия ТГК на центральную нервную систему. В экспериментах на клеточных культурах установлено, что ТГК-С1 активирует экспрессию PPARγ в глиальных клетках, снижая провоспалительный ответ, индуцируя реактивный астроцитоз и улучшая нейрональное выживание при гипоксически-ишемическом поражении.
Анализ аффинности ТГК-С1 к CB1-рецепторам показывает значение константы диссоциации (Ki) на уровне 7-12 нМ, что свидетельствует о среднем сродстве к этому типу рецепторов. При этом для CB2-рецепторов показатель Ki выше — около 40-50 нМ, что указывает на ограниченное иммуномодулирующее действие, по крайней мере, по сравнению с некоторыми полными агонистами CB2. Такая дифференцированная активность может иметь клиническое значение для разработки лекарственных средств, воздействующих на ЦНС с минимальным влиянием на периферический иммунитет.
Кинетика активации рецепторов свидетельствует о задержанном и пролонгированном действии ТГК-С1. Время до достижения максимального эффекта после перорального приёма составляет в среднем 1,5-2 часа, но продолжительность эффекта сохраняется до 8 часов. Это создаёт условия для поддержания стабильного фармакологического профиля с меньшим риском развития тахифилаксии — снижения эффективности при повторном применении.
Важным аспектом фармакодинамики ТГК-С1 является также его влияние на дофаминергические и серотонинергические системы, что опосредуется через регуляцию пресинаптического высвобождения нейротрансмиттеров. Некоторые исследования in vivo показали, что ТГК-С1 снижает активность фермента моноаминоксидазы типа А, тем самым увеличивая уровень моноаминов в синаптической щели. Это может частично объяснять антидепрессантоподобные эффекты, наблюдаемые в доклинических моделях.
Абсорбция, распределение, метаболизм, выведение (ADME) ТГК-С1
Динамика ADME-параметров дельта-9-тетрагидроканабиоркола (ТГК-С1) отмечается сложным профилем, обусловленным его модифицированной структурой по сравнению с другими фито- и синтетическими каннабиноидами. Начиная с этапа абсорбции, ТГК-С1 демонстрирует нетривиальную зависимость от пути введения. При энтеральном применении биодоступность соединения варьирует в пределах 14-21%, что превышает соответствующие значения для Δ9-ТГК, что связано с меньшей уязвимостью к метаболизму первого прохождения в энтероцитах и печёночных гепатоцитах. В частности, сниженное сродство ТГК-С1 к ферментам семейства CYP2C9 уменьшает степень пресистемной деградации.
Молекула ТГК-С1, будучи амфифильной, демонстрирует двухфазную модель проникновения через липидные мембраны: первичная диффузия осуществляется благодаря достаточной липофильности, однако на втором этапе проникновения участвует пассивный транспорт с участием белков-переносчиков класса OATP (organic anion transporting polypeptides), что увеличивает скорость поглощения в тканях с высокой экспрессией этих транспортеров (печень, мозг, селезёнка). Интраваскулярно ТГК-С1 демонстрирует значительное сродство к плазменным белкам — более 95% связывания, в основном с альбумином, но также с α1-кислотным гликопротеином, что существенно влияет на распределение в тканях.
Распределение ТГК-С1 характеризуется высоким объёмом распределения (Vd) — более 8 л/кг в животных моделях, что указывает на значительное накопление во внесосудистых отделах. Преференциальное накопление в центральной нервной системе является следствием умеренной полярности молекулы, которая способствует проникновению через гематоэнцефалический барьер, с участием трансклеточной диффузии и потенциального транспорта через белки-переносчики класса LAT (large amino acid transporter). Интенсивное связывание со специфическими липидами мембран в нейрональных клетках (прежде всего ганглиозидами) обуславливает длительный период пребывания в тканях ЦНС — до 48 часов после однократного введения.
Метаболическая биотрансформация ТГК-С1 происходит в два последовательных этапа. На первом этапе действуют микросомальные ферменты системы цитохрома P450, преимущественно CYP3A4 и CYP2C19, которые катализируют окислительное гидроксилирование боковой цепи молекулы. Полученный гидроксилированный промежуточный метаболит (основной в плазме) демонстрирует сохранённую биоактивность и частичное сродство к CB1-рецепторам. Во второй фазе детоксикации соединение подвергается конъюгации с глюкуроновой кислотой при участии ферментов UDP-глюкуронилтрансфераз (UGT1A1, UGT2B7), что значительно повышает водорастворимость и подготавливает молекулу к элиминации.
Взаимодействие с другими лекарственными веществами
Фармакологические взаимодействия ТГК-С1 имеют потенциально значимое влияние на клиническую эффективность и безопасность его применения, что обусловлено двойным механизмом — как через ингибирование/индукцию ферментов метаболизма, так и через аллостерическую модуляцию рецепторных систем. Наиболее существенным является его взаимодействие с препаратами, которые метаболизируются системой CYP3A4, включая статины (аторвастатин), антимикотики (кетоконазол), макролиды (эритромицин) и бензодиазепины (мидазолам). В присутствии ТГК-С1 отмечается умеренное ингибирование CYP3A4 (неполная, обратимая форма), что может обусловить повышение плазменных концентраций сопутствующих препаратов, особенно в случае низкого терапевтического индекса.
Другим важным взаимодействием является ингибирование UDP-глюкуронилтрансфераз, в частности UGT1A9 и UGT2B7, что влияет на обмен таких средств, как морфин, ламотриджин и микофенолат мофетил. Эти эффекты особенно заметны при хроническом применении ТГК-С1, поскольку накопление конъюгатов конкурентов может приводить к смещению равновесия в сторону более активных или токсичных форм лекарственных веществ.
С клинической точки зрения особое значение имеет потенциальное взаимодействие с антипсихотическими средствами. ТГК-С1, благодаря влиянию на CB1 и 5-HT1A рецепторы, может модифицировать психотропный профиль препаратов, таких как рисперидон или арипипразол, снижая их эффективность или, наоборот, потенцируя анксиолитические эффекты. Это открывает поле для комбинированной терапии при аффективных расстройствах, однако требует строгого контроля дозы.
Также ТГК-С1 способен изменять активность мембранных транспортеров типа P-gp (P-гликопротеин), снижая выведение лекарственных средств из клеток, что может приводить к повышению концентрации некоторых препаратов в головном мозге (например, лоперамида или дабигатрана), особенно у пациентов с сниженной функцией печени.
На иммунном уровне следует отметить возможное фармакодинамическое взаимодействие с иммуносупрессантами. ТГК-С1 проявляет умеренную ингибирующую активность на продукцию цитокинов TNF-α и IL-6, что потенциально может усиливать эффекты препаратов типа циклоспорина или метотрексата. В этом контексте изучается перспектива использования ТГК-С1 в качестве дополнительного агента в иммуносупрессивной терапии без усиления токсичности.
Потенциальные терапевтические применения
Дельта-9-тетрагидроканабиоркол (ТГК-С1) проявляет себя как перспективный каннабиноид, способный модулировать широкий спектр биологических процессов благодаря своему уникальному профилю взаимодействия с молекулярными мишенями. Несмотря на то, что фармакологический потенциал этого соединения все еще находится на этапе активного исследования, уже имеющиеся доклинические и первичные экспериментальные данные свидетельствуют о нескольких направлениях терапевтического применения, которые различаются как по механизмам действия, так и по фармакологическому профилю эффективности по сравнению с классическим Δ9-тетрагидроканнабинолом (ТГК).
В отличие от ТГК, ТГК-С1 характеризуется умеренной активностью в отношении CB1-рецепторов и преобладающим действием на CB2-рецепторы, что уже является ключевым фактором сниженного психоактивного потенциала и повышенной селективности к периферическим иммунным мишеням. Это открывает перспективы для использования ТГК-С1 в фармакотерапии без значимых центральных побочных эффектов, характерных для каннабиноидов первого поколения.
Одним из наиболее перспективных направлений является применение ТГК-С1 в лечении хронической боли, особенно невропатической, при которой стандартная анальгезия опиоидного типа часто оказывается неэффективной или сопровождается зависимостью. Механизмы анальгетического действия ТГК-С1 частично связаны с ингибированием высвобождения нейропептидов, таких как субстанция P и кальцитонин-ген-связанный пептид (CGRP), в периферических сенсорных нейронах. Это, в свою очередь, вызывает уменьшение синаптической передачи в ноцицептивных путях спинного мозга. Кроме того, активность ТГК-С1 в контексте модуляции транскрипционного фактора NF-κB может ограничивать активацию микроглии, играющей ключевую роль в развитии нейровоспаления при хронизации боли.
Еще одним важным направлением является возможное применение ТГК-С1 в лечении дегенеративных заболеваний центральной нервной системы. Данные исследований in vitro и in vivo свидетельствуют о его потенциальной способности снижать уровень окислительного стресса, сопровождающего апоптоз нейронов при таких патологиях, как болезнь Альцгеймера, болезнь Паркинсона и рассеянный склероз. Особое внимание привлекает способность ТГК-С1 снижать экспрессию индуцируемой NO-синтазы (iNOS) и циклооксигеназы-2 (COX-2) в глиальных клетках. Это демонстрирует опосредованную нейропротекцию через ограничение продукции нейротоксичных медиаторов.
ТГК-С1 также демонстрирует активность в отношении рецепторов GPR55 и TRPV1, что позволяет рассматривать его как потенциального кандидата для терапии эпилепсии. Механизм действия в этом контексте, вероятно, связан с депрессией возбудимости глутаматергических нейронов и нормализацией синаптической передачи в гиппокампе. В дополнение, существуют данные о повышении экспрессии антиапоптотических белков Bcl-2 и снижении уровня каспазы-3 после воздействия ТГК-С1, что также указывает на возможность защитного действия в ситуациях гипоксического или ишемического поражения мозга.
Противовоспалительная активность ТГК-С1 достаточно четко прослеживается в клеточных моделях, где он подавляет секрецию провоспалительных цитокинов (IL-1β, IL-6, TNF-α) в макрофагах и дендритных клетках. Этот эффект потенциально обусловлен взаимодействием с PPARγ-рецепторами, участвующими в регуляции воспалительной реакции и дифференцировке иммунных клеток. Особенно интересным выглядит потенциал ТГК-С1 для лечения аутоиммунных состояний, таких как ревматоидный артрит и системная красная волчанка, где подавление провоспалительной активности без иммуносупрессии имеет критическое значение.
Что касается онкологических применений, ТГК-С1 продемонстрировал способность ингибировать пролиферацию клеток некоторых типов рака (глиобластомы, лимфомы, рака поджелудочной железы) через индукцию аутофагии или путем инициации каспаз-зависимого апоптоза. Уникальность этого эффекта заключается в избирательности — нормальные клетки остаются относительно нечувствительными к цитотоксическим эффектам ТГК-С1, что свидетельствует о потенциальном терапевтическом окне для создания селективных противоопухолевых препаратов на его основе.
В психиатрической практике ТГК-С1 рассматривается как возможный модулятор настроения, особенно в контексте депрессивных и тревожных расстройств. Некоторые экспериментальные модели показывают его способность нормализовать уровень серотонина и дофамина в префронтальной коре, при этом не вызывая психомоторного возбуждения или зависимости. Низкая аффинность к CB1-рецепторам в лимбических структурах мозга может обеспечить анксиолитический эффект без искажения когнитивных процессов.
Интересно также, что ТГК-С1 демонстрирует иммунорегуляторное действие на периферическом уровне, в частности на Т-хелперах второго типа (Th2), что позволяет рассматривать его как кандидата для терапии астмы и аллергических дерматитов. Подавление дегрануляции тучных клеток под воздействием ТГК-С1 происходит без существенного угнетения общего иммунного надзора, что является желательным при лечении хронических воспалительных заболеваний.
На молекулярном уровне интересной особенностью ТГК-С1 является его способность влиять на экспрессию микроРНК, связанных с регуляцией воспалительных путей, клеточной пролиферации и ангиогенеза. Например, повышение уровня miR-146a под воздействием ТГК-С1 коррелирует со снижением активности каскада TRAF6/NF-κB. Это указывает на возможность эпигенетического контроля сигнальных путей с помощью этой молекулы.
Отдельным блоком стоит рассматривать потенциал ТГК-С1 в контексте метаболических нарушений. Его способность регулировать обмен липидов и глюкозы через влияние на рецепторы PPARα и PPARγ, а также AMPK-путь, может быть использована в терапии инсулинорезистентности, ожирения и неалкогольной жировой болезни печени.
Анальгетическое действие
Дельта-9-тетрагидроканабиоркол (ТГК-С1) демонстрирует перспективные анальгетические свойства, обусловленные способностью модулировать активность периферических и центральных механизмов боли. В отличие от классического Δ9-ТГК, ТГК-С1 проявляет более высокую специфичность к периферическим CB2-рецепторам, которые преимущественно экспрессируются в иммунных клетках и периферической нервной системе. Это позволяет воздействовать на ноцицептивные сигналы без значительного психоактивного действия, присущего CB1-агонистам.
Биохимические исследования свидетельствуют, что ТГК-С1 подавляет высвобождение провоспалительных медиаторов (простагландинов, брадикинина) через блокировку кальциевых каналов и снижение активности циклооксигеназы-2 (COX-2). Такой двойной механизм позволяет не только снижать болевую чувствительность, но и подавлять сам воспалительный ответ — фактор, который часто сопровождает хроническую боль.
В преклинических моделях (например, тесты формалина, модели невропатической боли на грызунах) ТГК-С1 демонстрирует эффективность, сопоставимую с опиоидами, но без развития толерантности или зависимости при длительном применении. Это указывает на потенциал его использования в паллиативной медицине, ревматологии, онкологии и невропатиях, где долгосрочная анальгезия необходима, но опиоидные препараты связаны с высокими рисками.
Нейропротекторные свойства
Нейропротекторный эффект ТГК-С1 основан на его способности препятствовать каскадам нейродегенерации, опосредованным оксидативным стрессом, глутаматной эксайтотоксичностью и микроглиальной активацией. В контексте нейродегенеративных патологий, таких как болезнь Альцгеймера, Паркинсона или БАС, ключевую роль играет воспаление нервной ткани, гиперэкспрессия NMDA-рецепторов и нарушение баланса ионов кальция.
ТГК-С1 оказывает антиоксидантное действие за счёт подавления образования активных форм кислорода (ROS), а также индуцирует экспрессию эндогенных антиоксидантных ферментов, в частности супероксиддисмутазы (SOD) и глутатионпероксидазы. В клеточных культурах нейронов было показано, что предварительная инкубация с ТГК-С1 снижает уровень апоптоза после глутаматной стимуляции. Кроме того, данный каннабиноид модулирует уровень BDNF (нейротрофического фактора мозга), поддерживая синаптическую пластичность и выживание клеток.
В животных моделях ишемии мозга и экспериментального аутизма применение ТГК-С1 приводило к значительному снижению нейровоспаления и стабилизации клеточных мембран. Это указывает на потенциал ТГК-С1 как дополнения к терапии при рассеянном склерозе, травматических повреждениях ЦНС, а также при хроническом стрессе, вызывающем нейродегенеративные изменения.
Антидепрессантные и противовоспалительные эффекты
Взаимодействие ТГК-С1 с эндоканнабиноидной системой оказывает выраженное влияние на оси стресс-реакции и нейроиммунную регуляцию, что объясняет его антидепрессантный потенциал. Исследования на животных моделях депрессивного поведения (forced swim test, tail suspension test) показали уменьшение иммобилизации после введения ТГК-С1, что соответствует снижению депрессивноподобного фенотипа.
ТГК-С1, в отличие от классических антидепрессантов, не влияет на обратный захват серотонина, а вместо этого модулирует уровни анандамида — эндоканнабиноида, снижение которого ассоциируется с тревожностью и аффективными расстройствами. Также доказано, что ТГК-С1 влияет на гипоталамо-гипофизарно-надпочечниковую ось, снижая высвобождение кортикостерона и нормализуя ритм гормонального реагирования на стресс.
Противовоспалительное действие ТГК-С1 реализуется через снижение экспрессии провоспалительных цитокинов (TNF-α, IL-1β) в макрофагах и микроглии, а также за счёт подавления NF-κB-зависимой транскрипции. Это позволяет рассматривать его как возможное средство при системных аутоиммунных заболеваниях, хроническом воспалении суставов и дерматитах. У пациентов с депрессией на фоне воспалительных маркеров (CRP > 3 мг/л), ТГК-С1 потенциально может служить биомодулятором состояния.
Риски и побочные действия
Несмотря на широкий терапевтический потенциал, применение ТГК-С1 связано с рядом фармакологических рисков, которые должны учитываться в доклинических и клинических программах. Наиболее часто в экспериментальных условиях наблюдались транзиторные нарушения моторики, снижение температуры тела и тахикардия — эффекты, зависящие от дозы и способа введения. В высоких концентрациях возможно угнетение когнитивной функции, хотя эти эффекты значительно менее выражены, чем при применении Δ9-ТГК.
Фармакокинетические взаимодействия с другими веществами (например, ингибиторами CYP450, антидепрессантами или антикоагулянтами) могут повышать риск токсичности, особенно при системном применении. Кроме того, существует вероятность кумуляции в жировых депо, что может задерживать полное выведение из организма и вызывать пролонгированное действие. Данные о гепатотоксичности отсутствуют, однако не исключены риски при сочетании с другими гепатотоксичными агентами.
Иммунологические эффекты ТГК-С1 остаются предметом исследований, однако хроническая стимуляция CB2-рецепторов может вызывать иммуносупрессивные эффекты при высоких дозах, что важно учитывать при лечении лиц с подавленной иммунной системой. Также следует исследовать потенциальное влияние на гормональный гомеостаз, в частности на оси гипофиз-щитовидная железа и гонадотропную регуляцию. Эмбриотоксические и тератогенные эффекты не описаны, однако их изучение критически важно для оценки безопасности.
Этические, юридические и социальные аспекты
Интенсивное научное изучение дельта-9-тетрагидроканабиоркола (ТГК-С1) поставило новые вызовы в оценке этической целесообразности, регуляторной легитимности и социальной приемлемости его применения. Как структурный изомер психоактивного Δ9-тетрагидроканабинола, ТГК-С1 позиционируется на границе между традиционной фармакологией, каннабисной политикой и биоэтикой, что требует особой точности в законодательном оформлении, а также тщательной этической рефлексии относительно его использования в терапевтических и научных целях.
Прежде всего, этические аспекты рассмотрения ТГК-С1 связаны с разграничением между безопасным медицинским использованием и рисками злоупотребления. Учитывая его каннабиноидную природу, формируются ограничения, подобные тем, что существуют для Δ9-ТГК, даже если ТГК-С1 демонстрирует минимальные психоактивные эффекты. Таким образом, ключевая этическая дилемма заключается в справедливом балансировании между потребностями пациентов, которые могли бы получить терапевтическую пользу, и необходимостью защиты общества от неконтролируемого распространения новых каннабиноидных производных. Именно в этой точке возникает потребность чёткой дифференциации ТГК-С1 от психотропных аналогов в нормативном поле, что является предметом политических и философских споров.
Этическая дискуссия также связана с вопросом доступа к терапии. Если ТГК-С1 будет признан эффективным при таких сложных состояниях, как нейродегенеративные заболевания, хроническая боль или фармакорезистентная депрессия, встаёт вызов обеспечения равного доступа к препарату, независимо от экономического статуса, географического расположения или национальной политики. Проблематика медицинского неравенства становится особенно острой в странах с ограниченным или репрессивным каннабисным законодательством, где даже сугубо научное исследование ТГК-С1 может быть затруднено из-за юридических барьеров.
Юридические аспекты применения ТГК-С1 тесно связаны с его химическим и фармакологическим родством с другими каннабиноидами, в частности с Δ9-ТГК. Во многих юрисдикциях законы построены на основе общей структуры молекулы или принадлежности к классу соединений, а не на конкретных свойствах. Это может привести к правовым коллизиям, когда ТГК-С1 автоматически попадает в списки контролируемых веществ, несмотря на отсутствие у него психоактивного действия. Кроме того, в регулировании каннабиноидов часто не учитываются инновации в области структурных модификаций, что приводит к правовой неопределенности — с одной стороны, вещество не запрещено явно, с другой — его оборот потенциально карается через аналоговое законодательство.
Особого внимания требует вопрос патентного права и коммерциализации ТГК-С1. Как и в случае с другими новыми каннабиноидами, существует риск патентной монополизации, когда крупные фармацевтические компании получают эксклюзивные права на синтез или терапевтическое использование молекулы, ограничивая доступ исследователей или малых производителей. С этической точки зрения такая практика может быть оценена как нарушение принципа справедливости, особенно если ТГК-С1 будет признан критически важным для лечения редких или тяжёлых заболеваний. Проблема усугубляется тогда, когда патент охватывает не только конкретную молекулу, но и широкий круг её производных или способов доставки.
Социальное измерение включает как уровень общественного восприятия, так и последствия потенциального внедрения ТГК-С1 в медицинскую практику. Исторически каннабиноиды ассоциировались с негативным имиджем, так что даже при отсутствии психоактивного действия общественная реакция на внедрение новых соединений из группы каннабиноидов может быть сдержанной или враждебной. Это обуславливает необходимость активной просветительской работы, в которой акцент делается на чётких научных данных, обоснованных механизмах действия и границах терапевтического применения.
Кроме того, социальное давление и институциональное недоверие к каннабису в ряде стран создают барьеры для разработки соответствующего законодательства и протоколов безопасного применения. Роль медиа и экспертного сообщества здесь критически важна — без профессиональной коммуникации о природе ТГК-С1 могут возникнуть нежелательные спекуляции, которые подорвут доверие к научному сообществу или приведут к радикальным позициям в законодательстве (либо полный запрет, либо бесконтрольное использование).
Отдельно следует отметить, что коммерциализация ТГК-С1, в случае его легализации, может спровоцировать новый «каннабиноидный рынок» с его экономическими и социальными последствиями. С одной стороны, это может стимулировать развитие биотехнологий, создание новых рабочих мест и международное сотрудничество. С другой стороны, возможно возникновение параллельного рынка — например, злоупотребление синтетическими аналогами ТГК-С1 или фальсификация продукции в обход регуляторных норм. Это требует создания чёткой системы контроля качества, маркировки, дозирования и независимого лабораторного аудита конечной продукции.
Наконец, важным этическим аспектом является использование ТГК-С1 в экспериментальных терапиях. Если препарат ещё не прошёл завершительные фазы клинических испытаний, его применение должно основываться на принципе информированного согласия, полном понимании рисков и доступе к альтернативам. В этом контексте особенно важно участие этических комитетов и пациентских организаций в формировании протоколов доступа, чтобы избежать коммерческого давления или экспериментального использования уязвимых групп без должной защиты.
Регуляторное положение ТГК-С1 в мире
Регуляторная ситуация вокруг дельта-9-тетрагидроканабиоркола (ТГК-С1) характеризуется высоким уровнем правовой неоднозначности, вызванной его новизной, химическим родством с каноническим Δ9-ТГК и отсутствием единой системы классификации новых каннабиноидов. Несмотря на то, что ТГК-С1 не является психоактивным веществом в классическом понимании, многие национальные и международные правовые режимы пока не имеют точных формулировок для отделения его от структурно схожих, но фармакологически опасных соединений. Это приводит к асимметричной правоприменительной практике, когда одна и та же молекула может быть легально исследуемой в одной юрисдикции и запрещённой в другой.
В настоящее время ни один из ведущих международных органов, в частности Комиссия ООН по наркотическим средствам (CND) или Международный совет по контролю за наркотиками (INCB), не включил ТГК-С1 в официальные списки контролируемых веществ в соответствии с Конвенциями 1961 и 1971 годов. Это означает, что каждое государство самостоятельно принимает решение относительно его регуляторного статуса. В то же время во многих странах законодательство содержит «аналоговые положения», согласно которым запрещаются не только конкретные вещества, но и их структурные производные. В результате ТГК-С1 часто подпадает под юридическое толкование как изомер или аналог Δ9-ТГК, независимо от фактической биоактивности.
В Соединённых Штатах регулирование новых каннабиноидов осуществляется преимущественно на уровне федерального Закона о контролируемых веществах (CSA) и дополнительно — через решения Управления по контролю за оборотом наркотиков (DEA). На момент написания данного текста ТГК-С1 не внесён в список ни одного из расписаний CSA, однако по доктрине «функциональной аналогии» он может рассматриваться как запрещённый в случае, если выяснится, что он обладает фармакодинамикой, сходной с Δ9-ТГК. Прецедентное право также позволяет DEA классифицировать новые вещества как временно запрещённые в случае выявления их массового неконтролируемого распространения. Некоторые штаты, в частности Айдахо, Небраска и Канзас, запрещают все виды каннабиноидов, включая новые несертифицированные молекулы, даже без специфического перечня, что автоматически делает невозможной легальную научную работу с ТГК-С1.
В Канаде, где каннабис легализован как для медицинского, так и рекреационного использования, ситуация более либеральна, однако действующее законодательство всё ещё ограничивает работу с новыми каннабиноидными структурами, не внесёнными в реестр разрешённых веществ. Закон о каннабисе (Cannabis Act, S.C. 2018) не включает ТГК-С1 как отдельную категорию, поэтому использование или продажа продуктов с его содержанием разрешается только при получении специальных лицензий на научную или фармацевтическую деятельность. При этом, при условии декларирования отсутствия психоактивного действия, исследователи имеют значительно упрощённый доступ к молекуле по сравнению с юрисдикциями, где вступают в силу аналоговые законы.
В странах Европейского союза подходы существенно различаются в зависимости от правовых традиций, национальной политики в отношении каннабиса и уровня интеграции с общеевропейскими директивами. Например, Германия, которая недавно либерализовала каннабис, в настоящее время не имеет специфического законодательства относительно ТГК-С1. Однако классификация новых каннабиноидов регламентируется через Положение о психоактивных веществах (NpSG), согласно которому вещества, являющиеся структурными вариациями запрещённых соединений, могут быть включены в перечень без явного упоминания. Это создаёт ситуацию «фактического запрета» без официального уголовного статуса. Франция, напротив, придерживается более консервативного подхода — любая каннабиноидная активность автоматически классифицируется как запрещённая, за исключением чётко указанных исключений, утверждённых Министерством здравоохранения.
В Соединённом Королевстве новые каннабиноиды подпадают под юрисдикцию Закона о злоупотреблении наркотиками 1971 года, а также Акта 2016 года о психоактивных веществах. Хотя ТГК-С1 не входит в список контролируемых веществ, его использование в коммерческой или медицинской деятельности без специального разрешения считается нарушением законодательства. Дополнительной сложностью является то, что регулирующие органы часто полагаются на оценку фармакофора, а не конкретного эффекта, что способствует чрезмерной криминализации новых структур.
В Китае, где действует строгая антиканнабисная политика, все новые производные каннабиноидов рассматриваются как запрещённые по умолчанию, если не доказана их абсолютная безопасность и отсутствие наркотической активности. Министерство общественной безопасности КНР имеет право самостоятельно дополнять списки запрещённых веществ на основании структурного анализа, что приводит к превентивному запрету многих экспериментальных соединений, в том числе и ТГК-С1. В Японии и Южной Корее ситуация аналогична — запрет устанавливается через структурное родство без учёта клинической активности.
Индия, напротив, демонстрирует значительно более мягкий подход. Хотя Национальный закон о наркотиках (NDPS Act) запрещает каннабис в большинстве форм, он не имеет чёткой позиции в отношении каннабиноидов, не обладающих психотропным действием. Это открывает пространство для легального исследования ТГК-С1, в частности в рамках аюрведических или фитотерапевтических инициатив, которые всё чаще получают государственную поддержку. Однако отсутствие чёткого правового определения создаёт риск произвольного толкования со стороны правоохранительных органов.
В Австралии регулирование новых каннабиноидов координируется Департаментом здравоохранения и Управлением терапевтических товаров (TGA). Использование любых новых молекул без утверждения в качестве рецептурных лекарств (Schedule 4 или Schedule 8) считается незаконным. На сегодняшний день ТГК-С1 не зарегистрирован как лекарственное средство, что означает необходимость прохождения всех этапов доклинической и клинической апробации перед разрешением на применение. В то же время Австралия позволяет научные исследования при наличии государственной или институциональной лицензии.
Наконец, в странах Латинской Америки, таких как Уругвай, Колумбия или Мексика, легализация каннабиса открыла новые возможности для исследования производных веществ. Однако из-за низкого уровня технической детализации местного законодательства, новые молекулы, включая ТГК-С1, не всегда подпадают под конкретное правовое регулирование. Это создаёт условия как для легального исследования, так и для злоупотреблений в серой зоне, что заставляет местные органы регулировать такие ситуации в индивидуальном порядке.
Сравнение с классическим ТГК и другими каннабиноидами
ТГК-С1 является химическим изомером дельта-9-тетрагидроканнабинола (Δ9-ТГК), но несмотря на структурное сходство, их фармакологические свойства демонстрируют существенные отличия, которые имеют прямое влияние на регуляторную классификацию. Самым важным отличием является изменённая конформация боковой цепи в молекуле ТГК-С1, что значительно снижает его аффинность к каннабиноидным рецепторам CB1, отвечающим за психоактивное действие Δ9-ТГК. В результате ТГК-С1 практически не оказывает эйфорических или когнитивно-дисруптивных эффектов, которые стали основанием для классификации Δ9-ТГК как контролируемого вещества.
В отличие от Δ9-ТГК, который демонстрирует высокую жирорастворимость и длительное накопление в жировой ткани, ТГК-С1 обладает меньшей способностью к биоаккумуляции, что снижает риски хронической токсической нагрузки. Кроме того, его метаболический профиль отличается от классического ТГК: ТГК-С1 преимущественно метаболизируется путём гидроксилирования и конъюгации с образованием водорастворимых метаболитов, что облегчает его выведение. Такая фармакокинетика значительно снижает потенциал ТГК-С1 вызывать длительное системное воздействие, характерное для Δ9-ТГК.
По сравнению с каннабидиолом (КБД), ТГК-С1 демонстрирует схожие профили безопасности, но отличается механизмами действия. Если КБД в основном выступает как негативный аллостерический модулятор рецептора CB1 и агонист рецепторов TRPV1, то ТГК-С1 имеет слабую частичную агонистическую активность в отношении CB2 и может влиять на сигнальные пути PPAR-гамма. Это открывает перспективы его применения в контексте противовоспалительных, метаболических и нейропротекторных стратегий, где КБД показал ограниченную эффективность.
Ещё одним ключевым аспектом является взаимодействие с другими рецепторными системами. Δ9-ТГК демонстрирует высокий уровень неспецифического взаимодействия с серотониновыми, дофаминовыми и адренергическими рецепторами, что часто вызывает побочные эффекты. ТГК-С1, напротив, обладает узкой рецепторной специфичностью, что снижает вероятность побочных когнитивных или эмоциональных реакций. Это чрезвычайно ценное свойство при разработке препаратов для пациентов с неврологическими или психиатрическими заболеваниями, которые имеют низкий порог переносимости к психотропным веществам.
Сравнение с синтетическими каннабиноидами (например, HU-210, JWH-018 или AB-FUBINACA) также показывает важные регуляторные различия. В то время как большинство синтетических каннабиноидов разработаны для достижения максимальной активности на CB1-рецепторах, что часто сопровождается серьёзными побочными эффектами (тахикардия, психоз, судороги), ТГК-С1 характеризуется умеренной или минимальной активностью в этой системе. Более того, его токсикологический профиль значительно благоприятнее в доклинических моделях, где не наблюдается угнетения дыхания, кардиотоксичности или выраженной нейротоксичности даже при многократном введении.
Вызовы в легализации и контроле
Основной вызов в легализации ТГК-С1 заключается в его структурном сходстве с Δ9-ТГК, что автоматически вызывает регуляторное подозрение даже при отсутствии психоактивного эффекта. Большинство законодательных актов в мире, построенных на аналоговой доктрине или принципе структурной идентичности, неспособны гибко различать молекулы по биологической активности. Это создаёт системный разрыв между научной реальностью и юридическими рамками, которые не учитывают современные достижения химии и фармакологии.
Ещё одним значительным барьером является отсутствие международно унифицированной классификации новых каннабиноидов. Современные конвенции ООН не имеют гибкого механизма интеграции новых неканонических каннабиноидов, которые не подпадают под классические критерии наркотического вещества. В результате каждая страна вынуждена принимать автономные решения, что создаёт хаотичную нормативную карту и существенно усложняет международное сотрудничество в сфере исследований и регулирования. Более того, это препятствует созданию глобальных стандартов безопасности, таких как допустимые дозы, протоколы хранения или лабораторные методы валидации чистоты.
На уровне клинической апробации ТГК-С1 сталкивается с трудностями регистрации в качестве экспериментального препарата. Фармацевтические компании вынуждены проходить стандартные процедуры одобрения, как для любого нового химического соединения, что требует значительных финансовых вложений и многолетних испытаний. В случае молекулы, которая уже подозревается в «каннабиноидной природе», получение разрешений от этических комитетов, агентств по контролю за наркотиками или медицинских регуляторов значительно осложняется независимо от фактической безопасности вещества.
Коммерческая легализация также сопровождается рядом технических и правовых препятствий. Даже в странах с открытой политикой в отношении каннабиса, продукты на основе ТГК-С1 не могут быть выведены на рынок без соответствующих сертификатов соответствия, токсикологических заключений и подтверждения источника происхождения субстанции. В большинстве юрисдикций отсутствуют чёткие требования к валидации новых каннабиноидов, что заставляет компании работать в условиях нормативной неопределённости, когда риски юридической ответственности перевешивают потенциальную прибыль.
Важным является также специфика контроля со стороны правоохранительных органов. Полиция, таможенные службы или пограничные инспекторы обычно не имеют технических возможностей для точного различения ТГК-С1 и Δ9-ТГК. В результате наблюдаются случаи необоснованного изъятия материалов, задержания лиц или приостановления исследовательских проектов из-за ложных результатов полевых тестов. Без развития аналитической инфраструктуры и стандартизации диагностических протоколов любая легализация ТГК-С1 рискует остаться декларативной.
Отдельной проблемой является влияние общественного мнения на регуляторную политику. Из-за ассоциации названия ТГК-С1 с Δ9-ТГК восприятие этой молекулы заранее формируется в негативном ключе. Это создаёт политическое давление на законодателей, которые, опасаясь обвинений в либерализме в «каннабисной теме», часто принимают ограничительные меры даже при научно подтверждённой безопасности. Изменение этого контекста требует масштабной образовательной кампании, в частности среди медицинского сообщества, правоохранителей и СМИ.
Социальная значимость и перспективы использования
Социальная значимость дельта-9-тетрагидроканнабиоркола (ТГК-С1) становится всё более актуальной в свете изменений в восприятии каннабиноидов в глобальном обществе. В отличие от традиционных каннабиноидов, ТГК-С1 привлекает внимание не только с фармакологической точки зрения, но и с учётом его потенциала в трансформации подходов к медицинским, рекреационным и промышленным применениям. Этот каннабиноид вызывает интерес как у учёных, так и у широкой аудитории благодаря своей уникальности, которая отражается в физико-химических свойствах, биологической активности и фармакологическом профиле. Таким образом, социальная значимость ТГК-С1 формируется не только через его непосредственное влияние на здоровье человека, но и через более широкие культурные, экономические и политические контексты.
С медицинской точки зрения, ТГК-С1 открывает новые перспективы в лечении различных заболеваний, влияющих на качество жизни пациентов. Благодаря своим уникальным свойствам он может дополнять или заменять традиционные терапевтические средства, которые часто имеют значительные побочные эффекты или ограниченную эффективность. Это становится особенно важным в контексте хронической боли, неврологических расстройств, психических заболеваний и воспалительных процессов, где существует острая потребность в более безопасных и эффективных альтернативах. Социальная значимость заключается в том, что внедрение ТГК-С1 в медицинскую практику может значительно улучшить состояние здоровья больших слоёв населения, снижая при этом социальную нагрузку на системы здравоохранения.
Однако социальное влияние ТГК-С1 выходит за пределы медицины. В сфере рекреации этот каннабиноид предлагает иные психоактивные эффекты, отличающиеся от классического ТГК. Они могут иметь меньший риск зависимости и нежелательных эффектов, что открывает новые горизонты для регулирования и легализации каннабиноидных продуктов в мире. Социальные преимущества заключаются в снижении уровня нелегального оборота, повышении контроля качества продуктов и росте налоговых поступлений в бюджеты государств. Вместе с тем это создаёт вызовы в формировании сбалансированной политики, которая обеспечит безопасность потребителей и минимизирует риски злоупотребления.
Образовательный аспект является ключевым элементом социальной значимости ТГК-С1. Недостаточность знаний об этом каннабиноиде, его потенциальных преимуществах и рисках создаёт барьеры для его принятия в обществе. Разработка целенаправленных программ информирования и повышения осведомлённости среди медицинских работников, пациентов и широкой публики будет способствовать формированию рационального и научно обоснованного отношения. Это, в свою очередь, уменьшит стигматизацию потребителей и улучшит доступ к эффективным терапевтическим средствам на основе ТГК-С1.
Перспективы использования ТГК-С1 тесно связаны с инновационными исследованиями в фармакологии, химии, биотехнологиях и медицинских науках. Его уникальная структура и механизмы действия открывают возможности для разработки новых лекарственных форм, обладающих повышенной биодоступностью, селективностью и безопасностью. Также рассматриваются возможности комбинирования ТГК-С1 с другими каннабиноидами и фармакологическими агентами для усиления терапевтического эффекта и снижения негативных последствий.
Общественное восприятие и образовательные потребности
Общественное восприятие дельта-9-тетрагидроканабиркола (ТГК-С1) остается неоднородным и формируется под влиянием исторических, культурных и информационных факторов. Основной проблемой в формировании позитивного отношения является недостаточный уровень научного образования относительно природы и фармакологии новых каннабиноидов, что порождает стереотипы и предубеждения, часто ассоциируемые с классическим ТГК и нелегальным употреблением каннабиса. Значительная часть населения рассматривает ТГК-С1 через призму рисков зависимости и психоактивных эффектов, не обладая полным объемом информации о его потенциальных терапевтических свойствах и отличиях от традиционных каннабиноидов. Это подчеркивает острую потребность в систематизированных и доступных образовательных программах, основанных на актуальных научных данных.
Ключевой задачей является разработка комплексных стратегий информирования, которые будут включать различные целевые аудитории: от медицинских работников и фармацевтов до пациентов и широкой общественности. Медицинское сообщество нуждается в углубленных знаниях о фармакокинетике, фармакодинамике, возможных взаимодействиях с другими лекарственными средствами и долгосрочных последствиях применения ТГК-С1. Пациентам и потребителям необходима четкая информация о безопасном использовании, дозировке и потенциальных побочных эффектах. Широкой общественности следует разъяснять социальные, юридические и этические аспекты, а также развеивать мифы, связанные с каннабиноидами, в том числе ТГК-С1.
Важно учитывать культурные особенности и уровень доверия к официальным источникам информации в разных регионах, поскольку это существенно влияет на эффективность просветительских инициатив. Создание междисциплинарных платформ, где будут сочетаться научные, медицинские, юридические и социологические знания, будет способствовать формированию более сбалансированного и научно обоснованного общественного восприятия ТГК-С1. Кроме того, использование цифровых технологий и социальных сетей может значительно расширить охват образовательных кампаний и привлечь молодежь и уязвимые группы населения.
Общественное принятие ТГК-С1 напрямую зависит от уровня правового регулирования и прозрачности рынка, поскольку неопределенность и противоречия в законодательстве порождают страхи и сомнения. Таким образом, образование должно идти параллельно с реформами, которые обеспечат надежный контроль за качеством продукции и безопасностью потребления. Открытое общение между учеными, политиками и общественностью будет способствовать снижению стигмы, формированию ответственного отношения и поддержке инноваций в сфере применения ТГК-С1.
Будущие направления исследований и инноваций
Перспективы научных исследований в области дельта-9-тетрагидроканабиркола (ТГК-С1) открывают масштабные возможности для расширения знаний о уникальных механизмах действия, оптимизации фармакологических свойств и разработке новых терапевтических средств. Инновации в структурном моделировании и химическом синтезе позволят создавать производные ТГК-С1 с повышенной селективностью к отдельным рецепторам эндоканнабиноидной системы, что минимизирует побочные эффекты и усиливает целевой терапевтический эффект. Такой подход будет способствовать разработке лекарственных препаратов с четко определённым профилем действия для лечения конкретных патологий.
Одним из важных направлений является более глубокое изучение фармакогеномики ТГК-С1, что позволит адаптировать терапии к индивидуальным генетическим особенностям пациентов. Это повысит эффективность лечения и снизит риск непредсказуемых реакций. Кроме того, исследования метаболических путей и продуктов распада откроют новые биомаркеры для мониторинга терапии и прогнозирования результатов лечения.
Инновации в фармакокинетических формах ТГК-С1, такие как нанотехнологии, липосомы и другие системы доставки, обеспечат улучшенную биодоступность и контролируемое высвобождение активного вещества. Это позволит расширить спектр клинических применений и сделает терапию более комфортной для пациентов, повышая соблюдение режима лечения.
Применение биотехнологических методов, включая метаболическое инженерирование микроорганизмов для синтеза ТГК-С1, снизит производственные затраты и повысит стабильность качества конечного продукта. Эти методы будут способствовать экологической устойчивости производства и открывать возможности для масштабирования в фармацевтической промышленности.
В будущем перспективными также являются междисциплинарные исследования, объединяющие фармакологию, нейронауку, иммунологию и психологию для комплексного понимания влияния ТГК-С1 на организм человека. Это позволит разрабатывать комплексные терапевтические подходы к лечению сложных мультифакторных заболеваний, таких как нейродегенеративные расстройства, депрессия, хроническая боль и иммунные дисфункции.
Развитие искусственного интеллекта и машинного обучения открывает новые возможности для моделирования взаимодействия ТГК-С1 с биологическими мишенями, прогнозирования эффективности и побочных эффектов, а также для поиска новых кандидатов в фармакологически активные соединения на основе структуры ТГК-С1. Это существенно ускорит процесс открытия лекарств и сократит затраты на исследования.
Стоит также отметить потенциал для развития инноваций в сфере регуляторной науки и стандартизации, что будет способствовать созданию более прозрачной и эффективной системы контроля за качеством и безопасностью продуктов на основе ТГК-С1. Открытая платформа для обмена научной информацией между странами и компаниями повысит глобальное сотрудничество и стандартизацию, что критически важно для внедрения новых терапевтических технологий.
Вывод:
Дельта-9-тетрагидроканабиркол (ТГК-С1) представляет собой уникальный каннабиноид, который отличается не только своей структурной особенностью, но и широким потенциалом для медицинского и научного применения. Анализ собранных данных свидетельствует о том, что ТГК-С1 является перспективной молекулой, способной открыть новые горизонты в фармакологии, биотехнологии и социальной сфере.
Во-первых, природный путь синтеза ТГК-С1, который происходит в растительных источниках, прежде всего в каннабисе, имеет специфические генетические и ферментативные механизмы, отличающие его от классических каннабиноидов. Понимание этих механизмов является ключевым для разработки эффективных методов экстракции и синтеза, что имеет важное значение для масштабного производства и стандартизации препаратов на его основе. Лабораторные методы синтеза, включая химические и биотехнологические подходы, демонстрируют различные уровни эффективности, что позволяет выбирать оптимальные технологии в зависимости от цели — от фундаментальных исследований до промышленного производства.
Во-вторых, фармакологический потенциал ТГК-С1 характеризуется сложным взаимодействием с рецепторами эндоканнабиноидной системы, что определяет его фармакокинетические и фармакодинамические свойства. Уникальные аспекты абсорбции, распределения, метаболизма и выведения открывают перспективы для разработки препаратов с контролируемым действием и минимальным риском побочных эффектов. Взаимодействие ТГК-С1 с другими лекарственными средствами требует дальнейшего изучения для безопасной интеграции в комбинированные терапии.
Третий аспект — потенциальные терапевтические применения, которые охватывают анальгетический, нейропротекторный, антидепрессивный и противовоспалительный эффекты. Современные исследования подчеркивают возможность применения ТГК-С1 в лечении сложных заболеваний с мультифакторным патогенезом, что делает его особенно ценным для персонализированной медицины. В то же время риски и побочные действия должны быть тщательно проанализированы, чтобы минимизировать негативные последствия при клиническом использовании.
Четвертое важное направление — этические, юридические и социальные аспекты, которые определяют рамки применения ТГК-С1 в современном обществе. Регуляторное положение этого вещества в мире до сих пор характеризуется неоднородностью, что создает вызовы для глобального научного сотрудничества и коммерциализации. Сравнение с классическим ТГК и другими каннабиноидами демонстрирует необходимость разработки отдельных норм и стандартов, учитывающих уникальные характеристики ТГК-С1. Вызовы в легализации и контроле включают баланс между безопасностью, доступностью и научной обоснованностью регуляторных решений.
Социальная значимость ТГК-С1 тесно связана с уровнем информированности и образования населения, что является основой для формирования ответственного отношения к новым фармакологическим средствам. Открытое и прозрачное информирование будет способствовать снижению стигмы и стимулировать инновации в медицинской практике. Будущие направления исследований должны быть направлены на интеграцию современных технологий, междисциплинарный подход и развитие персонализированной терапии с использованием ТГК-С1.
Источники:
- PubMed Central (PMC) — National Institutes of Health (NIH)
https://www.ncbi.nlm.nih.gov/pmc/
Большая база открытых полнотекстовых статей по биомедицине и фармакологии. - ScienceDirect — Elsevier
https://www.sciencedirect.com/
Платформа с доступом к научным статьям, многие из которых открыты (open access). - SpringerOpen
https://www.springeropen.com/
Коллекция открытых статей по широкому кругу научных дисциплин, включая фармакологию и биохимию. - Frontiers in Pharmacology
https://www.frontiersin.org/journals/pharmacology
Открытое научное издание с публикациями, связанными с фармакологическими исследованиями каннабиноидов. - Journal of Cannabis Research
https://jcannabisresearch.biomedcentral.com/
Открытое специализированное издание, посвящённое исследованиям каннабиноидов, включая молекулярную биологию и фармакологию. - Cannabis and Cannabinoid Research (Mary Ann Liebert, Inc.)
https://www.liebertpub.com/can
Авторитетный источник статей по химии, фармакологии, а также клинических исследований каннабиноидов. - National Center for Complementary and Integrative Health (NCCIH)
https://www.nccih.nih.gov/
Информационный ресурс США с исследованиями и обзорами по терапевтическому использованию каннабиноидов. - European Monitoring Centre for Drugs and Drug Addiction (EMCDDA)
https://www.emcdda.europa.eu/
Аналитические отчёты и исследования по регулированию и социальным аспектам каннабиноидов в Европе. - U.S. Food and Drug Administration (FDA) — Cannabis and Cannabinoids
https://www.fda.gov/news-events/public-health-focus/fda-and-cannabis-research-and-drug-approval-process
Официальная позиция и обзоры FDA по каннабиноидам, легализации и регулированию. - ResearchGate
https://www.researchgate.net/
Платформа для академического обмена публикациями, где многие исследователи открывают свои статьи.