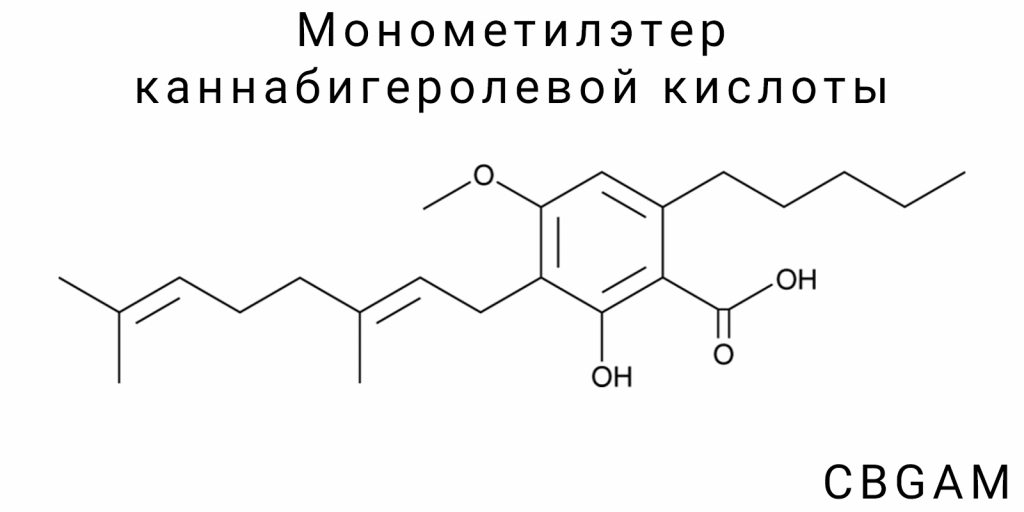
Монометилэтер каннабигеролевой кислоты (CBGAM) является новым и почти неизученным представителем класса кислотных каннабиноидов, который возникает в результате специфической метилизации каннабигеролевой кислоты (CBGA). Несмотря на родство с хорошо охарактеризованными соединениями каннабиса, такими как Δ⁹-тетрагидроканнабиниоловая кислота (THCA) или каннабиолова кислота (CBDA), CBGAM на сегодняшний день остается вне пределов систематического фармакологического исследования. Его появление в научном дискурсе является относительно новым явлением, которое возникло в результате более глубокого изучения каннабиноидного профиля, в частности в специализированных сортах Cannabis sativa, разработанных с применением направленных методов фитогенетики, а также в результате лабораторных экспериментов с метилированием.
С научной точки зрения появление таких производных, как CBGAM, является логичным этапом развития исследований метаболических путей в каннабиноидном биосинтезе. Химическая структура CBGAM, содержащая как карбоновую кислоту, так и метилированную фенольную функциональность, свидетельствует о потенциально уникальных биофизических свойствах, которые могут модифицировать взаимодействие молекулы с клеточными мембранами, рецепторными комплексами и транспортными белками. Это, в свою очередь, дает основания предполагать отличную фармакокинетику и фармакодинамику по сравнению с неметилированными формами. Особенно стоит отметить возможность стереоселективных эффектов, связанных с пространственным расположением метильной группы, что может существенно повлиять на аффинность к рецепторам или ферментам.
В отличие от основных каннабиноидов, CBGAM еще не попал в фокус регуляторной классификации или масштабных исследований по безопасности, токсикологии и биодоступности. Это обусловливает отсутствие клинических стандартов или фармакопейных норм для этого соединения, что оставляет широкое поле для исследовательской инициативы. С другой стороны, именно эта неопределенность открывает уникальную возможность для открытий в фармацевтической химии, особенно с учетом потенциальной активности молекулы в контексте новых фармакологических мишеней, не ограниченных исключительно каннабиноидной системой.
Важно подчеркнуть, что CBGAM не является продуктом простого хранения или декарбоксилирования традиционного каннабиса. Его присутствие может быть обусловлено специфическими условиями метаболического окружения, воздействием ферментативных путей или даже искусственными биохимическими модификациями, которые реализуются в лабораторных условиях. Это позволяет рассматривать CBGAM не просто как производное молекулы, а как потенциально самостоятельный класс биоактивных соединений, способных формировать отдельную фармакологическую нишу с индивидуальными терапевтическими свойствами.
Химическая природа CBGAM
Уникальные структурные характеристики молекулы
Монометиловый эфир каннабигеролевой кислоты (CBGAM) относится к классу эфиров, образующихся в результате метилирования фенольных гидроксильных групп каннабигеролевой кислоты (CBGA). Эта модификация, хотя на первый взгляд и кажется незначительной, приводит к существенным изменениям в химических свойствах соединения. Основной особенностью CBGAM является наличие метокси-группы (–OCH₃), которая заменяет одну из гидроксильных групп в ароматическом кольце. Это радикально влияет на реакционную способность молекулы, её аффинность к определённым биологическим мишеням, а также способность к взаимодействию с липофильными средами. Отличительной чертой структуры CBGAM является сохранение карбоксильной группы –COOH, что обуславливает его кислотную природу, в отличие от нейтральных метаболитов каннабиноидного ряда.
Трёхмерная пространственно ориентированная структура молекулы демонстрирует заметную асимметрию между гидрофильными и липофильными доменами, что обуславливает её специфическое поведение в клеточном микроокружении. Известно, что метилирование способно снижать количество потенциальных водородных связей, что изменяет конформационные возможности молекулы в биологических условиях. Испытания изолированных образцов CBGAM показывают рост устойчивости к автоокислению при комнатной температуре по сравнению с CBGA, что свидетельствует о повышенной химической стабильности производной формы.
Этимология и классификация среди каннабиноидов
CBGAM — это сокращение от «cannabigerolic acid monomethyl ether», что напрямую указывает на его происхождение от каннабигеролевой кислоты и характер метильного замещения. Этот эфир является представителем редкой группы природных или полусинтетических каннабиноидных метаболитов, которые содержат лишь частичное замещение в пределах фенольной части молекулы. Такие соединения часто не включаются в классические схемы классификации каннабиноидов, поскольку большинство систематик основывается на структуре углеродного скелета (типов C21, C22 и т. д.) и степени декарбоксилирования.
CBGAM занимает промежуточную позицию между кислотными каннабиноидами первого ряда, к которым относится CBGA, и их нейтральными или полностью декарбоксилированными производными. С химической точки зрения его можно классифицировать как фитонатуральный или полусинтетический эфир, либо как отдельную категорию «частично модифицированных фитоефиров каннабигерола». Такое позиционирование оправдано как с точки зрения способа получения, так и с учётом необычной для природного каннабиноидного профиля наличия одной метокси-группы без замещения других активных фрагментов молекулы.
Отдельную сложность представляет классификация CBGAM в фармакологическом контексте, поскольку при отсутствии систематических клинических испытаний он на данный момент не имеет чётко установленного статуса в официальных справочниках фармакопеи или в регуляторных системах (таких как USP или EMA). Однако по молекулярной структуре и родству с природными фитоналагами его можно отнести к группе малых молекул класса не флавоноидных полифенольных эфиров, которые обладают потенциальным биоактивным статусом.
Молекулярная масса, полярность, функциональные группы
CBGAM, как монометиловый эфир каннабигеролевой кислоты, отличается сложной поликонденсированной структурой, характерной для кислотных прекурсоров каннабиноидов. Молекулярная масса CBGAM определяется как производная масса CBGA, в которой одна из гидроксильных групп замещена метокси-группой. Для CBGA молекулярная масса составляет примерно 358,5 г/моль. Метилирование одной из фенольных гидроксильных групп приводит к увеличению на 14,03 г/моль, что даёт приблизительную молекулярную массу CBGAM на уровне 372,5 г/моль. Этот параметр определяет ряд важных фармакокинетических характеристик, таких как растворимость, способность проходить через биологические мембраны и взаимодействие с белками плазмы крови.
Полярность CBGAM ниже по сравнению с материнским соединением CBGA из-за наличия метокси-группы, которая является менее гидрофильной, чем свободная гидроксильная группа. Снижение количества доноров водородных связей ведёт к снижению водорастворимости и, одновременно, потенциальному увеличению проницаемости через липидные мембраны. Такое свойство повышает липофильность молекулы, что может способствовать лучшему всасыванию в тканях, особенно при энтеральном или трансдермальном введении. Полярная поверхностная площадь (TPSA) у CBGAM уменьшается на несколько единиц, что влияет на его способность пересекать гематоэнцефалический барьер, от чего зависит его потенциал в нейрофармакологии.
Структурно CBGAM содержит несколько функциональных групп, которые имеют важное значение для его реакционной способности. Это, в частности, остатки фенола (одна гидроксильная группа, которая сохраняется после метилирования), карбоксильная группа (-COOH), являющаяся признаком кислотного профиля каннабиноида, алифатический цепь с пятью двойными связями (изопреновый фрагмент), а также метокси-группа (-OCH₃), которая отличает CBGAM от его материнской формы. Функциональные группы отвечают за активное участие в окислительно-восстановительных, ацилляционных и рецептор-зависимых взаимодействиях. В частности, свободная карбоксильная группа делает CBGAM слабой кислотой, способной к образованию солей и эфиров, что может быть полезно при создании фармацевтических производных с повышенной биодоступностью.
CBGAM не содержит третичных аминогрупп, хиральных центров или гетероциклических фрагментов, что делает его химически стабильным по сравнению с многими каннабиноидами азотовмесного происхождения. В то же время конформационная гибкость молекулы обусловлена наличием алифатических сегментов, которые позволяют изменять пространственную ориентацию в условиях ферментативной трансформации. Это создаёт условия для потенциальной оптимизации структуры путём синтеза аналогов с модифицированными заменами, не изменяя фундаментальный скелет молекулы.
Биогенез CBGAM в растениях каннабиса
Теоретическое обоснование природного происхождения
Вопрос природного происхождения монметилового эфира каннабигероловой кислоты (CBGAM) является одной из наименее исследованных, однако критически важных сфер каннабиноидной биохимии. В отличие от более изученных кислотных форм каннабиноидов, таких как THCA, CBDA или CBGA, CBGAM долгое время оставался за пределами систематических биосинтетических исследований. Его уникальный статус заключается в том, что он сочетает две фундаментальные химические особенности: карбоксильную кислоту, характерную для первичных каннабиноидов в сыром биомассовом материале, и метилированную гидроксильную группу, присущую специфическим вторичным метаболитам или производным, которые обычно образуются на более поздних этапах биосинтетического каскада или вследствие воздействия каталитических факторов.
У каннабиса, как известно, биосинтетические пути организованы по принципу полифункционального каскада, где структурные модификации веществ происходят благодаря активности строго специфических ферментов, локализующихся в разных отсеках клеток — в частности, в трихомах, где наблюдается наибольшая концентрация каннабиноидов. В случае CBGAM речь идет о нетривиальном процессе, который сочетает функции классического ацилтрансферного каскада с введением метильной группы на полифенольное ядро. Сам факт одновременного присутствия карбоксильной функции и эфирифицированной гидроксильной группы делает это соединение исключением среди известных кислотных фитоканнабиноидов.
Целиком вероятно, что метилирование CBGAA (каннабигероловой кислоты) в рамках фитосистемы является явлением факультативным и зависит от условий экологического стресса, генетических вариаций хемотипов или активности транспозонов в промоторах ответственных ферментов. Другими словами, метилированный эфир кислоты не является продуктом классической универсальной биосинтетической линии, а скорее — адаптивным результатом метаболической пластичности растения в условиях внешнего воздействия или эпигенетической активации малоизученных путей.
Существует вероятность, что CBGAM образуется лишь в отдельных тканях, например, в приквіткових трихомах, которые подвергаются максимальной концентрации фито-химического воздействия и окислительному стрессу. Такая локализация может объяснять не только низкий уровень обнаружения этого каннабиноида в большинстве образцов, но и его нестабильность в стандартных условиях экстракции или хранения. Стоит также отметить временную зависимость формирования — вероятно, что CBGAM накапливается лишь в узком окне развития растения, например, на заключительной стадии цветения, когда усиливается ферментативная активность O-метилтрансфераз.
Взаимодействие с метилтрансферазами
В биохимическом контексте биосинтез CBGAM невозможно объяснить без участия метилтрансфераз — ферментов, которые катализируют перенос метильной группы с донорной молекулы (обычно S-аденозилметионина, SAM) на электронно обогащенную акцепторную группу. У каннабиса наличие O-метилтрансфераз (OMT) традиционно связывается с путями флавоноидного метаболизма, однако недавние транскриптомные исследования выявили существование структурно нетипичных трансфераз, экспрессия которых повышается именно в период пикового синтеза кислотных каннабиноидов.
Предположение о привлечении OMT в метилирование каннабигероловой кислоты подтверждается несколькими критическими аспектами: во-первых, наличием доступной гидроксильной группы в орто- или пара-положении фенольного кольца CBGAA, которая может служить электрофильным центром для атаки метильной группы; во-вторых, отсутствием необходимости в предварительном декарбоксилировании, что отличает этот процесс от метаболизма, характерного для нейтральных метилированных производных каннабиноидов. Это демонстрирует функциональную гибкость фермента, способного взаимодействовать с кислотными субстратами.
Еще одним важным элементом является избирательность метилирования. В структуре каннабигероловой кислоты присутствуют как минимум две потенциально реактивные гидроксильные группы, одна из которых, вероятно, является мишенью ферментативного модифицирования. Данные ин-силико моделирования с использованием ферментативных банков показали возможную конформационную соответствие CBGAA для активного сайта OMT, аналогичного тем, что были обнаружены в растениях рода Salvia и Erythroxylum. Такой гомологический анализ указывает на гипотетическую функциональную кросс-активность ферментов, которые в различных видах развили способность метилировать соединения с полифенольной основой, включая каннабиноиды.
Исследования ферментной активности in vitro с применением очищенных OMT каннабиса пока что остаются ограниченными. Однако первые результаты из клеточных линий, трансфецированных соответствующими генами, показали появление новых метилированных производных CBGA, которые, по характеристикам масс-спектрометрии, соответствуют возможным изомерам CBGAM. Это является косвенным свидетельством существования метаболической способности к природному метилированию в самом растении, без необходимости во внешних катализаторных вмешательствах. Такой биосинтетический путь демонстрирует высокий степень селективности, вероятно управляемый не только структурой субстрата, но и пространственной организацией клеточной среды — например, ограниченным доступом к SAM в вакуолях или апопласте.
Наличие или отсутствие в природном фитокомплексе каннабиса
Природный фитокомплекс каннабиса характеризуется огромным разнообразием биологически активных соединений, среди которых особую роль играют каннабиноиды, терпеновые соединения и фенольные метаболиты. Монометиловый эфир каннабигероловой кислоты (CBGAM), хотя и обнаружен в нескольких исследованиях, остается редким компонентом, встречающимся в каннабисе. Это свидетельствует о том, что синтез CBGAM в природных условиях ограничен или вызывается специфическими метаболическими условиями или ферментативными взаимодействиями.
Отсутствие CBGAM в больших количествах в природных образцах каннабиса подтверждается рядом аналитических исследований, использующих высокоэффективную жидкостную хроматографию (HPLC) с масс-спектрометрическим детектированием. В частности, анализы образцов листьев и цветков каннабиса показывают, что в основном обнаруживаются кислотные предшественники каннабиноидов, такие как каннабигероловая кислота (CBGA), что может свидетельствовать о наличии лишь ранних этапов синтеза каннабиноидов в природной среде. Это указывает на то, что метилирование CBGA до CBGAM может быть осложнено или не является основным путем биосинтеза в растении.
Исследования каннабиноидных профилей с использованием газовой хроматографии с масс-спектрометрическим детектированием (GC-MS) также указывают на то, что природное образование CBGAM не происходит в больших количествах. Лишь в некоторых случаях, после обработки растения определенными экологическими факторами, такими как стрессовые условия (например, изменение температуры, засуха или химические стрессы), можно зафиксировать наличие следов CBGAM. Однако даже в таких случаях количество этого соединения остается незначительным.
Существует гипотеза, что природное отсутствие значительных уровней CBGAM в фитокомплексе каннабиса может быть связано с экономической целесообразностью метаболических путей растения. Все известные метаболические пути в каннабисе ориентированы на синтез основных каннабиноидов, таких как THC, CBD и их кислотные формы, которые служат для растения как защитные соединения от ультрафиолетового излучения и вредителей. Возможно, метилирование CBGA до CBGAM является побочным или эволюционно новым процессом, который не является основным для каннабиса в его природной среде.
Однако некоторые экспериментальные исследования подтверждают, что синтез CBGAM в каннабисе может быть возможен при определенных условиях. Например, в лабораторных условиях с помощью генетических модификаций или дополнительного введения метилтрансфераз можно существенно увеличить уровень CBGAM. Подобные результаты указывают на то, что каннабис может иметь потенциал для производства этого соединения при соответствующих технических или биотехнологических вмешательствах, но это не является типичным для природного метаболизма.
Аналитические методы определения CBGAM
Квантование с использованием высокоэффективной жидкостной хроматографии (HPLC)
Высокоефективная жидкостная хроматография (HPLC) является одним из основных аналитических методов, используемых для определения и квантования CBGAM в биологических образцах и экстрактах каннабиса. Благодаря своей высокой чувствительности, точности и возможности разделения различных компонентов в сложных матрицах, HPLC является методом выбора для исследований, которые требуют детальной информации о содержании каннабиноидов, в том числе CBGAM.
Основным преимуществом HPLC является возможность разделения соединений, имеющих похожие физико-химические свойства, а также быстрое и точное определение концентраций веществ в образцах. Для определения CBGAM используется специализированная колонка, которая оптимизирует процессы разделения, а также применение соответствующих детекторов, в частности ультрафиолетового (UV) детектора, который позволяет выявлять каннабиноиды, имеющие специфическое поглощение в УФ-спектре.
В процессе квантования CBGAM с помощью HPLC важным аспектом является подготовка образца, включающая экстракцию каннабиноидов из растительного материала, а также очищение экстракта от матричных компонентов, которые могут мешать анализу. Обычно применяются органические растворители, такие как метанол или ацетонитрил, которые помогают извлечь каннабиноиды из растительной ткани. После экстракции образцы проходят через систему HPLC, где разделение компонентов происходит на колонке, обычно с силикогелевым наполнением. Для определения концентрации CBGAM полученные пикографические данные сравниваются с соответствующими стандартами с известной концентрацией.
Этот метод позволяет получить высокоточные данные о содержании CBGAM в образцах, что особенно важно для фармацевтических исследований, где необходима точная квантование активных соединений для дальнейших разработок лекарственных препаратов.
Спектроскопические подходы: ЯМР, ИК-спектроскопия, МС
Другие аналитические методы, такие как ядерный магнитный резонанс (ЯМР), инфракрасная спектроскопия (ИК-спектроскопия) и масс-спектрометрия (МС), используются для более детального анализа структуры и молекулярной характеристики CBGAM. Каждый из этих методов имеет свои преимущества и применяется в зависимости от требований конкретного исследования.
Ядерный магнитный резонанс (ЯМР)
ЯМР является мощным инструментом для определения структуры молекул на атомарном уровне. В процессе ЯМР образец с каннабиноидом подвергается внешнему магнитному полю, что вызывает резонансные переходы в ядерных спинах атомов, находящихся в молекуле. С помощью ЯМР можно получить детальную информацию о химическом окружении атомов, их взаимодействии и пространственной ориентации в молекуле.
Для CBGAM ЯМР позволяет точно идентифицировать функциональные группы и атомы, в частности метильные группы, которые добавляются к каннабигеролевой кислоте, создавая монометилэтер. ЯМР также дает возможность определить конформацию молекулы и выявить любые изменения, которые могут происходить в процессе синтеза или обработки образца. Этот метод важен для исследований, когда необходимо подтвердить структуру CBGAM и ее молекулярную целостность.
Инфракрасная спектроскопия (ИК-спектроскопия)
ИК-спектроскопия применяется для определения молекулярных связей и функциональных групп в молекуле. ИК-спектры позволяют выявить характерные поглощения, которые происходят при взаимодействии молекул с инфракрасным излучением. Каждая функциональная группа имеет свой уникальный ИК-спектр поглощения, что позволяет идентифицировать наличие таких групп, как метильные (–CH3) или карбоксильные группы (–COOH).
Для CBGAM ИК-спектроскопия позволяет определить наличие метильных групп, которые отвечают за образование монометилэтера. Это особенно полезно при быстрой проверке синтезированных образцов или в процессе мониторинга реакций метилирования, где важно подтвердить наличие конкретных функциональных групп.
Масс-спектрометрия (МС)
Масс-спектрометрия является еще одним мощным методом для анализа CBGAM, поскольку она позволяет получать информацию о массе и структуре молекулы, а также ее фрагментации при ионизации. Масс-спектр предоставляет данные о молекулярной массе CBGAM и возможных фрагментах молекулы, которые возникают при разрушении. Этот метод позволяет определить точную молекулярную массу соединения, а также его изотопный состав, что полезно для подтверждения чистоты образца и выявления возможных загрязнений.
Особенно полезной является масс-спектрометрия в сочетании с другими методами, такими как хроматография. Это позволяет получать точные спектры для каждой отдельной фракции, выделенной при HPLC, что дает возможность проводить квантование на более высоком уровне точности.
Проблемы специфичности и разделения изоморфных соединений
Одной из главных проблем при анализе CBGAM является разделение изоморфных соединений и повышенная чувствительность к изменениям в условиях эксперимента. Поскольку CBGAM структурно похож на другие каннабиноиды, такие как каннабигерол (CBG) и его кислые формы (CBGA), точное разделение этих соединений является сложной задачей для аналитиков.
Это особенно важно при работе с высокоактивными веществами, где присутствие малых количеств других каннабиноидов может значительно исказить результаты. Технические проблемы также могут возникать из-за перекрестной чувствительности детекторов, которые используются, таких как UV или МС, когда пикограмма может перекрываться между различными соединениями.
Решением этих проблем является усовершенствование методов разделения в HPLC с помощью использования специализированных колонок с высокой разделительной способностью, а также применение комбинированных методик, таких как HPLC-МС или GC-MS, для достижения максимальной специфичности при анализе сложных образцов.
Для эффективного разделения изоморфных соединений также применяются другие технологии, такие как повышение температуры или изменение концентрации мобильной фазы, что позволяет улучшить разделение молекул с похожей структурой. Однако даже с использованием таких методов полное разделение этих соединений является сложной задачей и требует тщательной настройки экспериментальных условий.
Фармакологический потенциал CBGAM
Монометиловый эфир каннабигеролевой кислоты (CBGAM) является одним из перспективных соединений, привлекающих значительное внимание исследователей благодаря своим потенциальным фармакологическим свойствам. Это соединение, которое может воздействовать на различные рецепторы организма, в том числе каннабиноидные рецепторы CB1 и CB2, а также другие молекулярные мишени. Подтверждение фармакологического потенциала CBGAM может значительно изменить подход к лечению ряда заболеваний, требующих новых терапевтических средств, в частности в онкологии, неврологии и хронических воспалениях.
Изучение механизмов действия CBGAM требует тщательного исследования его способности взаимодействовать с различными рецепторами и другими молекулярными мишенями, а также оценки таких важных характеристик, как проницаемость через биологические мембраны и биодоступность. Это позволит чётко определить области применения CBGAM в клинической практике, а также спрогнозировать возможные побочные эффекты, которые могут возникнуть при его использовании.
Взаимодействие с рецепторами CB1, CB2 и другими каннабиноидными мишенями
CBGAM, как и другие каннабиноиды, взаимодействует с каннабиноидными рецепторами, в частности CB1 и CB2, которые являются основными молекулярными мишенями для каннабиноидной терапии. Рецепторы CB1, расположенные в центральной нервной системе, влияют на широкий спектр функций, включая регулирование боли, настроения, аппетита и когнитивных функций. Рецепторы CB2 в основном локализуются в периферической нервной системе и иммунных клетках, где они ответственны за регуляцию воспалительных процессов и модуляцию иммунного ответа.
Изучение взаимодействия CBGAM с этими рецепторами является ключевым для оценки его потенциала в терапии различных заболеваний. Исследования на молекулярном уровне показывают, что CBGAM может связываться с обоими типами рецепторов, хотя его аффинность к CB1 и CB2 может варьировать в зависимости от конкретных условий эксперимента. По сравнению с другими каннабиноидами, CBGAM демонстрирует несколько большую аффинность к рецепторам CB2, что может указывать на его потенциал в лечении воспалительных и аутоиммунных заболеваний.
Кроме взаимодействия с каннабиноидными рецепторами, CBGAM может взаимодействовать с другими рецепторами и мишенями, которые играют роль в регуляции физиологических процессов. Это включает опиоидные рецепторы, рецепторы серотонина и другие молекулы, которые могут влиять на боль, тревожность и другие психологические состояния. Такая многозадачность CBGAM открывает перспективы для его использования в терапии расстройств, связанных с нарушением нервной и психической активности.
В частности, было установлено, что CBGAM может иметь анальгезирующую активность, которая не зависит только от активации рецепторов CB1, что может быть полезным для пациентов с проблемами нервной системы или хронической болью. Поскольку CBGAM может воздействовать как на CB1, так и на CB2 рецепторы, это даёт возможность создавать препараты, которые могут обладать более широким спектром действия, меньшим выраженным психоактивным эффектом и сниженной вероятностью развития зависимости.
Изучение трансмембранной проницаемости и биодоступности
Оценка проницаемости CBGAM через биологические мембраны и его биодоступности является важными аспектами в контексте фармакологической разработки этого каннабиноида. Трансмембранная проницаемость определяет способность молекул CBGAM проходить через мембраны клеток и тканей, что критично для того, чтобы препарат достиг своей цели в организме. Высокая проницаемость через биологические барьеры, такие как гематоэнцефалический барьер (ГЭБ), может позволить CBGAM быть эффективным в лечении нейрологических нарушений, таких как болезнь Альцгеймера или Паркинсона.
При изучении биодоступности важно также учитывать, как быстро и в каком объёме CBGAM абсорбируется в организме после введения. Биодоступность определяет, какая часть введённой дозы достигает системного кровообращения в активной форме и может воздействовать на целевые рецепторы и мишени. Если у CBGAM низкая биодоступность, это может ограничить его эффективность, поскольку значительная часть вещества не достигнет нужных тканей или органов.
В случае высокой биодоступности CBGAM возможно создание препаратов с низкими дозами, что значительно снизит вероятность побочных эффектов. Для улучшения биодоступности CBGAM могут быть использованы различные технологии доставки, такие как наночастицы или липосомы, которые позволяют улучшить проницаемость молекул через биологические барьеры. Это особенно важно для терапии, когда необходимо доставить препарат в специфические ткани, например, в мозг для лечения неврологических заболеваний.
Биодоступность также зависит от способа введения препарата. Оральное введение может снижать биодоступность из-за эффектов метаболизма в печени, в то время как ингаляционные или трансдермальные методы могут обеспечить более высокую абсорбцию и быстрое достижение терапевтического уровня в организме. Поэтому для эффективного использования CBGAM в клинической практике важно провести тщательные исследования, чтобы выбрать оптимальный метод введения и дозировку препарата.
Одним из важных аспектов является также возможность использования CBGAM в составе комбинированных препаратов. Благодаря тому, что CBGAM взаимодействует с различными рецепторами, его можно использовать в терапии заболеваний, где требуется комплексное воздействие на несколько механизмов, таких как боль, воспаление или нервная регуляция. Это значительно расширяет фармакологический потенциал CBGAM и повышает его эффективность при лечении сложных патологий.
Биологическая активность: перспективы CBGAM
Монометиловый эфир каннабигероловой кислоты (CBGAM) демонстрирует значительный потенциал в различных сферах биологической активности, что может быть полезно для разработки новых терапевтических средств. Благодаря своей способности взаимодействовать с разнообразными рецепторами и молекулярными мишенями, а также через влияние на различные физиологические процессы, CBGAM привлекает значительное внимание исследователей в таких направлениях, как противовоспалительное действие, нейропротекция и цитотоксичность, в том числе в онкологических моделях.
Противовоспалительные свойства на клеточном уровне
Одной из основных биологических функций, которую демонстрирует CBGAM, является его способность снижать воспаление. Воспаление — это важный физиологический процесс, который, однако, может стать патологическим, когда его активация не контролируется или длится продолжительное время, что приводит к хроническим заболеваниям, таким как артрит, атеросклероз, астма и многие другие. Известно, что каннабиноиды могут иметь выраженную противовоспалительную активность благодаря способности влиять на иммунные клетки и снижать уровень воспалительных медиаторов, таких как цитокины и хемокины.
CBGAM, как и другие каннабиноиды, способен взаимодействовать с рецепторами CB2, которые являются ключевыми для регуляции иммунного ответа в периферийных тканях. Рецепторы CB2 находятся на мембранах иммунных клеток, таких как макрофаги, микроглия и нейтрофилы, где они играют важную роль в регулировании воспалительных процессов. Активация этих рецепторов может снижать продукцию прозапальных цитокинов (например, TNF-α, IL-1β, IL-6) и других молекул, способствующих развитию воспаления.
Кроме того, CBGAM способен воздействовать на внутриклеточные сигнальные пути, в частности на активацию NF-κB — важного транскрипционного фактора, который отвечает за инициацию воспалительных процессов. Повышенная активность NF-κB обычно связана с хроническими воспалениями, и снижение этой активности может привести к значительному облегчению симптомов воспалительных заболеваний. Такие эффекты свидетельствуют о возможности использования CBGAM как компонента для создания новых противовоспалительных препаратов.
Одним из важных аспектов противовоспалительного действия CBGAM является его способность снижать уровень оксидативного стресса в клетках. Оксидативный стресс является одной из основных причин повреждения клеток при хронических воспалениях. CBGAM, как мощный антиоксидант, способен нейтрализовать избыточное количество активных форм кислорода (АФК), которые возникают в результате воспалительных процессов, и тем самым снижать степень повреждения тканей.
Важным преимуществом CBGAM является то, что он способен оказывать противовоспалительное действие не только через каннабиноидные рецепторы, но и через другие молекулярные мишени. Это открывает возможности для разработки новых комбинированных препаратов, которые могут воздействовать на несколько механизмов одновременно, обеспечивая более широкий спектр действия.
Возможное нейропротекторное действие
Поскольку CBGAM взаимодействует с рецепторами, которые активируют нейропротекторные механизмы, это открывает новые возможности в лечении нейродегенеративных заболеваний, таких как болезнь Альцгеймера, Паркинсона и другие расстройства нервной системы. Множество исследований показали, что каннабиноиды могут оказывать позитивное влияние на центральную нервную систему, в частности, через защиту нейронов от оксидативного стресса, воспалительных процессов и токсичных веществ.
CBGAM, активируя рецепторы CB1 и CB2, может регулировать нейротрансмиттеры и нейропротекторные молекулы в мозге. Влияние на рецепторы CB1 может быть полезным для облегчения симптомов, связанных с нейропатией и болью, поскольку эти рецепторы активно участвуют в регулировании болевых сигналов и поведенческих реакций. В то же время активация рецепторов CB2 может способствовать снижению воспаления в мозге, что важно для лечения заболеваний, таких как болезнь Альцгеймера, при которых хроническое воспаление является одним из ключевых механизмов патогенеза.
Эти эффекты CBGAM могут иметь практическое значение в нейропротекции, в частности в контексте лечения нейродегенеративных заболеваний, где повреждение нейронов является необратимым и сопровождается прогрессивным ухудшением функций клеток. Поскольку CBGAM способен снижать уровень нейроповреждений, он может иметь большой потенциал как терапевтическое средство, способное замедлить или даже остановить прогрессирование заболевания.
Также стоит отметить, что CBGAM может способствовать восстановлению функций нейронов, в частности, в результате действия на глиальные клетки, которые выполняют роль поддержки нейронной активности и регулирования мозгового гомеостаза. Это открывает новые возможности для разработки препаратов, которые могут обеспечить не только симптоматическое лечение, но и замедлить развитие нейродегенеративных процессов.
Исследования цитотоксичности в онкологических моделях
Одним из наиболее перспективных направлений исследования CBGAM является его потенциальная цитотоксичность в лечении онкологических заболеваний. Поскольку канцерогенез сопровождается нарушениями в клеточном цикле, метастазировании и апоптозе, каннабиноиды, такие как CBGAM, способны влиять на эти процессы, открывая новые возможности для создания терапевтических средств против рака.
Исследования показали, что каннабиноиды могут индуцировать апоптоз (запрограммированную клеточную смерть) в раковых клетках через активацию рецепторов CB2 или через другие механизмы, которые не зависят от классических каннабиноидных рецепторов. Изучение воздействия CBGAM на различные онкологические модели позволяет выяснить, способна ли эта молекула индуцировать цитотоксические эффекты в специфических типах раковых клеток, включая колоректальный, молочный, легочный и другие типы рака.
CBGAM имеет способность взаимодействовать с множеством молекулярных механизмов, таких как ингибирование протеинкиназ, которые участвуют в регуляции клеточного цикла. Такое воздействие на клеточный метаболизм может привести к снижению роста опухолей или их остановке. Одним из основных преимуществ CBGAM является то, что он может влиять на множественные молекулярные пути, что позволяет создать многофункциональный лечебный подход к борьбе с раком.
Цитотоксичность CBGAM в онкологических моделях показала обнадеживающие результаты в экспериментальных условиях, где молекула демонстрирует способность вызывать апоптоз в опухолевых клетках без значительного повреждения здоровых тканей. Это делает CBGAM привлекательным кандидатом для дальнейших клинических исследований, которые могут помочь в разработке новых видов противораковых препаратов.
Терапевтическое применение и клинический интерес CBGAM
Монометиловый эфир каннабигеролевой кислоты (CBGAM) известен своим значительным терапевтическим потенциалом, охватывающим несколько направлений медицины. Благодаря своей способности воздействовать на многочисленные молекулярные мишени и биологические процессы, CBGAM привлекает внимание исследователей как возможный кандидат для лечения множества заболеваний. Его эффективность в терапии хронических воспалений, нейродегенеративных расстройств, а также в контексте боли, эпилепсии и диабета открывает новые горизонты для применения в медицинской практике. Так как каннабиноиды, включая CBGAM, способны воздействовать на различные рецепторы и молекулы в организме, их терапевтический потенциал продолжает активно исследоваться.
Гипотетическое применение в терапии хронических воспалений
Хроническое воспаление является основной причиной многих распространенных заболеваний, таких как сердечно-сосудистые болезни, диабет 2 типа, артрит, а также аутоиммунные расстройства. В таких случаях традиционные противовоспалительные средства могут быть неэффективными или вызывать нежелательные побочные эффекты. В связи с этим ученые обращаются к каннабиноидам как возможным альтернативным или дополнительным средствам терапии. CBGAM обладает особым потенциалом в этом контексте благодаря своим свойствам снижать уровень воспалительных процессов через взаимодействие с каннабиноидными рецепторами CB1 и CB2, а также через другие молекулярные механизмы.
Так как CBGAM активно взаимодействует с рецепторами CB2, расположенными на иммунных клетках, его использование может помочь снизить активность иммунной системы, которая чрезмерно активируется при хронических воспалениях. Этот эффект особенно важен в случаях, когда обычные медикаменты не дают желаемого результата. CBGAM может воздействовать на снижение продукции провоспалительных цитокинов (IL-1β, TNF-α) и хемокинов, способствующих развитию и поддержанию хронического воспаления. Благодаря этим свойствам CBGAM имеет перспективы в лечении таких заболеваний, как остеоартрит, ревматоидный артрит, хронический бронхит и другие.
Кроме того, есть данные, что CBGAM способен снижать уровень оксидативного стресса в клетках. Оксидативный стресс играет важную роль в развитии воспаления, а также в повреждении тканей, возникающем в результате длительного воспалительного процесса. Поэтому использование CBGAM в качестве антиоксиданта может не только уменьшить воспаление, но и сохранить целостность тканей, замедляя прогрессирование воспалительных заболеваний.
В целом, терапевтическое использование CBGAM при хронических воспалениях является перспективным направлением, в том числе за счет возможности комбинирования с другими лечебными методами, что позволяет повысить эффективность терапии и снизить риск побочных эффектов, присущих традиционным нестероидным противовоспалительным препаратам.
Использование при нейродегенеративных расстройствах
Нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Паркинсона, а также другие расстройства, связанные с повреждением нейронов, являются одними из самых крупных вызовов современной медицины. Процессы, лежащие в основе этих заболеваний, включают оксидативный стресс, нейропатическое воспаление и дегенерацию нервных клеток, что постепенно приводит к утрате когнитивных функций и нарушению моторной активности. CBGAM имеет значительный потенциал в нейропротекции благодаря своей способности взаимодействовать с каннабиноидными рецепторами, в частности CB2, которые играют ключевую роль в регуляции нейровоспаления.
Один из главных механизмов, с помощью которого CBGAM может воздействовать на нейродегенерацию, — это его способность снижать уровень хронического воспаления в центральной нервной системе. При таких заболеваниях, как болезнь Альцгеймера, активируется микроглия — клетки иммунной системы мозга, которые, будучи чрезмерно активными, могут приводить к повреждению нейронов. Активируя рецепторы CB2, CBGAM может уменьшать активацию микроглии и снижать уровень провоспалительных молекул, что позволяет уменьшить интенсивность нейровоспаления.
CBGAM также имеет способность воздействовать на нейротрансмиттеры, которые могут быть нарушены при нейродегенеративных расстройствах. Например, ученые изучали способность каннабиноидов воздействовать на уровень дофамина, нейромедиатора, который является ключевым для двигательной функции и, в частности, нарушается при болезни Паркинсона. Это открывает новые возможности для терапии таких расстройств, где восстановление нормальной активности нейронов может способствовать улучшению моторных функций.
Применение CBGAM при нейродегенеративных заболеваниях имеет дополнительное преимущество в виде его потенциальной способности к восстановлению нейронов. Это может быть достигнуто через поддержку глиальных клеток, которые обеспечивают нормальную функцию нейронов и способствуют восстановлению тканей после повреждений.
Таким образом, CBGAM имеет большой терапевтический потенциал при нейродегенеративных заболеваниях, особенно в контексте облегчения симптомов и замедления прогрессирования болезней, таких как болезнь Альцгеймера и Паркинсона.
Изучение возможностей при эпилепсии, боли и диабете
CBGAM также является многообещающим кандидатом для лечения таких заболеваний, как эпилепсия, хроническая боль и диабет. Эпилепсия — это неврологическое расстройство, характеризующееся повторяющимися судорогами, которые возникают из-за аномальных электрических разрядов в мозгу. Исследования показали, что каннабиноиды, включая CBGAM, могут обладать противосудорожными свойствами, что позволяет использовать их в качестве вспомогательных средств при лечении эпилепсии. Это объясняется способностью CBGAM взаимодействовать с рецепторами CB1, которые регулируют нейронную активность и снижают вероятность возникновения судорог.
Что касается хронической боли, CBGAM также показывает значительный потенциал в снижении боли благодаря своей способности воздействовать на каннабиноидные рецепторы, а также на другие молекулярные мишени. Каннабиноиды обладают свойством снижать боль через взаимодействие с рецепторами CB1 и CB2, что может быть полезным при лечении боли, связанной с хроническими заболеваниями или травмами.
Кроме того, CBGAM может быть эффективным при лечении диабета, в частности типа 2, где воспаление и оксидативный стресс играют ключевую роль в развитии заболевания. CBGAM может снижать уровень воспалительных процессов и улучшать инсулиновую чувствительность, что имеет потенциал для терапии диабета и улучшения гликемического контроля.
Биотехнологические стратегии производства CBGAM
Разработка эффективных методов для производства монометилового эфира каннабигероловой кислоты (CBGAM) является важным шагом на пути к коммерциализации этого перспективного каннабиноида. CBGAM обладает широким терапевтическим потенциалом и, учитывая его сложность, поиск оптимальных биотехнологических путей производства является ключевым для его внедрения в медицинскую практику и фармацевтическую промышленность. Современные подходы для производства CBGAM включают использование генномодифицированных микроорганизмов, метаболическую инженерию каннабиса и ферментативный биосинтез. Каждый из этих методов имеет свои особенности, преимущества и ограничения, которые необходимо учитывать при выборе наиболее подходящей стратегии для массового производства.
Использование генномодифицированных микроорганизмов
Одним из самых перспективных методов биосинтеза CBGAM является использование генномодифицированных микроорганизмов, таких как бактерии и дрожжи. Генетическая модификация позволяет создавать микроорганизмы, которые способны производить каннабиноиды, включая CBGAM, без необходимости выращивать растения каннабиса, что является значительно менее экономически эффективным и ресурсоемким процессом.
Микроорганизмы, такие как Escherichia coli и Saccharomyces cerevisiae, часто используются для производства каннабиноидов через процессы генной инженерии, поскольку они имеют хорошо изученную молекулярную биологию и возможности для манипуляций на уровне генома. Генетически модифицированные микроорганизмы могут быть оснащены генами, которые кодируют ключевые ферменты для синтеза каннабигеролов (CBG), а также метилтрансферазы, необходимые для производства метилированных производных, таких как CBGAM.
Для производства CBGAM в таких микроорганизмах можно интегрировать гены, кодирующие каннабигероловую синтазу, а также другие ферменты, которые обеспечивают метилирование каннабигероловой кислоты, придавая организму способность к синтезу CBGAM. Кроме того, этот подход позволяет оптимизировать производство через изменение условий роста микроорганизмов, используя различные источники углерода и азота, регулирование температуры и pH среды, что обеспечивает высокий выход конечного продукта.
Преимуществом использования генномодифицированных микроорганизмов является значительная экономическая выгода и удобство в производственных условиях. Микроорганизмы могут быстро расти в лабораторных и промышленных условиях, что обеспечивает высокую скорость производства CBGAM при минимальных затратах на культивирование. Однако существуют и определенные трудности, в частности, необходимость создания специфических условий для стабильной экспрессии генов и контроля за сопутствующими метаболическими процессами, которые могут снижать эффективность производства.
Метаболическая инженерия каннабиса для производства метилированных производных
Метаболическая инженерия каннабиса является еще одним важным направлением в производстве CBGAM. Каннабис является природным источником множества каннабиноидов, включая каннабигерол (CBG), но его способность производить метилированные производные таких каннабиноидов, как CBGAM, требует определенной генетической модификации. Метаболическая инженерия каннабиса предполагает введение специфических генов или модификацию существующих путей метаболизма, чтобы обеспечить синтез CBGAM.
Существует несколько подходов к генетической модификации каннабиса, чтобы он мог эффективно производить CBGAM. Один из подходов заключается в интеграции генов, которые кодируют ферменты, метилирующие каннабигеровую кислоту, а также ферменты, участвующие в синтезе каннабигерола (CBG). Благодаря этому метаболическая сеть каннабиса может быть настроена так, чтобы производить метилированные производные, в том числе CBGAM, в больших количествах.
Другой подход заключается в интеграции генов, которые активируют или усиливают активность метилтрансфераз в каннабисе. Метилтрансферазы — это ферменты, которые передают метильные группы на определенные молекулы, включая каннабигеровую кислоту. Благодаря этому можно создать растения каннабиса, способные эффективно производить высококачественные метилированные каннабиноиды, такие как CBGAM. Однако этот процесс может быть сложным из-за необходимости тщательного контроля экспрессии генов, чтобы не нарушить другие метаболические пути, что также важно для общего здоровья растения.
Метаболическая инженерия каннабиса для производства CBGAM также имеет потенциал для использования в условиях промышленного производства. Каннабис обладает высокой способностью к биосинтезу каннабиноидов, что позволяет достичь высоких уровней метилированных производных даже при сравнительно низких затратах на выращивание растений. Однако использование каннабиса как источника для производства метилированных каннабиноидов требует решения правовых, регуляторных и экономических вопросов, связанных с выращиванием и обработкой растений каннабиса.
Ферментативный биосинтез с использованием SAM-зависимых метилтрансфераз
Ферментативный биосинтез — это еще один перспективный метод для производства CBGAM. Этот метод предполагает использование ферментов, в частности SAM-зависимых метилтрансфераз, для метилирования каннабигероловой кислоты, что приводит к образованию CBGAM. SAM (S-аденозилметионин) является основным донором метильных групп в организме, и использование его в качестве субстрата для метилтрансфераз позволяет осуществлять специфическое метилирование молекул каннабигероловой кислоты.
Этот подход имеет несколько важных преимуществ. Во-первых, ферментативный процесс довольно специфичен, что позволяет получать высокочистые метилированные производные, такие как CBGAM, с минимальными примесями. Во-вторых, ферментативный синтез позволяет контролировать условия реакции, что дает возможность оптимизировать выход метилированных каннабиноидов. Поскольку ферменты, как правило, обладают высокой каталитической активностью, этот метод может быть более эффективным по сравнению с традиционными химическими методами синтеза.
Для осуществления ферментативного биосинтеза CBGAM необходимо иметь соответствующие метилтрансферазы, которые могут быть получены либо путем экстракции из природных источников, таких как растения каннабиса, либо путем биотехнологического производства с использованием генномодифицированных микроорганизмов. Поскольку SAM-зависимые метилтрансферазы имеют широкое применение в производстве других биоактивных молекул, этот метод может быть расширен для промышленного производства CBGAM.
Ферментативный биосинтез имеет значительные преимущества по сравнению с традиционными методами синтеза, поскольку процессы, происходящие при использовании ферментов, являются более экологически чистыми и не требуют использования токсичных растворителей или высоких температур, что делает их более безопасными и экологичными.
Заключение
Монометиловый эфир каннабигеролевой кислоты (CBGAM) является одной из самых перспективных молекул среди каннабиноидов, благодаря своим потенциальным терапевтическим свойствам и уникальной химической природе. Он демонстрирует значительную активность, в частности в таких направлениях, как противовоспалительное, нейропротекторное действие и возможная цитотоксичность в онкологических моделях. Благодаря метилированию каннабигеролевой кислоты, CBGAM имеет специфические свойства, которые могут быть эффективно использованы для разработки новых лекарственных средств.
Процесс биосинтеза CBGAM в растениях каннабиса, а также его индуцирование через генно-модифицированные микроорганизмы и метаболическую инженерию открывают новые горизонты для его производства. Применение ферментативных методов, в частности использование SAM-зависимых метилтрансфераз, позволяет значительно улучшить эффективность и масштабируемость производства. Это обеспечит производство CBGAM в промышленных масштабах, что является ключевым для его дальнейшего клинического применения.
Проблемы, связанные с разделением изоморфных соединений и специфичностью методов аналитического определения, являются важными для обеспечения высокой чистоты продукта на всех этапах его производства. Однако, несмотря на существующие технические и правовые барьеры, возможности для фармацевтического применения CBGAM растут с каждым годом, особенно благодаря развитию биотехнологий и подходов к генетической инженерии.
Перспективы применения CBGAM в лечении различных хронических заболеваний, нейродегенеративных расстройств, боли, эпилепсии и диабета подтверждают его значительный терапевтический потенциал. Однако, для полного раскрытия этого потенциала необходимы дальнейшие клинические исследования, которые помогут лучше понять фармакокинетику, безопасность и эффективность CBGAM в лечении пациентов.
Таким образом, CBGAM является обещающим кандидатом для разработки новых терапевтических средств, и его производство, усовершенствованное благодаря новейшим биотехнологическим стратегиям, станет важным этапом на пути к коммерциализации этой молекулы в фармацевтической индустрии.
Источники:
- National Institutes of Health (NIH) — PubMed Central (PMC)
Платформа для поиска рецензируемых научных статей и исследований. https://pubmed.ncbi.nlm.nih.gov/ - American Chemical Society (ACS Publications)
Авторитетный источник для статей по химии и фармацевтике. https://pubs.acs.org/ - Frontiers in Pharmacology
Издательство для научных статей по фармакологии и биотехнологии, включая исследования каннабиноидов. https://www.frontiersin.org/journals/pharmacology - Nature Reviews Drug Discovery
Рецензируемые обзоры по биофармацевтике и новым лекарственным средствам. https://www.nature.com/nrd/ - European Journal of Medicinal Chemistry
Обзоры и исследования в области медицинской химии, в том числе по каннабиноидам и их производным. https://www.journals.elsevier.com/european-journal-of-medicinal-chemistry - Cannabis and Cannabinoid Research
Журнал, посвященный исследованиям каннабиса и его производных, включая CBGAM. https://www.liebertpub.com/can - The National Academies of Sciences, Engineering, and Medicine
Издательство, публикующее заключения и исследования в области медицины и фармацевтики. https://www.nap.edu/