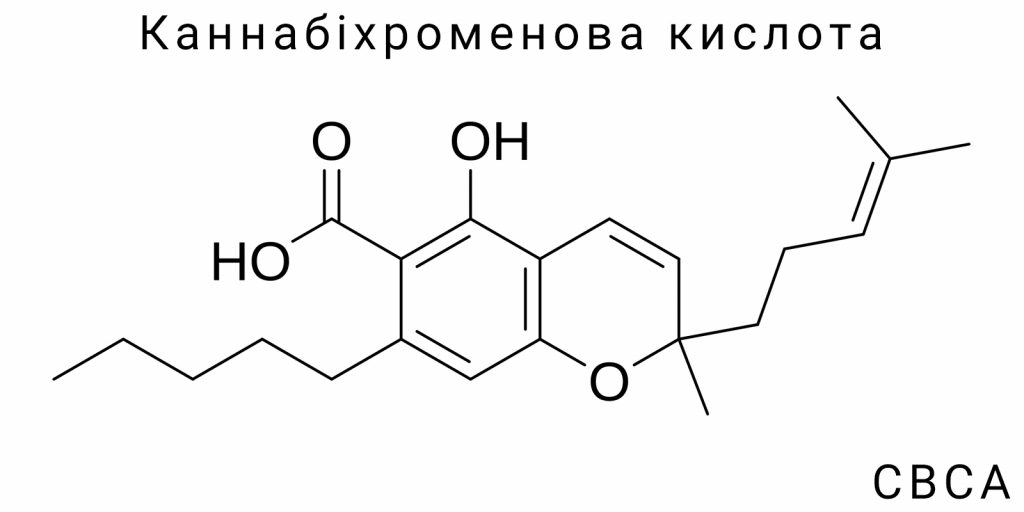
Канабіноїди – це хімічні сполуки, що зустрічаються в рослині Cannabis sativa, яка має давню історію використання в медичних цілях. Вони належать до групи вторинних метаболітів, що продукуються рослиною для захисту від стресових факторів, таких як ультрафіолетове випромінювання та шкідники. До основних канабіноїдів відносяться Δ9-тетрагідроканабінол (THC), канабідіол (CBD) та їх похідні, однак сучасні дослідження зосереджуються також на менш відомих сполуках, таких як канабіхроменова кислота (CBCA).
Загальний огляд канабіноїдів як вторинних метаболітів Cannabis sativa
Канабіноїди, як і інші вторинні метаболіти рослин, не мають функції в основних біологічних процесах, таких як ріст або розвиток рослини. Проте їх роль у захисті від шкідливих впливів навколишнього середовища є ключовою. Канабіноїди, зокрема, здатні взаємодіяти з різними рецепторами в організмах, включаючи людину, що зумовлює їх біологічну активність. Ці сполуки синтезуються в Cannabis sativa у вигляді кислотних форм, які потім декарбоксилюються для утворення нейтральних канабіноїдів, таких як THC і CBD.
Місце CBCA серед кислотних форм канабіноїдів
Канабіхроменова кислота (CBCA) є одним з головних кислотних попередників канабіхромену (CBC), одного з канабіноїдів, що привертає увагу завдяки своїм потенційним медичним властивостям, зокрема протизапальній та анальгезуючій дії. CBCA є первинною сполукою, що перетворюється на CBC після втрати карбоксильної групи. Однак важливо зазначити, що CBCA має свої унікальні властивості, які можуть бути корисними для медицини, хоча дослідження щодо цієї кислоти тривають.
Визначення CBCA як біохімічного попередника канабіхромену (CBC) і перспективної самостійної сполуки
CBCA є ключовим попередником канабіхромену (CBC), однак самостійно CBCA має певний біологічний потенціал. Дослідження свідчать про те, що CBCA може впливати на деякі фізіологічні процеси, зокрема через свою здатність взаємодіяти з канабіноїдними рецепторами, хоча її активність в цьому контексті потребує подальших досліджень. З огляду на це, CBCA має перспективи як самостійна сполука, зокрема в контексті її використання в медичних або терапевтичних цілях.
Враховуючи все це, дослідження CBCA як окремої сполуки може призвести до нових відкриттів у фармакології канабіноїдів, а також сприяти розвитку нових методів лікування на основі канабіноїдів.
Біогенез та хімічна характеристика
Канабіхроменова кислота (CBCA) є складовою частиною вторинного метаболізму Cannabis sativa, який продукує десятки біоактивних речовин із потенціалом до фармакологічного застосування. Біогенез CBCA розпочинається з канабігеролової кислоти (CBGA) – ключового попередника майже всіх основних канабіноїдів. Цей метаболіт, у свою чергу, утворюється шляхом конденсації оліветолової кислоти з геранілпірофосфатом у присутності специфічної синтетази. Далі на сцену вступає CBCA-синтаза – флавопротеїновий фермент, який каталізує циклізацію CBGA з утворенням три циклічної структури CBCA. Унікальність цього шляху полягає в тому, що CBCA-синтаза не виробляє інших канабіноїдів, а виключно CBCA, що підкреслює її ферментну специфічність (Taura et al., 2009, NIH.gov).
На відміну від більш поширених кислотних форм канабіноїдів, таких як THCA чи CBDA, CBCA менш вивчена, однак її біохімічна природа свідчить про важливу функціональну роль. CBCA має у складі карбоксильну групу, яка не лише визначає її кислотність, а й впливає на її фізико-хімічні властивості – зокрема, на здатність до іонізації, розчинність у полярних середовищах та хімічну стабільність. Молекулярна структура CBCA характеризується трициклічним ядром, що зумовлює просторову жорсткість і, ймовірно, визначає її взаємодію з білками чи рецепторами на відміну від гнучкіших лінійних форм канабіноїдів.
Особливої уваги заслуговує термолабільність CBCA. За збереження зразків при температурі навколишнього середовища, а тим більше під час нагрівання, CBCA поступово декарбоксилюється, втрачаючи вуглекислий газ і перетворюючись у нейтральну форму – канабіхромен (CBC). Цей процес є типовим для багатьох кислотних канабіноїдів, однак у випадку CBCA він має додаткову наукову цінність, оскільки дозволяє отримати CBC без сторонніх домішок інших канабіноїдів. Це особливо важливо в лабораторній практиці, де чистота реакції впливає на валідність фармакологічних досліджень (Morimoto et al., 1998, PubMed).
Слід зазначити, що навіть у природному середовищі CBCA може зазнавати спонтанного перетворення в CBC, особливо в умовах підвищеної температури або вологості. Цей факт має практичне значення для зберігання сировини Cannabis sativa, а також для визначення оптимальних умов екстракції канабіноїдів для дослідницьких або медичних потреб.
Інтерес до CBCA зростає також у контексті пошуку нових біомаркерів для хемотипування канабісу. Високий рівень CBCA в деяких сортах може вказувати на специфічну активність CBCA-синтази, що є потенційно цінним для селекційних програм і фармакологічного скринінгу. Більш того, хімічна унікальність цієї сполуки – зокрема, її відмінна стереохімія – може зумовлювати взаємодію з нетиповими молекулярними мішенями, що розширює горизонти її медичного застосування.
Дослідження фармакологічних властивостей
На відміну від більш відомих фітоканабіноїдів, таких як Δ9-тетрагідроканабінол (THC) або канабідіол (CBD), канабіхроменова кислота (CBCA) протягом тривалого часу залишалася поза основним фокусом наукової спільноти. Вона вважалася лише проміжним метаболітом на шляху до канабіхромену (CBC). Однак останні роки принесли нові дані, які дозволяють по-новому оцінити потенціал CBCA як біоактивної сполуки. Далі розглянуто основні напрямки досліджень, що формують уявлення про її фармакологічні властивості.
Протизапальна активність
Інгібування синтезу прозапальних факторів: CBCA має здатність впливати на процеси, які лежать в основі запалення. На клітинному рівні вона може пригнічувати експресію ферментів, які каталізують утворення прозапальних молекул. Зокрема, було показано, що CBCA знижує активність циклооксигенази-2 (COX-2), яка є ключовим ферментом у біосинтезі простагландинів – сполук, що ініціюють набряк, біль та почервоніння при запальних процесах.
Імуномодуляція: Окремі in vitro дослідження засвідчили здатність CBCA знижувати вивільнення прозапальних цитокінів, таких як інтерлейкін-6 (IL-6) та фактор некрозу пухлин альфа (TNF-α). Це може вказувати на потенціал CBCA як речовини, що регулює імунну відповідь, не пригнічуючи її повністю, а лише пом’якшуючи надмірну активацію, яка характерна для багатьох хронічних запальних станів.
Перспективи для клінічного застосування: Така протизапальна активність є особливо важливою з огляду на пошук альтернатив нестероїдним протизапальним препаратам (НПЗП), що часто викликають побічні ефекти з боку шлунково-кишкового тракту. Враховуючи, що CBCA не проявляє токсичності у фізіологічно релевантних дозах, вона заслуговує на подальше доклінічне дослідження як м’який імуномодулятор або допоміжний компонент у протизапальній терапії.
Антибактеріальні властивості
Дія на патогенні мікроорганізми: CBCA, подібно до деяких інших кислотних канабіноїдів, демонструє антибактеріальну активність проти низки грампозитивних бактерій. Особливо перспективною вважається її дія проти Staphylococcus aureus, включаючи антибіотикорезистентні штами. У лабораторних умовах вона сприяє порушенню структури клітинної стінки бактерій, що призводить до їх загибелі.
Механізм дії: мембранна дисфункція: На відміну від класичних антибіотиків, CBCA не впливає на синтез білків або ДНК бактерій. Замість цього вона, імовірно, дестабілізує ліпідну мембрану, створюючи пори, через які бактерія втрачає осмотичну рівновагу. Це цікавий і важливий механізм, оскільки дозволяє уникнути традиційних шляхів розвитку резистентності.
Можливість синергізму: Ще одним об’єктом дослідження є можливість поєднання CBCA з іншими протимікробними засобами. Згідно з окремими спостереженнями, CBCA може посилювати ефект таких сполук, як канабігеролова кислота (CBGA) або навіть класичних антибіотиків – це відкриває шлях до нових стратегій боротьби з мультирезистентними інфекціями.
Зв’язок із TRP-каналами
Вплив на сенсорні рецептори: CBCA виявляє активність у відношенні до рецепторів сімейства Transient Receptor Potential (TRP), зокрема TRPA1 та TRPV1. Ці іонні канали беруть участь у сприйнятті температури, хімічних подразників і болю. В експериментальних умовах CBCA здатна активувати ці канали, що може пояснювати її потенціал у зменшенні болю або зміні терморегуляторних реакцій.
Терапевтичні наслідки: Активація TRP-каналів асоціюється з полегшенням хронічного болю, зменшенням нейропатичних проявів та навіть участю у контролі запалення нервової тканини. Це дозволяє розглядати CBCA як компонент у створенні нових засобів для лікування станів, що супроводжуються сенсорними порушеннями, зокрема в контексті мігрені, фіброміалгії або термоневропатій.
Необхідність подальшого вивчення
Фармакокінетичні аспекти: Наразі існує обмежена кількість даних щодо всмоктування, розподілу, метаболізму і виведення CBCA в організмі людини або тварин. З огляду на її кислотну природу та потенційну нестабільність у нейтральному середовищі, вивчення фармакокінетики є критично важливим для майбутнього терапевтичного застосування.
Важливість як самостійної сполуки: CBCA не слід розглядати виключно як проміжний етап на шляху до CBC. Її власна біоактивність, відсутність психоактивних ефектів та багатогранна дія на різні біологічні системи дозволяють говорити про неї як про перспективну сполуку для фармакології, особливо у тих випадках, коли необхідна легка модуляція фізіологічних процесів без грубого втручання.
Наукова та клінічна привабливість: Застосування CBCA у медицині може бути привабливим як у монотерапії, так і у комбінації з іншими природними сполуками. Сучасні методи синтезу та очищення відкривають можливості для стандартизації, яка є необхідною умовою для початку доклінічних і клінічних досліджень.
Наукові перспективи та виклики
Попри зростаючий інтерес до рідкісних канабіноїдів, канабіхроменова кислота (CBCA) залишається мало вивченою порівняно з такими сполуками, як Δ9-тетрагідроканабінол (THC) чи канабідіол (CBD). Визначення її місця в сучасній біомедицині вимагає системного підходу – від базових досліджень до клінічного застосування, що наразі наштовхується на низку міждисциплінарних викликів.
Відсутність масштабних клінічних досліджень
На сьогодні жодне з великих фармакологічних чи клінічних досліджень, опублікованих у базах даних PubMed, ClinicalTrials.gov чи NIH.gov, не зосереджене винятково на CBCA. Наявна інформація про біологічну дію цієї сполуки базується переважно на попередніх лабораторних дослідженнях на культурах клітин (in vitro) або на тваринних моделях (in vivo). Це створює суттєвий інформаційний розрив між передклінічними результатами та потенційним клінічним застосуванням.
Наприклад, обіцяючі дані про протизапальну та антибактеріальну активність CBCA не можна автоматично перенести на людську фізіологію без підтвердження у клінічних умовах. Додатковою проблемою є низька біодоступність кислотних форм канабіноїдів, що ускладнює оцінку їх ефективності у пероральному або парентеральному введенні.
Крім того, чинні міжнародні протоколи клінічних досліджень не враховують особливостей рідкісних фітоканабіноїдів, що ускладнює їх реєстрацію в рамках дослідницьких ініціатив.
Ентомедичний контекст: потреба в системному підході
CBCA, як і інші кислоти канабіноїдів, може демонструвати фармакологічну активність не стільки в ізольованій формі, скільки в комбінації з іншими компонентами канабісу. Саме тому її слід вивчати в межах ентомедичного підходу – концепції, згідно з якою сумісна дія канабіноїдів, терпеноїдів та флавоноїдів забезпечує комплексну біологічну відповідь (ефект антуражу).
На даному етапі наукового розвитку бракує досліджень, які б оцінювали CBCA як частину хімічного ансамблю. Зокрема, невідомо, як CBCA впливає на активність CB1/CB2-рецепторів у присутності інших кислотних форм, чи може вона модулювати ефекти CBDA або THCA, чи існує синергія з терпеноїдами, що впливають на центральну або периферичну нервову систему.
Це відкриває перспективи для створення стандартизованих фітокомплексів, у яких CBCA відіграватиме роль не лише попередника CBC, а й модулятора системної відповіді організму.
Становлення фармацевтичного застосування
- Ще одним перспективним напрямом є включення CBCA до складу фармацевтичних засобів. Проте перед впровадженням у клінічну практику слід подолати низку викликів:
- Хімічна нестабільність: CBCA схильна до швидкого декарбоксилювання навіть при помірному нагріванні або тривалому зберіганні. Цей процес перетворює її на CBC, змінюючи як хімічні, так і біологічні властивості речовини. Для забезпечення стабільності необхідно розробити спеціальні умови зберігання та доставки (наприклад, мікроінкапсуляція або застосування антиоксидантних середовищ).
- Методи введення: CBCA має кислотну природу, що може ускладнювати її абсорбцію в шлунково-кишковому тракті. Потребує вивчення транспорту в біологічних мембранах, впливу рН-середовища, ферментативного розщеплення тощо. Серед перспективних форм – сублінгвальні краплі, трансдермальні пластирі або інгалятори.
- Потреба у фармакопейній стандартизації: жодна з провідних фармакопей світу – USP, EMA, JP – наразі не містить стандартів на CBCA, що робить неможливим її офіційне використання у медичній практиці. Для цього необхідне створення методів кількісного аналізу, визначення профілю домішок і стабільності, як це вже реалізовано для CBD.
Міждисциплінарні бар’єри: етика, право, технології
- Етичні аспекти
У багатьох юрисдикціях канабіноїди досі класифікуються як контрольовані речовини незалежно від того, чи мають вони психоактивні властивості. Це призводить до того, що дослідники мусять проходити ті ж самі регуляторні процедури, що й при роботі з THC, навіть якщо йдеться про CBCA – кислоту без відомого психоактивного ефекту. Подолання цих бар’єрів вимагає змін у нормативній базі та освітніх програмах для етичних комітетів. - Правові перепони
CBCA не має окремого правового статусу у більшості країн. Її наявність у екстрактах канабісу автоматично підпадає під загальні обмеження, навіть коли продукт містить її лише в мікродозах. Це ускладнює патентування, транспортування через кордон, ліцензування на виробництво та участь у спільних міжнародних дослідженнях. - Технологічні труднощі
Низька природна концентрація CBCA в рослинах унеможливлює економічно вигідну екстракцію за традиційними методами. Крім того, під час звичайної обробки сировини (сушіння, нагрівання, екстракція етанолом або CO₂) сполука деградує або перетворюється в CBC. Перспективними виглядають біотехнологічні методи – зокрема, виробництво CBCA за допомогою генетично модифікованих дріжджів або клітинних культур канабісу, що дозволяє створювати стандартизовану сировину для досліджень і фармацевтики.
Висновки
Канабіхроменова кислота (CBCA) дедалі більше привертає увагу як окрема ціль для наукових досліджень, а не лише як хімічний попередник канабіхромену (CBC). Зі структурної точки зору вона є відносно стабільною сполукою в межах кислотних форм канабіноїдів, що відкриває можливості для її зберігання, стандартизації та потенційного терапевтичного застосування без негайної необхідності декарбоксилювання.
Наявність карбоксильної групи формує унікальні властивості CBCA – зокрема, вплив на проникність клітинних мембран, можливості кон’югації з іншими біомолекулами та іншу фармакокінетику порівняно з декарбоксилировании аналогами. Її біологічна активність, хоч і не вивчена в повному обсязі, вказує на потенціал до регуляції імунних реакцій, антимікробної дії та взаємодії з TRP-рецепторами – що заслуговує на поглиблену експериментальну перевірку.
CBCA варто розглядати не лише в контексті її природного походження чи ролі у вторинному метаболізмі Cannabis sativa, а як перспективну фармакологічну одиницю. Подальше дослідження її властивостей вимагає мультидисциплінарного підходу – від хімії природних сполук до фармакології та біотехнології. Важливо також створити правове, технологічне й етичне підґрунтя для включення CBCA до майбутніх клінічних програм.
Використані джерела
- Shoyama, Y., et al. (2008). Біосинтез і функції канабіноїдних синтаз.
Журнал Journal of Natural Medicines.
Посилання: https://doi.org/10.1007/s11418-008-0251-5
У статті розглядається, як синтази канабіноїдів (ферменти, що утворюють канабіноїди) беруть участь у біосинтезі ТГК (THC), КБД (CBD) та інших сполук, а також які функції ці речовини виконують у рослині. - Gülck, T., & Møller, B. L. (2020).
Фітоканабіноїди: походження та біосинтез. Журнал Trends in Plant Science.
Посилання: https://doi.org/10.1016/j.tplants.2020.06.001
Оглядовий матеріал про те, як утворюються канабіноїди в рослинах, з поясненням генетичних шляхів, ферментів та еволюційного значення цих речовин як захисту від стресів і патогенів. - Appendino, G., et al. (2008). Антибактеріальні канабіноїди з Cannabis sativa: дослідження зв’язку між структурою та активністю.
Журнал Journal of Natural Products.
Посилання: https://doi.org/10.1021/np8002673
У цій роботі досліджуються антибактеріальні властивості різних канабіноїдів та визначається, як їх хімічна структура впливає на ефективність проти бактерій. - Russo, E. B. (2011). Приборкання ТГК: потенційна синергія канабісу та ефекти «супроводу» фітоканабіноїдів і терпенів.
Журнал British Journal of Pharmacology.
Посилання: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3165946
У статті описується ефект “супроводу”, за якого фітоканабіноїди та терпени працюють разом, підсилюючи один одного та покращуючи терапевтичний ефект канабісу. - Національна медична бібліотека США, база даних PubChem. Канабіхроменова кислота (CBCA).
Посилання: https://pubchem.ncbi.nlm.nih.gov/compound/CBCA
Сторінка з хімічними та біологічними даними про CBCA — менш відомий канабіноїд, попередник CBC (канабіхромену), з потенційними медичними властивостями. - Національні інститути здоров’я США (NIH). Дослідження канабіноїдів.
Посилання: https://cancer.gov
Офіційний ресурс із результатами досліджень використання канабіноїдів, зокрема для лікування онкологічних захворювань, знеболення та полегшення побічних ефектів хіміотерапії. - Європейський центр моніторингу наркотиків та наркоманії (EMCDDA). Канабіс і канабіноїди: фармакологія та токсикологія.
Посилання: https://www.emcdda.europa.eu
Інформація про дію канабіноїдів на організм, їхню фармакологічну дію, побічні ефекти, токсичність і медичне використання в ЄС.