Упродовж останніх десятиліть канабіноїди з об’єкта криміналізації поступово трансформувалися у предмет інтенсивного наукового інтересу. На тлі вичерпання можливостей класичних фармакотерапевтичних підходів, молекули, похідні від Cannabis sativa L., почали розглядатися як перспективні агенти для таргетного лікування складних поліетіологічних станів, таких як фармакорезистентна епілепсія, аутичні розлади спектру (РАС), нейродегенеративні захворювання та різні форми хронічного болю. Проте, попри успіхи CBD (канабідіолу) як першого офіційно визнаного терапевтичного агента, більшість інших канабіноїдів залишаються на периферії наукової розробки.
Новий фокус досліджень зміщується з вивчення головних канабіноїдів (Δ9-ТГК і CBD) на мінорні, маловивчені молекули, такі як каннабідіварін (CBDV), каннабідиварінова кислота (CBDVA) та ізомери типу Cannabielsoic Acid B (CBDA-B). Ці сполуки, відмінні за структурою та механізмами дії, обіцяють розширити існуючий фармакологічний інструментарій за рахунок взаємодії з альтернативними біологічними мішенями: транзиторними рецепторними потенціалами (TRP-каналами), PPAR-рецепторами, серотонінергічною системою. Такі взаємодії відкривають нові терапевтичні можливості, зокрема для модулювання нейровідновлювальних процесів, регуляції запальних каскадів та нейропротекції.
Ключовим викликом залишається біотехнологічне виробництво рідкісних канабіноїдів у достатній кількості для досліджень і клінічного застосування. Традиційні методи екстракції вимагають великих масивів сировини і несуть ризик деградації кислотних форм молекул. Новітні підходи, такі як генетична модифікація Saccharomyces cerevisiae для біосинтезу канабіноїдів, уже сьогодні пропонують альтернативу аграрному виробництву, що може суттєво змінити баланс доступності цих речовин.
Одночасно виникає необхідність у перегляді методології препарування канабіноїдів: чистота субстанцій, визначення стереохімії, контроль стабільності у фармацевтичних формах. Без цих змін неможливо просунути маловідомі канабіноїди на рівень реальних лікарських засобів.
Хімічна структура та біогенез CBDV
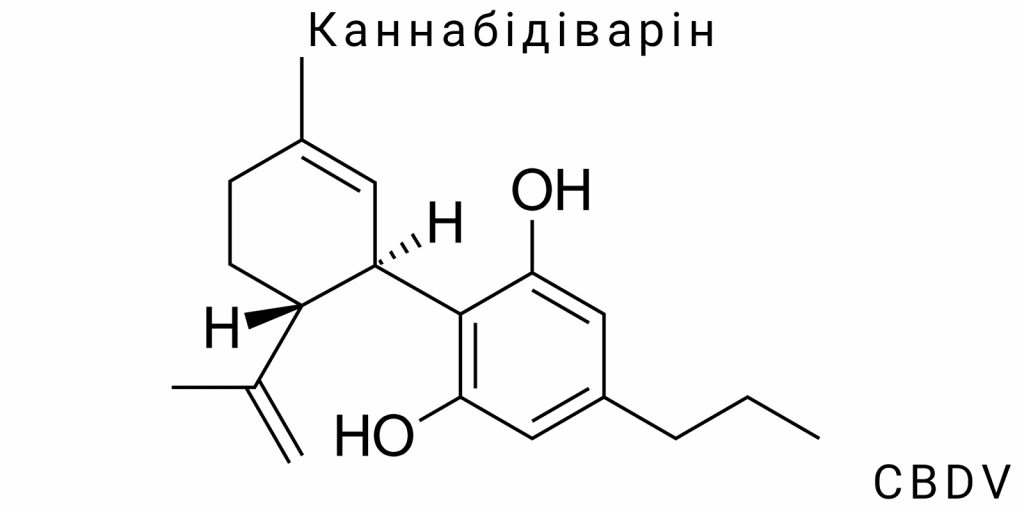
Хімічна структура каннабідіваріну
Каннабідіварін (CBDV) – це природна біоактивна сполука із групи фітоканабіноїдів, хімічна ідентичність якої обумовлена ключовою модифікацією алкільного ланцюга: присутністю трикарбонового (пропільного) радикалу замість звичного для канабідіолу п’ятикарбонового (пентильного). Ця заміна формує відмінну хімічну мікрооточення молекули і визначає її унікальні властивості взаємодії з біологічними мішенями.
Молекулярна формула каннабідіваріну – C₁₉H₂₆O₂, молекулярна маса – 286,41 г/моль. Основу структури становить ароматичне бензольне кільце, на якому у позиціях 1 і 3 локалізуються гідроксильні групи (–OH), що забезпечують полярні характеристики молекули і її здатність до утворення водневих зв’язків у біологічних середовищах.
Циклічна частина молекули представлена модифікованим монотерпеновим фрагментом (цикло-гексеновий кістяк), з’єднаним з бензольним кільцем через кон’юговану систему подвійних зв’язків. Особливу увагу заслуговує ізопренова частина, що включає подвійний зв’язок у проп-1-ен-2-ільній групі, орієнтованій просторово таким чином, щоб мінімізувати стеричні перешкоди та оптимізувати взаємодію із рецепторними структурами.
Рентгеноструктурний аналіз кристалів CBDV продемонстрував стабільну сателітну упаковку молекул через інтермолекулярні водневі зв’язки між гідроксильними групами сусідніх молекул. Така архітектоніка може пояснювати відносно високу стабільність CBDV у твердому стані порівняно з деякими іншими канабіноїдами. Окрім цього, спостерігалося, що при фізіологічній температурі молекула зберігає специфічну напівплоску конформацію, що потенційно покращує її здатність до пасивної дифузії через клітинні мембрани.
Наявність коротшого пропільного ланцюга впливає на розподіл електронної густини вздовж молекули: спектроскопічні дослідження (NMR, FT-IR) показали зміщення характеристичних піків порівняно з CBD, зокрема в області зв’язків C–C і C–O, що вказує на змінену поляризацію молекули та її здатність до участі у нековалентних взаємодіях.
Електронні моделі (з використанням теорії функціоналу густини, DFT) підтверджують, що пропільна версія має знижений енергетичний бар’єр для обертання навколо деяких σ-зв’язків, що робить CBDV більш гнучким у динамічних біологічних середовищах (плазма, міжклітинна рідина) порівняно з жорсткішою структурою CBD.
Також важливо, що CBDV, маючи меншу молекулярну площу полярної поверхні (PSA) у порівнянні з CBD, демонструє поліпшену фармакокінетичну поведінку, зокрема в контексті абсорбції через кишковий епітелій.
Біосинтетичне походження каннабідіваріну
Формування основних прекурсорів
Біогенез каннабідіваріну (CBDV) базується на альтернативній метаболічній гілці класичного канабіноїдного шляху Cannabis sativa. Основним джерелом для синтезу канабіноїдів є полікеїдні сполуки, зокрема оліветолова кислота та її варинова форма. Для класичного шляху використовується гексаноїл-КоА, що призводить до утворення пентильних похідних. Натомість для варинової серії ключовим стартовим субстратом є бутирил-КоА. Ця відмінність визначає формування коротшого, пропільного бічного ланцюга у структурі кінцевих канабіноїдів.
Конденсація бутирил-КоА з трьома малоніл-КоА за участю специфічної полікеїдсинтази призводить до утворення варинової оліветолової кислоти. Подальша пренілазація гернілпірофосфатом за участю варіанту CBG-синтази формує канабігероваринову кислоту (CBGVA), яка є універсальним попередником для утворення як канабідіварінової кислоти (CBDVA), так і тетрагідроканабідіварінової кислоти (THCVA).
Специфічність синтаз та ферментативні особливості
Перетворення CBGVA у CBDVA каталізується ферментами, які є мутантними або варіативними версіями класичної CBDA-синтази. Ці синтази демонструють змінену просторову організацію активного центру, що забезпечує вищу спорідненість до коротколанцюгових субстратів. Структурні біологічні дослідження показали, що заміна всього декількох амінокислот у активному сайті може радикально змінити селективність ферменту на користь варинової серії.
Існують також дані про активність гібридних синтаз, здатних продукувати як пентильні, так і пропільні продукти в залежності від доступності субстрату в тканинах рослини. Ця пластичність ферментів дає можливість селекційним програмам створювати високовмістові сорти CBDV без потреби в генноінженерному втручанні.
Декарбоксилювання і стабільність CBDVA
CBDVA, що формується у рослинних тканинах, є нестабільною молекулою і підлягає декарбоксилюванню під впливом температури, світла або тривалого зберігання. Декарбоксилювання – це хімічна реакція елімінації карбоксильної групи у вигляді CO₂, яка перетворює CBDVA у активний CBDV.
Термін природного декарбоксилювання залежить від вологості, температури середовища та ступеня подрібнення біомаси: чим вища площа поверхні контакту з повітрям, тим швидше відбувається реакція. За лабораторними даними, при нагріванні рослинного матеріалу до 110–120°C декарбоксилювання CBDVA у CBDV відбувається з ефективністю понад 90% за 30 хвилин.
Генетичні та екологічні чинники
Генетична основа виробництва CBDV пов’язана з алельними варіаціями генів CBDA-синтази та CBG-синтази. Рослини з високим вмістом CBDV мають специфічні мутації, які забезпечують ефективнішу пренілазацію коротколанцюгових прекурсорів. Окремі популяції дикого канабісу з Азії (особливо з північного Таїланду та регіонів південного Китаю) демонструють природну селекцію на користь варинової біосинтетичної траєкторії.
Кліматичні умови значною мірою впливають на співвідношення пентильних і пропільних канабіноїдів. Дослідження показали, що підвищений рівень ультрафіолетового випромінювання (особливо UV-B) стимулює активність полікеїдного комплексу, збільшуючи концентрацію варинових сполук. Крім того, дефіцит азоту у ґрунті корелює зі збільшенням частки коротколанцюгових продуктів серед канабіноїдів.
Біотехнологічні перспективи
Глибоке розуміння біогенезу CBDV стало підґрунтям для розвитку біотехнологічних стратегій з оптимізації його виробництва. Генно-редаговані лінії Cannabis sativa, створені за допомогою CRISPR-Cas9 технологій, дозволяють індукувати надекспресію варин-специфічних синтаз. Альтернативним підходом є синтез CBDV у гетерологічних системах, таких як Saccharomyces cerevisiae або Escherichia coli, шляхом інтеграції генетичних конструкцій, що кодують ферменти повного біосинтетичного каскаду.
Перспективи для індустрії включають створення сортів канабісу, які продукують високі рівні CBDV за рахунок модифікації ферментних каскадів або шляхом оптимізації агротехнічних умов вирощування для стимулювання варинової гілки метаболізму.
Природні джерела: Роль генетичних мутацій у коноплі
Вплив генетичних мутацій на канабіноїдний профіль канабісу
Генетичні мутації відіграють ключову роль у формуванні канабіноїдного профілю Cannabis sativa. Вивчення геному канабісу та молекулярних механізмів синтезу канабіноїдів демонструє, що мутації в генах, які кодують канабіноідні синтази, визначають не лише видову різноманітність, а й можливість синтезувати різні класи канабіноїдів, включаючи варинові, як CBDV, що є основною метою цієї теми.
Генетичні модифікації і варіації у канабіноідних синтазах
Природні мутації, зокрема однонуклеотидні поліморфізми (SNP), здатні змінювати структуру активних сайтів ферментів, що синтезують канабіноіди. У канабідіваріновій серії важливими є мутації в генах CBDA-синтази та THCA-синтази, що дозволяють рослинам виробляти варіанти канабіноїдів з коротким пропільним бічним ланцюгом замість стандартного пентильного. Відмінності в цих генах призводять до створення різних класів канабіноїдів, здатних мати значно іншу біологічну активність.
Дослідження, проведене на канабісі різних сортів, показало, що мутації в активному центрі CBDA-синтази змінюють її ефективність при взаємодії з прекурсорами канабіноідів. У канабісу, що виробляє високі рівні CBDV, були виявлені специфічні мутації в генах, що відповідають за синтез канабідіварінової кислоти (CBDVA). Це свідчить про наявність специфічних алелей, які дають перевагу утворенню варинових канабіноїдів у порівнянні з традиційними пентильними формами, як CBD або THC.
Генетичні мутації в природних популяціях канабісу
Генетичні мутації, що призводять до збільшення вмісту CBDV, часто зустрічаються в природних популяціях канабісу, що ростуть в ізольованих чи екстремальних умовах. Для таких рослин характерно накопичення мутацій в генофондах, де є обмежене перехрестя з іншими популяціями. Це дозволяє таким мутаціям стати стабільними в локальних умовах. Наприклад, в районах Східної Азії та на південному заході США було зафіксовано високі рівні CBDV у дикорослих зразках канабісу, що є результатом локальних мутацій та адаптацій до кліматичних умов.
Для таких рослин характерно збереження варіацій у генах канабіноїдних синтаз, що передаються на наступні покоління. Ці варіації можуть бути результатом природного добору, що стимулює їх на виживання в умовах кліматичних стресів або навантаження патогенами. Наприклад, в гірських районах з високою інтенсивністю сонячного випромінювання канабіс із високим вмістом варинових канабіноїдів може мати більшу стійкість до ультрафіолетового опромінення та посухи.
Механізм еволюції канабіноїдного шляху
Еволюція канабіноїдного метаболічного шляху в рослинах канабісу є результатом тривалого процесу адаптації до змінюваних екологічних умов. Одним із механізмів адаптації є активація різних шляхів біосинтезу канабіноїдів. Наприклад, у рослинах, які ростуть в екстремальних умовах, може відбуватися активація варіантів генів, що приводять до переважного синтезу варинових канабіноїдів (як CBDV), що забезпечує стійкість до стресових факторів.
Дослідження фітоканабіноїдної системи канабісу, проведені за допомогою філогенетичних методів, показали, що такі адаптивні мутації є результатом тривалого тиску навколишнього середовища. Наприклад, в деяких районах з високою активністю ультрафіолетового випромінювання канабіс з вариновими канабіноїдами має значно менше ушкоджень від UV-B, оскільки варинові канабіноїди можуть мати більш потужну антиоксидантну активність.
Селекція та модифікація канабіноідних шляхи
Селекційні програми, орієнтовані на створення сортів канабісу з високим вмістом CBDV, використовують як природні мутації, так і методи генної інженерії. Завдяки точковим мутаціям в генах синтаз канабіноїдів можна створити рослини з бажаним профілем канабіноїдів без використання хімічних реагентів або синтетичних процесів. Однак такі технології потребують ретельного моніторингу і вивчення потенційних екологічних і еволюційних наслідків.
Одним з перспективних напрямків є створення генно модифікованих рослин канабісу, в яких використовуються специфічні генетичні варіанти канабіноідних синтаз для підвищення концентрації варинових канабіноїдів. Випробування таких рослин у лабораторних умовах показали значне підвищення ефективності виробництва CBDV при оптимізації ферментативних шляхів. Також такі сорти канабісу мають потенціал для вирощування в регіонах з важкими агрокліматичними умовами.
Таким чином, селекція канабісу для підвищення вмісту CBDV представляє інноваційну стратегію, що базується на генетичних модифікаціях, які можуть мати значення як для фармацевтичної, так і для сільськогосподарської промисловості. Враховуючи особливості регулювання метаболічних шляхів у рослинах, такі генетичні підходи можуть бути застосовані для розробки нових сортів канабісу з покращеними властивостями та вищою стійкістю до стресів.
Методи отримання каннабідіваріну: від класичних до біотехнологічних підходів
Отримання каннабідіваріну (CBDV) та інших канабіноїдів може бути здійснено різними методами, включаючи класичні способи екстракції з рослинних матеріалів та більш новаторські біотехнологічні підходи. Вибір методу залежить від багатьох факторів: цільового результату, варіацій у складі канабіноїдів, економічної доцільності та законодавчих обмежень. Розглянемо основні підходи до отримання CBDV, починаючи з традиційних методів і закінчуючи сучасними біотехнологічними рішеннями, які обіцяють значно більш ефективні результати в майбутньому.
Класичні методи екстракції CBDV
Традиційні методи отримання CBDV здебільшого залежать від екстракції канабіноїдів з рослинних матеріалів. Оскільки CBDV присутній у низьких концентраціях в рослинах канабісу, то екстракція часто включає декілька етапів очищення та концентрації.
Екстракція за допомогою розчинників
Один із найбільш поширених способів – це екстракція з використанням органічних розчинників, таких як етанол, бутан чи CO₂ (в рідкому стані). Метод за допомогою органічних розчинників є простим і доступним, але вимагає додаткового очищення для видалення слідів розчинників. У деяких випадках це може призвести до утворення токсичних залишків, тому важливо використовувати методи очищення, які забезпечують безпеку продукту.
При екстракції етанолом рослини подрібнюються і заливаються етаноловим розчином, після чого суміш нагрівають для випаровування розчинника, залишаючи концентрат канабіноїдів, включаючи CBDV. Це дозволяє виділити зразки високої концентрації канабіноїдів, але потребує подальших кроків для відділення небажаних речовин, таких як хлорофіл та воски.
Суперкритична CO₂ екстракція
Суперкритична CO₂ екстракція є більш складним, але більш ефективним методом для отримання чистих канабіноїдів, включаючи CBDV. У цьому процесі використовуються надкритичні умови (температура і тиск), що дозволяють CO₂ діяти як розчинник, при цьому він не залишає токсичних залишків. Це особливо важливо, оскільки метод дозволяє отримати канабіноїди високої чистоти, з мінімальними втратами активних компонентів, а також зберігаючи їх біологічну активність.
Цей метод широко використовується в фармацевтичній та косметичній індустрії для отримання високоякісних екстрактів. Однак його висока вартість і складність реалізації робить його менш доступним для малих виробників.
Парова дистиляція
Метод парової дистиляції є старим і добре відомим способом, використовуваним для очищення ефірних масел. У контексті канабісу він дозволяє виділити канабіноїди шляхом прогрівання рослинного матеріалу до температури, що сприяє випаровуванню активних компонентів. Вакуумна дистиляція може застосовуватися для зниження температури випаровування та запобігання розкладу термолабільних речовин, таких як CBDV. Хоча цей метод є достатньо ефективним, він вимагає точного контролю температури та оптимальних умов для отримання високоякісного кінцевого продукту.
Тверда фаза екстракції (SPE)
Метод твердофазної екстракції (SPE) дозволяє зменшити кількість органічних розчинників, необхідних для екстракції. За допомогою цього методу можна концентрувати канабіноїди на твердій фазі і потім використовувати відповідні елюенти для їх вилучення. В основному цей метод застосовується для розділення та очищення канабіноїдів після основної екстракції.
Біотехнологічні методи отримання CBDV
У результаті прогресу в галузі біотехнологій з’явилися нові методи отримання CBDV, які значно зменшують витрати та покращують якість кінцевого продукту.
Генетична інженерія та мікробіологічні підходи
Один із найбільш перспективних шляхів отримання CBDV – це використання генної інженерії для введення генів канабіноїдних синтаз у мікроорганізми. Застосування бактерій та дріжджів для синтезу канабіноїдів вже активно досліджується в рамках синтетичної біології. Для цього дослідники впроваджують гени, що кодують канабіноідні синтази (CBDV-синтазу, CBGVA-синтазу), до геному дріжджів або бактерій. В результаті ці мікроорганізми здатні ефективно синтезувати CBDV в лабораторних умовах.
Цей підхід має значні переваги: зниження вартості виробництва, можливість контролювати умови синтезу і мінімізувати вплив на навколишнє середовище. Сучасні розробки також передбачають можливість масштабування цього методу, що відкриває можливості для масового виробництва CBDV у фармацевтичних цілях.
Клеточне ферментування
Ще одним підходом є використання клітинних культур рослин канабісу для отримання CBDV. У цьому випадку використовуються клітинні культури, які можна стимулювати для вироблення певних канабіноїдів. Відомо, що клітини канабісу можуть синтезувати CBDV, коли їх обробляють специфічними ферментами або умовами росту, що стимулюють вариновий шлях біосинтезу.
Цей метод дозволяє ефективно вирощувати канабіноіди в контрольованих умовах без необхідності вирощування цілих рослин, що є більш економічно доцільним для великих виробників. Більше того, цей метод дозволяє значно знизити рівень токсичних компонентів, що можуть потрапити до кінцевого продукту.
Синтетичний біосинтез
Один з найбільш революційних підходів до отримання CBDV – це повністю синтетичний біосинтез через використання складних біохімічних реакцій. У цьому випадку штучно створюються передумови для перетворення попередників канабіноідів у CBDV шляхом використання спеціальних ферментів, що каталізують ці реакції. Технології синтетичного біосинтезу стають все більш популярними через можливість отримувати канабіноїди в чистому вигляді без необхідності екстракції з рослин.
Синтетичні методи дозволяють повністю контролювати склад канабіноїдів, що виробляються, і при цьому знизити негативний вплив на екологію, оскільки не потрібно вирощувати великі площі канабісу. Однак цей метод також вимагає значних інвестицій у розвиток технологій та оптимізацію процесів.
Фармакологічні механізми дії CBDV через TRP-канали
Каннабідіварін (CBDV) належить до класу канабіноїдів, що проявляють широкий спектр фармакологічної активності, зокрема через взаємодію з транс’ємними потенціальними (TRP) каналами. TRP-канали являють собою групу іонних каналів, які грають вирішальну роль у ряді фізіологічних функцій організму, зокрема в сенсорному сприйнятті болю, температури, механічних подразників, а також у запальних і терморегуляторних процесах. Дослідження взаємодії CBDV з TRP-каналами дозволяє краще зрозуміти його механізм дії та з’ясувати, як цей канабіноїд може бути використаний для лікування ряду захворювань, що пов’язані з болем, запаленням і температурними дисфункціями.
TRP-канали мають величезну різноманітність в контексті функціональних характеристик. Вони можуть відкриватися або закриватися в залежності від зовнішніх або внутрішніх стимулів, таких як температура, механічний тиск, хімічні речовини або зміни в електричному потенціалі клітинної мембрани. Ці канали забезпечують основу для сенсорних відчуттів, таких як біль, температура та дотик, і відіграють важливу роль у відчуттях та рефлексах. Вони також беруть участь у регуляції іонного балансу в клітинах і органах, а тому мають ключове значення в цілісності гомеостазу організму. Важливо, що певні підтипи TRP-каналів асоціюються з різними патогенетичними механізмами, зокрема болем і запаленням.
Особливу роль серед TRP-каналів відіграють канали TRPV1, TRPV2, TRPA1 і TRPM8, які беруть участь у процесах, що стосуються як болю, так і механізмів терморегуляції. CBDV виявляє здатність модуляторно впливати на ці канали, що відкриває нові можливості для його використання в терапії низки захворювань.
TRPV1 (Transient Receptor Potential Vanilloid 1) є, ймовірно, найвідомішим серед TRP-каналів і бере участь у сприйнятті тепла та болю. Він активується при підвищенні температури або при хімічному подразненні, зокрема, за рахунок молекул, таких як капсаїцин. Активація цього каналу сприяє випуску нейропептидів, зокрема субстанції P, які індукують запалення і болючі відчуття. CBDV може мати інгібуючий ефект на TRPV1, зменшуючи болючі відчуття та знижуючи рівень запалення. Це особливо важливо для лікування хронічного болю, який часто пов’язаний з нейропатією та запальними захворюваннями.
Взаємодія CBDV з TRPV1: інгібування запальних процесів
TRPV1 (Transient Receptor Potential Vanilloid 1) є важливим мішенем для багатьох терапевтичних підходів, що стосуються запалення і болю. Це канал, який здатен активуватися не лише під впливом температури, але й хімічними речовинами, такими як капсаїцин. Активуючи TRPV1, ці подразники сприяють вивільненню молекул, які активують механізми болю і запалення, таких як субстанція P. У результаті цього процесу збільшується проникність клітинних мембран для кальцію, що спричиняє підвищення рівня кальцію в клітинах і, як наслідок, активацію різноманітних запальних сигналів.
CBDV взаємодіє з TRPV1 шляхом інгібування надмірної активації цього каналу. Його здатність модуляції активності TRPV1 дозволяє зменшити активацію субстанції P і інших запальних молекул, що знижує інтенсивність болю і обмежує прогресування запальних процесів. Це дуже важливо для лікування хронічного болю, який часто є наслідком захворювань, таких як артрит, фіброміалгія та травми нервової системи. Дослідження показали, що при хронічному болю рівень активації TRPV1 може бути значно підвищений, що погіршує стан пацієнтів. Взаємодія CBDV з цим каналом може допомогти знижувати чутливість до болю і, таким чином, зменшувати потребу в знеболювальних препаратах, які можуть мати серйозні побічні ефекти.
Вивчення впливу CBDV на TRPV1 є важливим етапом для розвитку нових терапевтичних стратегій у лікуванні болю, зокрема в контексті хронічних і запальних розладів, де традиційні методи лікування, як правило, не дають бажаних результатів.
Вплив на TRPV2: модуляція клітинної проліферації та регенерації
TRPV2 (Transient Receptor Potential Vanilloid 2) відіграє важливу роль в регуляції клітинних функцій, включаючи клітинну проліферацію, іонний транспорт і механічну чутливість клітин. Зв’язок між TRPV2 і клітинною активністю є ключовим для нормального функціонування організму, особливо в контексті тканинної регенерації та відновлення після травм.
CBDV здатний взаємодіяти з TRPV2, змінюючи його активність і тим самим регулюючи потоки кальцію в клітинах. Активуючи TRPV2, можна сприяти підвищенню кальцієвих потоків, що часто призводить до негативних наслідків для клітини, таких як оксидативний стрес або навіть апоптоз. Взаємодія CBDV з TRPV2 дозволяє знижувати цей ефект і забезпечувати стабільність клітинного стану, що важливо для запобігання розвитку запальних і дегенеративних захворювань.
Особливо важливим є вплив CBDV на TRPV2 в контексті нейродегенеративних захворювань. У таких станах, як хвороба Альцгеймера, Паркінсона та інші форми нейродегенерації, клітини мозку зазнають ушкоджень через порушення кальцієвих потоків. CBDV може допомогти стабілізувати ці процеси і таким чином знижувати ступінь ушкодження клітин, а також сприяти їх відновленню.
Крім того, CBDV може мати терапевтичний потенціал при онкологічних захворюваннях. Здатність TRPV2 активувати антиапоптозні механізми може сприяти росту клітин і розвитку пухлин, тому регулювання цього процесу через CBDV може стати важливою стратегією в боротьбі з раковими захворюваннями. Модулювання TRPV2 дозволяє інгібувати ці антиапоптозні шляхи, що може запобігти прогресуванню ракових клітин і зменшити ризик метастазування.
Загалом, взаємодія CBDV з TRPV2 відкриває нові можливості в лікуванні різноманітних захворювань, зокрема нейродегенеративних і онкологічних, де зміни в клітинній активності відіграють ключову роль у розвитку патології.
Взаємодія з TRPM8: ефект охолодження
TRPM8 (Transient Receptor Potential Melastatin 8) є рецептором, що має ключову роль у сприйнятті холодових подразників і створенні відчуття охолодження. Цей канал активується за допомогою ментолових сполук та інших охолоджуючих агентів, таких як евкаліпт або ксиліт. Активація TRPM8 не лише впливає на сприйняття температури, але й регулює процеси, пов’язані з болем, зокрема, при запаленнях і нейропатіях. Взаємодія каннабідіваріну (CBDV) з TRPM8 розширює можливості лікування таких захворювань, які супроводжуються порушеннями температурної чутливості, такими як дисфункції терморегуляції або хронічні болі, зокрема, у пацієнтів із нейропатією.
CBDV має здатність регулювати активність TRPM8, сприяючи полегшенню болю, який виникає в результаті патологічних температурних відчуттів. Наприклад, у хворих на нейропатії часто спостерігається відчуття “крижаних” або “пекучих” болів, які можуть бути знижені через активацію TRPM8 каналу. Таким чином, CBDV здатен створювати охолоджувальний ефект, який має терапевтичну користь при лікуванні захворювань, де біль пов’язаний з аномальними температурними відчуттями. Дослідження вказують, що активація TRPM8 може не лише зменшити неприємні відчуття, але й знижувати рівень запалення в тканинах, оскільки активація цього каналу також впливає на зменшення викиду прозапальних молекул, таких як цитокіни.
Цей ефект особливо важливий для пацієнтів, які страждають від хронічного болю, в тому числі від болю, що виникає після травм або при хронічних захворюваннях, таких як остеоартрит, фіброміалгія, або при порушеннях функцій терморегуляції. Взаємодія CBDV з TRPM8 відкриває нові можливості для розробки більш ефективних знеболювальних препаратів для пацієнтів, яким важко управляти болем за допомогою традиційних знеболювальних засобів. Ці препарати можуть бути менш агресивними, ніж опіоїди або нестероїдні протизапальні засоби, але при цьому забезпечувати стабільне зменшення болю та запалення.
Завдяки здатності знижувати температуру в патологічних вогнищах, CBDV може використовуватися для полегшення таких симптомів, як свербіж або дискомфорт, що виникають при дерматологічних станах або невропатичних розладах. Це дає нові можливості для лікування болів, пов’язаних з порушеннями температурної чутливості, таких як при синдромі Рейно або після операцій, що супроводжуються зміною нормальної терморегуляції.
Механізми впливу на запалення та біль
CBDV активно впливає на кілька типів TRP-каналів, зокрема на TRPV1, TRPV2, TRPA1 та TRPM8, що дозволяє йому гнучко модулювати різні аспекти запалення і болю. У випадку з TRPV1 каналом, який є основним рецептором для сприйняття болю, CBDV допомагає знизити чутливість до болю, пригнічуючи надмірну активацію цього каналу, що особливо важливо при хронічних запальних захворюваннях, таких як артрит. Через інгібування TRPV1, CBDV допомагає зменшити викид прозапальних нейропептидів, таких як субстанція P, що активно сприяють розвитку болю.
Дослідження також показують, що CBDV здатен модуляторно впливати на TRPV2, що має важливе значення для лікування нейродегенеративних захворювань, таких як хвороба Паркінсона або Альцгеймера. Активність цього каналу може сприяти надмірному накопиченню кальцію в клітинах, що веде до їх пошкодження і смерті. CBDV допомагає уникнути цього, знижуючи кальцієвий потік, що має важливе значення для попередження клітинного пошкодження, яке призводить до хронічних запальних процесів і нейродегенерації.
Що стосується TRPA1, то його активація сприяє розвитку запалення, зокрема внаслідок хімічних подразників, таких як акролеїн, що може викликати біль і набряки при травмах або при хронічних захворюваннях. CBDV, інгібуючи TRPA1, допомагає знижувати біль, що викликаний хімічними подразниками, і полегшує лікування запальних станів, таких як артрит, мігрень та різні форми нейропатії.
Усі ці механізми взаємодії CBDV з TRP-каналами створюють основу для розробки нових терапевтичних підходів у лікуванні різноманітних форм болю і запалення. Модулювання активності цих каналів дозволяє лікувати не тільки біль, а й запальні процеси, що виникають у зв’язку з травмами, хронічними хворобами або навіть при деяких аутоімунних розладах. Систематичне застосування CBDV може привести до покращення якості життя пацієнтів, оскільки дозволяє більш точно та ефективно регулювати больові відчуття, що виникають при різних патогенетичних процесах.
Клінічні дослідження: Фокус на рідкісних захворюваннях
Клінічні дослідження CBDV при епілепсії
Епілепсія є одним із найбільш поширених неврологічних розладів, який характеризується повторюваними епілептичними припадками, що виникають через аномальну електричну активність у мозку. Для багатьох пацієнтів з епілепсією стандартні антиепілептичні препарати не завжди дають бажаний ефект, особливо при лікуванні рідкісних або резистентних форм епілепсії, таких як синдром Драве або синдром Леннокса-Гасто. В цих випадках каннабіноїди, зокрема каннабідіварін (CBDV), привертають все більше уваги через свої потенційні терапевтичні властивості.
CBDV продемонстрував обнадійливі результати в клінічних дослідженнях, зокрема в лікуванні форм епілепсії, що не піддаються традиційному лікуванню. Одним з найбільш значущих досліджень є клінічне випробування, яке було проведено на пацієнтах із синдромом Драве. У цьому дослідженні було показано, що CBDV здатен знижувати частоту нападів у пацієнтів, у яких традиційні препарати не дають бажаного результату. Серед механізмів, через які CBDV може бути ефективним, є вплив на глутаматні рецептори та іонні канали, що сприяє стабілізації нейрональної активності та зменшує схильність до судом.
Важливим аспектом є здатність CBDV знижувати гіперактивність нейронів, що є основною причиною епілептичних нападів. У зв’язку з цим, дослідження показали, що CBDV може допомогти в регуляції нейропластичності та зменшити надмірну збудливість нейронів. Це робить CBDV перспективним засобом для лікування як типових, так і рідкісних форм епілепсії, які стійкі до стандартних терапевтичних методів.
Завдяки своїм властивостям, CBDV також є важливим інструментом в лікуванні педіатричних пацієнтів. Діти, які страждають від форм епілепсії, що не піддаються звичайному лікуванню, можуть отримати значну користь від застосування CBDV, оскільки він має менше побічних ефектів у порівнянні з традиційними антиепілептичними препаратами, такими як фенобарбітал або фенітоїн. Одним із ключових аспектів є можливість контролювати симптоми без необхідності в агресивній фармакологічній терапії, що дає можливість зберегти якість життя дітей.
Клінічні дослідження також відзначають, що CBDV має обмежену токсичність навіть при тривалому застосуванні. Це робить його перспективним кандидатом для використання в якості довгострокової терапії при епілепсії, зокрема в поєднанні з іншими антиепілептичними засобами.
CBDV при розладах аутистичного спектру (РАС)
Розлади аутистичного спектру (РАС) є групою неврологічних захворювань, що характеризуються порушенням соціальної взаємодії, комунікації та обмеженою репертуарністю поведінки. Лікування РАС є складним і часто включає в себе комбінацію медикаментозної терапії та терапевтичних втручань, таких як поведінкова терапія. Однак дослідження показують, що каннабідіварін (CBDV) має великий потенціал у полегшенні симптомів, пов’язаних з РАС, і може бути важливим інструментом у терапії цього розладу.
Дослідження на тваринах показали, що CBDV має здатність змінювати функцію нейрональних мереж, що сприяє покращенню соціальної поведінки та зниженню симптомів, таких як стереотипні рухи та поведінкові розлади, що часто спостерігаються у пацієнтів з аутизмом. На основі цих результатів було ініційовано ряд клінічних випробувань на людях, де було досліджено застосування CBDV у дітей з РАС.
Один з основних механізмів, через який CBDV може полегшити симптоми РАС, полягає у його здатності впливати на нейропластичність та синаптичні зв’язки. Цей канабіноїд має потенціал для регулювання нейротрансмісії в мозку, що може зменшити агресивну поведінку і підвищити здатність до соціальної взаємодії у пацієнтів з аутизмом. Дослідження показали, що CBDV має здатність знижувати рівень тривожності та покращувати когнітивні функції у пацієнтів, що є важливим аспектом при лікуванні аутизму.
Відомо, що пацієнти з РАС часто мають супутні порушення, такі як епілепсія або гіперактивність, для яких CBDV може бути ефективним засобом. Дослідження підтверджують, що CBDV має значний терапевтичний ефект при лікуванні судом, знижуючи їх частоту у пацієнтів з аутизмом, що страждають від цього супутнього симптома.
Важливим є те, що CBDV не викликає значних побічних ефектів і не має психоактивних властивостей, що робить його безпечним для використання в дітей, а також при тривалому лікуванні. Завдяки своїй високій безпеці та потенціалу зменшення симптомів, таких як стереотипна поведінка, тривожність, агресивні вчинки і навіть судоми, CBDV може стати важливим компонентом комплексного лікування РАС, зокрема, коли традиційні методи лікування не дають бажаного результату.
Клінічні дослідження, які продовжуються, зокрема дослідження, спрямовані на вивчення дозування та довгострокових ефектів, будуть визначати подальші можливості для застосування CBDV при розладах аутистичного спектру. Однак уже зараз можна зробити висновок, що CBDV має потенціал стати важливим інструментом в терапії аутизму, значно покращуючи якість життя пацієнтів з РАС і їхніх сімей.
Перспективи регуляторного статусу CBDV
Потенційний регуляторний статус CBDV на міжнародному рівні
Прогрес у розумінні фармакологічних властивостей каннабідіваріну (CBDV) та його перспективи в числі ряду серйозних захворювань, таких як епілепсія та розлади аутистичного спектру, сприяють все більшим зусиллям щодо встановлення регуляторного статусу цього з’єднання в різних країнах. Однак питання правового статусу CBDV все ще є предметом значних дискусій та варіюються в залежності від юрисдикції.
У Сполучених Штатах регуляція канабінодів знаходиться в процесі еволюції. У 2018 році Федеральне управління з контролю за продуктами і ліками (FDA) схвалило застосування препарату Epidiolex (який містить CBD) для лікування деяких форм епілепсії, зокрема синдрому Драве та Леннокса-Гасто. Це відкриття стало першим етапом у створенні юридичних рамок для каннабіноїдів, проте CBDV не отримає такого ж регуляторного статусу. Проте на сьогоднішній день кілька компаній вже завершили клінічні дослідження на основі CBDV для лікування спеціальних захворювань, що призвели до його втрати.
В Європейському Союзі ситуація є схожою. На рівні ЄС канабіноїди, такий ефект як CBD, регулюється в контексті продуктів, які не мають психоактивних речовин. Протест CBDV поки що знаходиться на стадіоні оцінки. Хоча деякі країни, наприклад Великобританія та Німеччина, вже дозволили використання каннабіноїдів для медичних цілей, регуляторні органи повинні досліджувати фармакологічні властивості CBDV та його медичні показання.
Одна з найбільших проблем, пов’язаних із регулюванням CBDV, виникає в тому, що канабідіварин походить з того самого джерела, що і THC та CBD – рослинні коноплі. Тому для багатьох країн регулювання CBDV стикається з юридичними перешкодами, пов’язаними із законодавчими обмеженнями щодо рослин канабісу. Проте позитивні результати клінічних досліджень та підвищення науково-допоміжних та медичних колів можуть сприяти зміні підходів до регулювання.
Виклики та майбутнє регуляторного статусу CBDV
Регуляторні органи, такі як FDA та EMA (Європейське агентство з лікарських засобів), стикаються з численними труднощами при визначенні чітких правил для каннабінодів, зокрема CBDV. Одним із головних викликів є показ стандартних і суворих критеріїв для оцінки безпеки та ефективності CBDV на рівнях глобальної медичної практики. Канабідіварін має бути остаточно вивчений на предмет деяких побічних ефектів, особливо при тривалому виробництві.
Не менше є розуміння того, як CBDV взаємодіє з іншими ліками, а також його довгострокова ефективність при лікуванні хронічних захворювань. Якщо ці питання будуть вирішені в позитивному ключі, це може стати основою для широкого застосування CBDV в медичній практиці.
Іншим аспектом є питання про стандартизацію процесу виробництва CBDV. Враховуючи, що цей канабіноїд міститься в певних сортах коноплі, забезпечення чистоти та точності складу продукції є необхідними для забезпечення високої якості показників. Можливість інноваційних ефективних методів екстракції та тестування CBDV вимагає значних інвестицій у технології та стандарти.
Крім того, багато країн мають розрізнені законодавчі норми щодо канабіноїдів, що створюють стійкість для глобального доступу до продуктів на основі CBDV. У деяких країнах, таких як Канада та Нідерланди, вже існує законодавство, яке дозволяє використовувати канабінодів для медичних цілей, і CBDV може бути доданий до цього списку в майбутньому. В інших країнах, таких як Китай чи Австралія, правовий статус каннабіноїдів залишається більш обмеженим, і процес прийняття нормативних актів може зайняти більше часу.
Враховуючи все вище зазначене, можна зробити висновок, що перспективи регуляторного статусу CBDV є дуже обнадійливими, однак на шляху до його широкого використання в медичній практиці є значні юридичні та наукові перешкоди. Більш глибоке розуміння фармакологічних властивостей CBDV, разом із розвитком клінічних досліджень, ймовірно, дозволить цій канабіній отримати більш чітке місце в законодавчих системах різних країн у найближчі роки.
Висновок
Каннабідіварін (CBDV) представляє собою значну наукову і терапевтичну цінність серед канабіноїдів завдяки своїм потенційним лікувальним властивостям, особливо в контексті рідкісних і складних захворювань, таких як епілепсія та розлади аутистичного спектру (РАС). Його механізм дії через взаємодію з транс’ємними потенціальними каналах (TRP-канали), зокрема TRPV1, TRPV2, TRPA1 та TRPM8, дозволяє знижувати болі, полегшувати запалення, а також коригувати терморегуляційні порушення. Ці властивості надають CBDV особливе значення у лікуванні таких станів, як хронічний біль, запальні захворювання та нейропатії.
Значним досягненням у розвитку CBDV є результати клінічних досліджень, які демонструють його ефективність в лікуванні рідкісних і складних захворювань. Зокрема, у пацієнтів з епілепсією, особливо в дитячому віці, відзначається зниження частоти судомних нападів, а у пацієнтів з розладами аутистичного спектру – покращення поведінкових реакцій і соціальних навичок. Терапевтичний ефект CBDV є результатом його здатності модуляторно впливати на нервову систему, знижуючи гіперактивність нейропептидів і покращуючи функціонування нейронів.
Проте, незважаючи на обнадійливі результати, наукове розуміння механізмів дії CBDV потребує подальших досліджень для забезпечення його безпеки і довгострокової ефективності. Зокрема, необхідні додаткові клінічні випробування для оцінки можливих побічних ефектів та оптимальних дозувань, а також для визначення тривалості його впливу на організм.
Щодо регуляторного статусу, CBDV знаходиться в стадії активного вивчення та оцінки в багатьох країнах. Хоча в деяких країнах уже розпочато схвалення канабіноїдів для медичних цілей, CBDV стикається з юридичними і нормативними перешкодами через своє походження з канабісу. Однак з огляду на зміни в законодавстві та зростаючий інтерес до терапевтичних властивостей канабіноїдів, можна очікувати, що в майбутньому CBDV стане більш доступним у медичних цілях.
Перспективи застосування CBDV у лікуванні рідкісних захворювань виглядають дуже обнадійливими, і цей канабіноїд має реальний потенціал для зміни підходів до лікування ряду складних і хронічних станів. Однак для його широкого застосування необхідні подальші наукові дослідження, а також гармонізація регуляторних норм, що дозволить забезпечити безпеку та ефективність застосування CBDV у медичній практиці.
У підсумку, CBDV може стати важливою складовою майбутньої терапевтичної практики, особливо в лікуванні тих захворювань, для яких сучасні методи лікування є недостатньо ефективними. Однак для повного розкриття його потенціалу потрібно ще провести ряд наукових досліджень і подолати існуючі юридичні бар’єри.
Джерела:
- National Institute on Drug Abuse (NIDA) – Канабіноїди та їх вплив на здоров’я, включаючи CBDV.
https://nida.nih.gov - PubMed Central (PMC) – Наукові статті, що стосуються фармакології каннабідіваріну та його клінічних застосувань, зокрема в контексті епілепсії та нейропатій.
https://pubmed.ncbi.nlm.nih.gov - World Health Organization (WHO) – Документація та дослідження щодо медичних застосувань канабіноїдів, в тому числі CBDV, для лікування різних захворювань.
https://www.who.int - Journal of Clinical Investigation – Клінічні дослідження щодо використання каннабідіваріну у лікуванні рідкісних захворювань, таких як епілепсія та розлади аутистичного спектру.
https://www.jci.org - European Medicines Agency (EMA) – Документація щодо регуляторного статусу канабіноїдів в Європі, включаючи CBDV.
https://www.ema.europa.eu - U.S. Food and Drug Administration (FDA) – Оцінка безпеки та ефективності канабіноїдів у медичних цілях, зокрема каннабідіваріну.
https://www.fda.gov - Cannabis and Cannabinoid Research Journal – Наукові дослідження і огляди, що вивчають ефекти каннабідіваріну на різні біологічні системи.
https://www.liebertpub.com/can - British Journal of Pharmacology – Дослідження механізмів дії канабіноїдів і їх потенційні терапевтичні ефекти.
https://bpspubs.onlinelibrary.wiley.com/journal/14765381