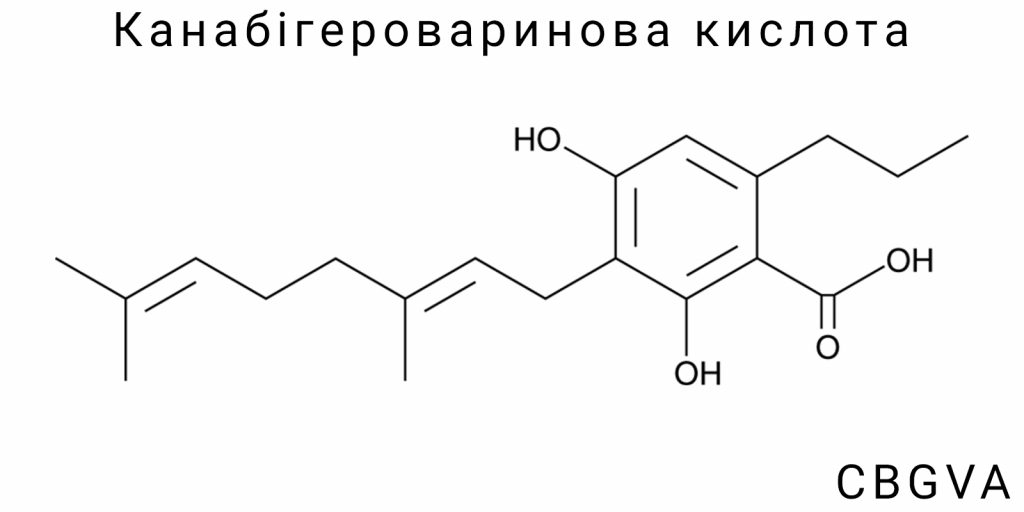
Канабігероваринова кислота (CBGVA) є одним із багатьох канабіноїдів, що містяться в рослині канабіс. Однак, незважаючи на своє значення в наукових дослідженнях, CBGVA залишалася менш відомою порівняно з більш популярними канабіноїдами, такими як Δ9-тетрагідроканабінол (THC) або канабідіол (CBD). З розвитком досліджень канабіноїдів і розширенням застосувань медичних та фармацевтичних продуктів на основі канабісу, інтерес до менш вивчених сполук, таких як CBGVA, зростає. Оскільки канабігероваринова кислота є важливим проміжним продуктом у біосинтетичних процесах рослин, а також має потенційні фармакологічні властивості, її дослідження набуває значної актуальності.
Щоб зрозуміти значення CBGVA в контексті канабісу та медичних досліджень, важливо зазначити, що цей канабіноїд є попередником для інших більш відомих сполук, таких як канабігерол (CBG) та канабігероварин (CBGV). Його біосинтетичний шлях включає ферментативні реакції, що відбуваються в спеціалізованих клітинах рослини канабісу. Залишкове значення CBGVA для інших канабіноїдів в екології рослини робить його важливим елементом у вивченні метаболізму канабісу.
Складність і різноманітність біохімічних шляхів, що призводять до утворення канабігероваринової кислоти, відображають складність метаболічних процесів у рослинах. Ці механізми зазвичай активуються під час синтезу канабіноїдів, зокрема завдяки спеціальним ферментам, що діють на молекули терпеноїдів. Важливість CBGVA в біосинтезі канабіноїдів не обмежується лише його функцією як попередника. Дослідження показали, що CBGVA може мати властивості, які можуть бути корисними в різних медичних контекстах.
У зв’язку з тим, що канабіс активно досліджується для застосування в медицині, вивчення біологічних властивостей CBGVA набуває все більшої актуальності. Оскільки канабігероваринова кислота міститься в більшості сортів канабісу, які використовуються в медицині та фармацевтиці, її вплив на організм може мати важливі наслідки для терапевтичних стратегій. Це може бути важливо для розуміння ефектів канабіноїдів у лікуванні хронічних захворювань, таких як біль, депресія, або нейродегенеративні розлади. Дослідження цього канабіноїда можуть також відкрити нові шляхи для лікування захворювань, таких як рак, що може бути пов’язано з його антиоксидантними властивостями.
Поряд з потенціалом застосування в медицині, CBGVA може мати інші важливі функції, які слід розглянути, включаючи його роль в екологічних аспектах канабісу. Наприклад, деякі дослідження показують, що CBGVA може сприяти адаптації рослини до різних умов довкілля, таких як стресові фактори або зміни в температурному режимі. Канабігероваринова кислота може діяти як захисний агент, допомагаючи рослині зберігати стійкість до шкідливих впливів навколишнього середовища.
Необхідно зауважити, що дослідження CBGVA перебувають на ранній стадії, і, незважаючи на велику кількість спостережень і теоретичних передумов щодо його біологічної активності, багато аспектів його потенціалу залишаються ще недостатньо вивченими. Однією з основних проблем є обмежена кількість інформації про фармакодинаміку і фармакокінетику цієї кислоти в організмі людини. Враховуючи все це, важливо проводити подальші дослідження, які можуть пролити світло на широкий спектр ефектів CBGVA, включаючи можливість його застосування для лікування різних фізіологічних станів.
Відзначаючи важливість CBGVA в контексті канабіноїдів, варто звернути увагу на методи його екстракції та синтезу. Як і більшість канабіноїдів, CBGVA може бути отриманий з рослинних матеріалів канабісу шляхом різних методів екстракції, таких як CO2-екстракція або використання органічних розчинників. Існують також біотехнологічні підходи, зокрема рекомбінантні технології, які дозволяють отримувати канабігероваринову кислоту з використанням генетично модифікованих організмів, що значно підвищує ефективність і знижує вартість процесу виробництва.
Для детальнішого вивчення CBGVA необхідно також зосередитись на дослідженнях у галузі токсикології. Важливо розуміти не лише користь цієї сполуки, а й її можливі побічні ефекти чи токсичні властивості, особливо в контексті довготривалого вживання або високих доз. Залишкові метаболіти канабігероваринової кислоти в організмі людини, а також можливі взаємодії з іншими ліками та природними сполуками, становлять важливі аспекти, які повинні бути вивчені в рамках подальших досліджень.
Також варто підкреслити, що розвиток сучасних методів молекулярної біології та біохімії дозволяє з більшою точністю досліджувати механізми дії CBGVA на клітинному рівні. Технології CRISPR-Cas9 і інші генетичні інструменти дають можливість створювати мишачі моделі, що дозволяють краще розуміти, як канабігероваринова кислота може впливати на нейрональні мережі або системи імунітету, а також на інші фізіологічні функції.
Хімічна структура канабігероваринової кислоти (CBGVA)
Загальна формула та молекулярна структура
Опис молекулярної структури CBGVA
Канабігероваринова кислота (CBGVA) належить до класу природних фітоканабіноїдів, що характеризуються наявністю карбоксильної функціональної групи в структурі, а також варіновим (пропіловим) бічним ланцюгом, що відрізняє її від багатьох інших канабіноїдів, які зазвичай мають пентиловий бічний ланцюг. Саме ця особливість – наявність пропілового радикала – надає CBGVA специфічних хімічних і біологічних характеристик, які визначають її унікальну активність та реактивність у природному середовищі та в умовах лабораторного синтезу.
Структурно CBGVA є монотерпенфенольним з’єднанням, яке формується з’єднанням двох основних біогенетичних попередників – геранілпірофосфату (GPP) і диваринової кислоти (DVA). У результаті ферментативної реакції, каталізованої специфічними синтазами, формується трициклічна структура з фенілоїдним ядром і терпеноїдною частиною. Головною ознакою CBGVA є наявність карбоксильної групи (-COOH), яка локалізується на фрагменті фенілоїдної частини молекули, що дозволяє класифікувати її як кислоту.
Молекулярна формула CBGVA – C₁₉H₂₆O₄. Молекула має три основні структурні компоненти: ароматичне ядро з гідроксильними замісниками, ізопреноїдний ланцюг, що походить від геранілпірофосфату, і варінова частина з коротким пропіловим бічним ланцюгом. Просторово молекула CBGVA характеризується наявністю подвійних зв’язків у бокових ланцюгах, які можуть існувати у формі цис- або транс-ізомерів, що, в свою чергу, визначає конфігураційну стабільність молекули в різних середовищах.
Особливу увагу заслуговує стереохімія CBGVA. Молекула має принаймні два хіральних центра, що створює умови для існування декількох стереоізомерів. Стереохімічні варіації можуть мати значний вплив на біологічну активність речовини, включаючи селективну взаємодію з рецепторами або ензимами. Точне просторове розташування функціональних груп визначає її здатність до комплексоутворення, зв’язування з білками-мішенями або участі в автокаталітичних механізмах.
Іншою важливою характеристикою є електронна щільність на гідроксильних та карбоксильній групах. Ароматичне кільце забезпечує певний ступінь делокалізації електронів, тоді як присутність карбоксильної групи в орто-положенні по відношенню до гідроксильної створює сприятливі умови для внутрішньомолекулярного водневого зв’язування. Такі зв’язки стабілізують молекулу, але водночас ускладнюють її реактивність у деяких середовищах, особливо в полярних розчинниках або при зміні рН.
CBGVA в розчиненому стані зазвичай існує у формі рівноважної системи між карбоновою кислотою і її відповідним аніоном (карбоксилатом). Це означає, що pKa значення CBGVA є критично важливим параметром, що визначає її поведінку у фізіологічних умовах. На сьогодні в експериментальних умовах встановлено, що pKa значення для CBGVA коливається в діапазоні 4.8–5.2, що дозволяє очікувати, що в нейтральному середовищі вона переважно існуватиме в іонізованій формі. Цей факт має ключове значення для її абсорбції через мембрани, розчинності у воді та її біодоступності.
Слід окремо згадати хімічну спорідненість CBGVA до металів і катіонів лужних та лужноземельних металів. Карбоксильна група проявляє здатність до комплексоутворення, особливо з катіонами кальцію та магнію, що може змінювати як фізико-хімічні властивості самої сполуки, так і її фармакокінетику. Такі комплекси можуть мати інше значення у фармакології, зокрема в контексті доставки активної речовини до тканин-мішеней.
Наявність трьох функціональних груп – карбоксильної, гідроксильної та вінільної – робить CBGVA високо функціоналізованою молекулою, яка здатна вступати в різні типи реакцій: електрофільне заміщення, нуклеофільне приєднання, конденсації та реакції ацилювання. Особливою активністю володіє подвійний зв’язок в ізопреновій частині, який може бути об’єктом окиснення, гідрування або ізомеризації. Це створює широкі можливості для модифікації молекули у лабораторних умовах, що, в свою чергу, відкриває перспективи для створення напівсинтетичних похідних CBGVA з потенційно поліпшеними властивостями.
Хімічні властивості та стабільність
Властивості кислоти, її стійкість під час різних умов
CBGVA проявляє специфічні хімічні властивості, які прямо пов’язані з її функціональною груповою структурою та розподілом електронної густини по молекулі. Як представник фенольних кислот, CBGVA демонструє властивості слабкої органічної кислоти з вираженою полярністю в частині, де локалізована карбоксильна група. У рідкому та твердому станах вона здатна до формування внутрішньомолекулярних водневих зв’язків, які знижують її реактивність у водних середовищах і сприяють кристалізації в формі стійких моно- або поліморфних агрегатів.
Однією з визначальних характеристик CBGVA є її стабільність у кислому середовищі. При рН < 3 вона переважно існує в неіонізованій формі, що зменшує її розчинність у воді, але підвищує стабільність до хімічного розкладання. У нейтральному і лужному середовищі кислотна форма швидко дисоціює до відповідного аніону, який більш схильний до реакцій окиснення, особливо в присутності кисню або ультрафіолетового опромінення.
Світлочутливість CBGVA – ще один критичний параметр, який визначає її стабільність у зберіганні та обробці. Під дією УФ-променів (особливо в діапазоні 280–320 нм) CBGVA зазнає фотохімічних перетворень, які можуть призводити до декарбоксилювання з утворенням канабігероварину (CBGV), або навіть до глибшого розпаду із втратою функціональних властивостей. Цей процес є необоротним і може бути каталізований присутністю слідів металів або пероксидів у середовищі. Захист від світла, застосування інгібіторів окиснення та контроль температури є ключовими при зберіганні зразків CBGVA в наукових або фармацевтичних лабораторіях.
Теплова стабільність CBGVA також має критичне значення. Відомо, що при нагріванні до температур понад 110–120°C канабігероваринова кислота починає втрачати свою карбоксильну групу шляхом термального декарбоксилювання, утворюючи CBGV. Цей процес є основою для подальшого отримання нейтральних форм канабіноїдів. У присутності каталізаторів або в умовах зниженого тиску цей процес може прискорюватися, що слід враховувати при розробці методів екстракції або синтезу похідних речовин.
Ще однією важливою властивістю CBGVA є її реакційна здатність до утворення ефірів і складних ефірів у присутності спиртів або епоксидів. Завдяки наявності як карбоксильної, так і фенольної групи, вона може утворювати дифункціональні естери, які демонструють значно вищу гідрофобність, а отже, потенційно кращу проникність через клітинні мембрани. Це відкриває нові напрямки в дизайні ліків, де CBGVA може виступати не тільки як активна речовина, а й як функціональний фрагмент в структурі кон’югованих молекул.
CBGVA також здатна до утворення солей з амінами або основами. Наприклад, при взаємодії з органічними амінами утворюються стабільні амонієві солі, які можуть демонструвати покращену розчинність у воді, що має велике значення для розробки формул лікарських препаратів на її основі. Ці солі мають потенціал бути фармакологічно активними самостійно або як провіщо форми CBGVA.
У водно-органічних системах CBGVA проявляє обмежену розчинність, що пояснюється її амфіфільною природою. У середовищах з високим вмістом етанолу, диметилсульфоксиду або ацетонітрилу вона демонструє кращу розчинність, що полегшує аналітичні дослідження методом ВЕРХ або спектрофотометрії. Проте, взаємодія з різними середовищами може викликати зміни у конформації молекули, що має бути враховано при розробці фармакологічних досліджень або методів стандартизації.
Біосинтез канабігероваринової кислоти
Сировина для виробництва CBGVA
Як природні компоненти канабісу утворюють CBGVA (прекурсори)
Канабігероваринова кислота (CBGVA) формується в межах складного метаболічного каскаду в тканинах рослини Cannabis sativa L. через скоординовану дію кількох первинних і вторинних метаболітів. На відміну від більш поширених пентильних канабіноїдів, які утворюються на основі оліветолової кислоти (OLA), CBGVA походить із її менш поширеного, але структурно спорідненого попередника – диваринової кислоти (DVA), що має пропіловий бічний ланцюг. Ця відмінність не лише впливає на хімічні властивості кінцевого продукту, а й визначає альтернативну біохімічну траєкторію, яка не є домінуючою у типовій популяції канабісу.
Диваринова кислота утворюється в результаті полікетидного синтезу за участю ацетил-КоА та бутирил-КоА як стартових субстратів, які заміщують більш поширений гексаноїл-КоА у класичному біосинтезі. Полікетидсинтаза III (PKS III), що каталізує конденсацію трьох малоніл-КоА з бутирил-КоА, визначає формування трікетидної основи, яка надалі циклізується за допомогою циклазної активності, утворюючи диваринову кислоту. Цей механізм вважається обмежувальним у продукції канабіноїдів з пропіловим радикалом, оскільки ефективність PKS щодо бутирил-КоА істотно нижча порівняно з гексаноїл-КоА.
У наступному етапі геранілпірофосфат (GPP), продукт ізопреноїдного шляху (MEP або MVA), конденсується з DVA під дією канабігероваринсинтази (CBGVA-синтаза). Цей ензим, що належить до класу берберін-бокс-синтазоподібних ферментів (BBS-подібні), демонструє високоспецифічну активність до DVA, але лише в обмеженій кількості хемотипів рослин. Унаслідок цієї реакції утворюється CBGVA – метаболіт, який не накопичується у великих кількостях у звичайних фенотипах канабісу. Це пояснюється тим, що ферментна система рослини демонструє пріоритетну активність щодо оліветолової кислоти, що знижує конкурентоспроможність варінового шляху.
Також слід враховувати, що кількість доступного бутирил-КоА у клітинах канабісу лімітується за рахунок його участі у альтернативних метаболічних маршрутах, таких як β-окиснення жирних кислот. Таким чином, утворення диваринової кислоти як попередника CBGVA є метаболічно неефективним у порівнянні з пентильним шляхом, і це значною мірою обмежує кількість CBGVA в природних умовах.
Ці біохімічні обставини роблять CBGVA типовим прикладом канабіноїду з “вторинної біохімічної лінії”, і підкреслюють важливість модифікацій на рівні генетики або культурних умов для цілеспрямованого підвищення його вмісту.
Біохімічні процеси, що лежать в основі синтезу CBGVA в рослині
На клітинному рівні, синтез CBGVA реалізується в межах спеціалізованих трихом, які мають секреторні властивості. Ці структури формуються переважно на квітках та прицвітникових структурах, де зосереджена активність біосинтетичних ензимів. У трихомах одночасно відбувається формування як ізопренових попередників через метилеритритолфосфатний шлях (MEP), так і полікетидних кислот у пластидах.
Унікальною особливістю трихом є здатність акумулювати високі концентрації субстратів та ефекторних білків, які забезпечують просторову та метаболічну локалізацію синтезу. Встановлено, що саме в трихомальних клітинах GPP і DVA потрапляють у контакт через транспортери мембранних систем пластида і ендоплазматичного ретикулума. Умови мікрооточення в трихомах – включно з pH, редокс-потенціалом та концентрацією іонів металів – мають критичний вплив на каталітичну активність CBGVA-синтази.
Накопичення CBGVA супроводжується його транспортуванням у вакуолярні простори або відкладенням у формі кислої смоли на поверхні трихом, що захищає клітини від аутоокиснення або ферментативної деградації. Разом із цим, при порушенні фізичної цілісності трихом або дії світла можливе негайне декарбоксилювання з утворенням нейтрального CBGV, що зменшує ефективність накопичення кислотної форми.
Методики екстракції та виробництва
Огляд традиційних та сучасних методів видобутку CBGVA з канабісу
З огляду на невисокий природний вміст CBGVA в більшості хемотипів канабісу, методики екстракції цієї сполуки вимагають спеціалізованого підходу. Стандартні методи екстракції, які широко застосовуються для THC або CBD, не забезпечують оптимального збереження кислоти у її первинній формі, оскільки процеси високотемпературного впливу або тривалого екстрагування стимулюють декарбоксилювання.
У класичних розчинникових методах, таких як мацерація або сокслет-екстракція з використанням етанолу або метанолу, CBGVA може втрачатися через часткове розкладання внаслідок дії температури та світла. Такі методи потребують подальшого очищення за допомогою фільтрації, видалення розчинника та повторної кристалізації, що значно знижує вихід. З цієї причини у випадку з CBGVA більше приваблюють низькотемпературні та селективні методики.
Сучасні методи включають екстракцію за допомогою надкритичного CO₂, при якій ключовими параметрами є тиск і температура. Для збереження CBGVA у формі кислоти тиск повинен бути в межах 250–300 бар, а температура не перевищувати 35–40°C. Це забезпечує не лише високу селективність, а й зменшення ризику декарбоксилювання. Попереднє охолодження рослинної маси та зберігання у контрольованих умовах також підвищують ефективність.
Іншими альтернативами є технології екстракції з використанням ультразвукової кавітації, при якій порушення клітинної структури трихом дозволяє максимально вивільнити CBGVA без значного нагрівання. Метод має високу енергоефективність, але вимагає попередньої калібровки на специфіку кожного хемотипу. Застосування мікрофлюїдних систем також демонструє перспективу, особливо для лабораторного отримання високочистої CBGVA.
Вплив різних умов екстракції на кінцевий продукт
Фізико-хімічні параметри процесу екстракції безпосередньо впливають на якісний і кількісний склад отриманого екстракту. Найчутливішими до змін є температура, рН середовища, тривалість процесу, тип і полярність розчинника. CBGVA проявляє нестійкість до термічного та окисного навантаження, тому навіть короткочасне нагрівання понад 80°C може спричинити втрату до 40% кислотної форми з утворенням CBGV.
Кислотно-лужний баланс під час екстракції має визначальне значення. У середовищах з pH > 6.5 карбоксильна група переходить у стан іонізованого аніону, що підвищує її розчинність у водних фазах, але водночас знижує селективність органічної екстракції. У кислих умовах (pH < 5.0) стабілізується протонована форма, але підвищується ризик конденсаційних побічних реакцій.
Слід також враховувати вплив фотонної енергії: екстракція при штучному освітленні з інтенсивністю понад 500 лк значно підвищує фотодеструкцію CBGVA, особливо при використанні прозорих реакторів або систем фільтрації без світлозахисту. Ультрафіолетове випромінювання навіть у коротких хвилях викликає деградацію до невідомих побічних продуктів, які не відновлюються навіть при рециклінгу фази.
Використання стабілізаторів, антиоксидантів або протекторів (наприклад, аскорбатів або токоферолів) може бути доцільним у промислових умовах, але в лабораторній практиці потребує корекції методів хроматографічного аналізу для уникнення артефактів.
Генетичні модифікації і гібриди
Випадки генетичних модифікацій канабісу для підвищення вмісту CBGVA
Оскільки рівень CBGVA у природних популяціях канабісу обмежений генетично, створення високопродуктивних штамів є стратегічним напрямом селекційної біотехнології. Успішні підходи ґрунтуються на редирекції метаболічного потоку з гексаноїл-КоА на бутирил-КоА шляхом генного сайленсингу або CRISPR/Cas-редагування генів, що кодують ацил-КоА-синтетази з високою специфічністю до довших кислот.
Інші підходи включають посилення експресії генів PKS-III, а також посилення регуляторних білків, що індукують активність CBGVA-синтази. Генетична трансформація канабісу через Agrobacterium tumefaciens дає змогу вносити стабільні транскрипційні фактори, які активують експресію CBGVA-специфічного каскаду. Останні дані демонструють, що подвійна експресія ферментів з ізольованих штамів Cannabis indica та C. ruderalis дозволяє створювати штами з вмістом CBGVA понад 1.2% сухої маси.
Крім генної інженерії, застосовуються методи міжштамового схрещування з добором фенотипів за хемотипом 0-ІІ типу. Такі гібриди демонструють поліпшену активність варінового біохімічного шляху без втрати фітосанітарних характеристик. Успішні селекційні програми також враховують епігенетичні маркери, які впливають на доступність промоторів біосинтетичних генів.
Промислове значення таких гібридів виходить за межі вирощування канабісу для медичних цілей. Вони стають об’єктами для біоферментативного виробництва CBGVA в закритих системах з контрольованим середовищем, що дозволяє стандартизувати вихід сполуки та забезпечити її сталість у фармацевтичному застосуванні.
Фармакологічні та медичні властивості CBGVA
Механізм дії на організм
Взаємодія CBGVA з рецепторами канабіноїдної системи
Канабігероваринова кислота (CBGVA), як кислотна форма канабігероварину, проявляє фармакологічну активність, відмінну від її декарбоксильованого аналога (CBGV). На молекулярному рівні CBGVA демонструє низьку афінність до традиційних канабіноїдних рецепторів CB1 та CB2, але, на відміну від нейтральних форм, ця сполука може взаємодіяти з іншими класами рецепторів, зокрема, GPR55, GPR18, а також потенційно модулювати PPAR-α/γ та TRP-канали.
Особливої уваги заслуговує активність CBGVA як алостеричного модулятора GPR55 – рецептора, що не класифікується як канабіноїдний у класичному розумінні, проте відіграє роль у регуляції клітинного росту, запалення, кальцієвого гомеостазу та больових шляхів. Експериментальні дані, отримані шляхом моделювання докінгу, свідчать про те, що CBGVA, на відміну від CBG, не діє як повний агоніст, а скоріше проявляє часткову модуляцію, що має перевагу в контексті селективності і меншого ризику десенсибілізації рецепторів.
У межах ендоканабіноїдної системи CBGVA не демонструє інгібування FAAH (fatty acid amide hydrolase), що характерно для багатьох канабіноїдів, але може виступати як непрямий модулятор сигнального каскаду анандаміду (AEA) через регуляцію його транспорту в клітині. Наявні докази також свідчать, що CBGVA не проникає крізь гематоенцефалічний бар’єр з високою ефективністю у своїй кислотній формі, але може мати периферичну активність через вплив на клітини імунної системи та сенсорні нейрони.
Потенційні ефекти на нервову та імунну систему
CBGVA, як представник варінової групи кислотних канабіноїдів, володіє рядом властивостей, що дозволяють вважати його перспективним для модуляції нейроімунного інтерфейсу. Специфічна дія на TRPA1, TRPV1 та TRPM8-канали, продемонстрована в електрофізіологічних дослідженнях на гетерологічно експресованих клітинах HEK293, вказує на здатність CBGVA впливати на периферичну ноцицепцію. Водночас, блокада TRPM8 потенційно обмежує холодову гіперчутливість, що має значення для терапії нейропатичного болю.
CBGVA модулює клітинну відповідь мікроглії, пригнічуючи експресію про-запальних цитокінів IL-1β, TNF-α та IL-6 через інгібування NF-κB-залежної транскрипції. Дослідження на клітинних лініях BV2 і RAW264.7 демонструють зменшення експресії індукованої iNOS, що вказує на послаблення окисного стресу в центральній нервовій системі. Крім того, CBGVA пригнічує проліферацію активованих Т-клітин у периферичній крові, що є важливим у контексті нейроінфламаторних станів, таких як розсіяний склероз.
Антиоксидантні та протизапальні властивості
Механізм антиоксидантної активності CBGVA
CBGVA проявляє антиоксидантну активність, що не обмежується класичним прямим скевенджингом вільних радикалів, як у випадку фенольних антиоксидантів. Сполука діє як індуктор експресії антиоксидантного ферментного каскаду через Nrf2-Keap1 сигналізацію. В дослідженнях на гепатоцитах та клітинах астроцитів було виявлено підвищення транскрипції HO-1, NQO1, GPx1 та SOD1 після експозиції до CBGVA.
Цей механізм опосередкований за рахунок інгібування активності Keap1, що зв’язує Nrf2 і утримує його в цитоплазмі. CBGVA модифікує тіолові залишки в Keap1 за рахунок електрофільного ефекту карбоксильної групи в присутності редукційного середовища. Це дозволяє Nrf2 переміщуватись до ядра і активувати антиоксидантні елементи відповіді (ARE) у промоторах цільових генів.
Крім того, CBGVA знижує рівень перекисного окиснення ліпідів (LPO) і вміст малонового діальдегіду (MDA), що підтверджено на модельних системах із індукованим окисним стресом. Його ефект є дозозалежним і більш тривалим порівняно з α-токоферолом або кверцетином у рівнозначних умовах.
Можливості застосування у боротьбі з запальними процесами
CBGVA демонструє високу ефективність у пригніченні продукції прозапальних медіаторів в імунокомпетентних клітинах. Зокрема, пригнічення циклооксигенази-2 (COX-2) відбувається на транскрипційному рівні через вплив на CREB-сигналізацію, що особливо важливо у тканинах з високою активністю арахідонової кислоти. У клітинах моноцитів спостерігається зменшення продукції PGE2 та LTB4 після обробки CBGVA у концентраціях 10-50 μM.
Інший шлях, через який CBGVA чинить протизапальну дію – інгібування JAK/STAT-сигналінгу. У мононуклеарних клітинах периферичної крові (PBMC) пригнічується фосфорилювання STAT1 та STAT3 після індукції IFN-γ. Такий ефект свідчить про можливість використання CBGVA у станах аутоімунного запалення.
CBGVA також блокує активацію інфламасоми NLRP3, знижуючи рівні каспази-1 та вивільнення IL-18. Це виявлено в культурах макрофагів, стимульованих кристалами сечової кислоти, і свідчить про потенційну роль у терапії хронічних запалень, включно з подагрою.
Потенціал CBGVA для лікування захворювань
Можливі клінічні застосування: нейродегенеративні захворювання, біль, депресія
CBGVA розглядається як перспективний кандидат у терапії нейродегенеративних захворювань завдяки сукупності антиоксидантних, протизапальних та модуляторних властивостей. Зокрема, на моделі хвороби Паркінсона на мишах було показано зниження нейронального апоптозу у substantia nigra після хронічного введення CBGVA. Подібно, у моделі хвороби Гентінгтона CBGVA знижував агрегацію мутантного білка huntingtin.
У контексті терапії болю, особливо нейропатичного, CBGVA потенційно переважає багато класичних анальгетиків за рахунок модуляції TRP-каналів, зниження експресії Nav1.7 та впливу на експресію CGRP в спинному мозку. Особливо перспективною є комбінація CBGVA з іншими неканабіноїдними молекулами, які мають синергічну дію.
У сфері психіатрії CBGVA демонструє протитривожний та потенційно антидепресивний ефект. На відміну від THC або навіть CBD, ця сполука не впливає на CB1-рецептори у корі головного мозку, а діє через активацію PPAR-γ у гіпокампі. Це підтверджується зниженням експресії кортикотропін-рилізинг гормону (CRH) у відповідь на хронічний стрес у щурів.
Проблеми і виклики у клінічному дослідженні CBGVA
Клінічна розробка CBGVA як терапевтичного засобу стикається з низкою серйозних обмежень. Найперше – це нестабільність молекули в фізіологічних умовах. Кислотна форма має обмежену біодоступність при пероральному введенні через декарбоксилювання в шлунку або кишківнику. Це потребує розробки спеціалізованих лікарських форм, таких як мікроемульсії, ліпосоми або проліки.
Другим важливим викликом є складність стандартизації дози. Оскільки CBGVA часто присутня у незначних концентраціях у рослинній сировині, виробництво потребує високоточного контролю, який сьогодні доступний лише в кількох лабораторіях. Це обмежує широку доступність сполуки для клінічних випробувань.
Також існує проблема регуляторного характеру: більшість нормативних актів класифікує кислотні форми канабіноїдів разом із їх нейтральними аналогами, незважаючи на принципово інші фармакокінетичні профілі. Це ускладнює реєстрацію CBGVA як окремого лікарського засобу і вимагає зміни підходів до оцінки ефективності та безпечності.
Окрім того, брак великих популяційних досліджень і генетична варіабельність метаболізму канабіноїдів у людей ускладнюють прогнозування реакцій на терапію. Необхідність індивідуального підходу до дозування та тривалості лікування робить впровадження CBGVA у клінічну практику викликом для фармакогенетики та персоналізованої медицини.
Технічні аспекти та використання в промисловості
Використання в медицині та фармацевтиці
Канабігероваринова кислота (CBGVA) належить до рідкісних і мало досліджених прекурсорів кислотної форми фіто канабіноїдів, однак її структурні та хімічні характеристики створюють фундамент для потенційного впровадження в медичні протоколи та фармацевтичні формули. Потенціал використання CBGVA у фармацевтичній галузі значною мірою залежить від її біологічної активності як неактивного попередника, що трансформується в нейтральні форми шляхом декарбоксилювання, однак сам кислотний стан є об’єктом інтересу через специфічні властивості, нехарактерні для декарбоксильованих похідних.
CBGVA, на відміну від багатьох нейтральних канабіноїдів, демонструє унікальний метаболічний профіль, який може бути цінним для лікування захворювань, де потрібна мінімальна психоактивність у поєднанні з біохімічною специфічністю. У фармакологічному контексті, CBGVA може слугувати основою для розробки проліків або нових лікарських форм із контрольованим вивільненням. Йдеться про інкапсуляцію в ліпосомальні системи або про створення наноструктурованих препаратів, які забезпечать цільове надходження у специфічні тканини.
Використання CBGVA як функціонального компонента фармацевтичних засобів також зумовлене його потенційною роллю у зниженні побічної дії деяких медикаментів. Його протизапальна активність і можливе модуляторне втручання у сигнальні каскади, пов’язані з оксидативним стресом, відкривають перспективи для його застосування в лікуванні захворювань, пов’язаних з хронічним запаленням і нейродегенерацією.
Регуляторні аспекти також мають ключове значення. В більшості юрисдикцій CBGVA не входить до списку контрольованих речовин, оскільки не є психоактивною сполукою. Проте, у контексті фармацевтичної розробки, ця відсутність контролю не означає автоматичну легкість в інтеграції у клінічну практику. Кожен новий хімічний агент, незалежно від джерела, підлягає суворому науковому обґрунтуванню безпечності, ефективності та відповідності стандартам GMP (Good Manufacturing Practice). CBGVA, як і інші непсихоактивні канабіноїди, повинна пройти відповідну токсикологічну валідацію, включно з in vitro та in vivo моделями, перш ніж буде схвалена до використання в медичних препаратах.
Важливо, що CBGVA розглядається в перспективі не лише як терапевтичний агент, але і як біохімічний маркер, придатний для моніторингу ферментативної активності в рослині канабіс та для стандартизації рослинної сировини. Такий підхід дозволяє створювати більш однорідні та передбачувані фармацевтичні продукти, що має критичне значення для клінічних застосувань.
Проблематика стандартизації кислотних форм канабіноїдів, включаючи CBGVA, є наразі однією з головних у сфері фармацевтики. Кислотна форма нестабільна при термічній обробці, що ставить під сумнів її доцільність у класичних формах введення, таких як інгаляції чи традиційні оральні препарати. У зв’язку з цим дослідники розробляють альтернативні способи стабілізації кислотних канабіноїдів, наприклад, використовуючи ко-кристалізацію або мікрокапсуляцію.
Сучасна фармацевтична технологія вивчає можливість використання CBGVA як компонента в багатокомпонентних препаратах з синергічною дією, зокрема, разом із неканабіноїдними молекулами, такими як флавоноїди, терпеноїди або інгібітори запальних каскадів. Це відкриває можливості розробки комбінованих засобів, де CBGVA діє не лише як активна речовина, але і як підсилювач фармакологічної дії інших агентів.
Проблеми інтеграції в комерційні продукти
Хоча перспективи використання CBGVA у промисловості виглядають привабливо, з технічної та правової точки зору існують численні перешкоди для його комерціалізації. Одним з головних бар’єрів залишається нестабільність сполуки. CBGVA має тенденцію до декарбоксилювання за умов зберігання або обробки, що ускладнює створення стабільних форм для комерційного розповсюдження. Навіть у контрольованих умовах, де температура і вологість регулюються, досягти тривалого збереження хімічної цілісності CBGVA є непросто.
Інший аспект – хімічна чистота. Оскільки CBGVA часто отримується в суміші з іншими кислотними формами канабіноїдів, його виокремлення потребує високоточних методів хроматографії або фракціонування, що значно підвищує собівартість виробництва. Крім того, оскільки молекула є нестабільною до окиснення, її ізоляція вимагає інертного середовища, що вимагає спеціалізованого обладнання.
Правове регулювання також є непростим. Хоча CBGVA сама не є контрольованою речовиною, її походження з канабісу часто підпадає під регуляторні обмеження, особливо в країнах із жорстким законодавством щодо продуктів, пов’язаних із коноплями. У багатьох випадках виробники зобов’язані підтвердити, що продукт не містить THC або його вміст не перевищує встановлені межі. Це створює додаткове навантаження на контроль якості та лабораторне тестування кожної партії продукції.
Відсутність широкої нормативної бази для кислотних форм канабіноїдів ускладнює отримання дозволів на патентування формул або реєстрацію препаратів. CBGVA, як рідкісний компонент, не має ще достатньої історії безпечного використання, а отже регуляторні органи схильні застосовувати консервативні підходи до його апробації. Це значно сповільнює інноваційні процеси у сфері застосування кислотних канабіноїдів у промислових продуктах.
Проблеми маркетингової стратегії також не є другорядними. Оскільки CBGVA не має значної популярності або клінічної історії, споживачі, навіть у нішевих фармацевтичних ринках, не мають сформованого уявлення про його властивості чи безпечність. Це призводить до того, що компаніям доводиться інвестувати не тільки у виробництво, але й у просвітницькі кампанії, клінічні дослідження та валідацію, що вимагає значних ресурсів.
З технічного боку, впровадження CBGVA у продукти харчування або косметику стикається з проблемами легалізації на рівні стандартів, таких як GRAS (Generally Recognized As Safe) у США або відповідні норми EFSA в ЄС. Без чіткої регуляторної позиції, виробники змушені дотримуватись обхідних стратегій, які можуть обмежувати функціональність або впливати на кінцеву вартість продукту.
Існують також труднощі у масштабуванні виробництва CBGVA. Враховуючи низьку природну концентрацію в рослині та високу вартість синтетичних або біотехнологічних методів отримання, промислова інтеграція вимагає розробки високопродуктивних біореакторів або генно-модифікованих ліній канабісу. Такі проекти мають довгий цикл розробки та високі інвестиційні ризики.
Використання CBGVA в майбутньому: Перспективи та дослідження
Потенціал для майбутніх досліджень
На тлі постійного зростання зацікавленості до маловивчених фітоканабіноїдів, канабігероваринова кислота (CBGVA) вирізняється своїм винятковим науковим потенціалом, який на сьогодні залишається суттєво недослідженим. Основна причина цієї наукової лакуни полягає в обмеженому доступі до чистої сполуки через її низьку природну концентрацію в рослинах роду Cannabis, а також через технічні бар’єри при її ізоляції та збереженні у стабільній формі. Однак саме цей недолік створює потребу в розробці більш досконалих методів аналітичної і біохімічної оцінки речовини, що водночас відкриває значні горизонти для інновацій.
Актуальним напрямом є синтез аналогів CBGVA, що можуть мати змінені фізико-хімічні властивості при збереженні або посиленні біологічної активності. Такий підхід дозволить вивчити SAR-моделі (structure–activity relationships), які розкривають, які структурні фрагменти молекули є відповідальними за специфічні біохімічні ефекти. Поглиблене розуміння цих взаємозв’язків дозволить не лише оптимізувати фармакологічний профіль, але й створити похідні речовини з заданою дією, що розширить арсенал потенційних терапевтичних засобів на основі канабіноїдних прекурсорів.
Крім того, перспективним виглядає застосування мультиоміки – зокрема метаболоміки та протеоміки – для визначення біологічних наслідків дії CBGVA на клітинному рівні. Ці технології дозволяють здійснювати системну оцінку метаболічних змін, спричинених введенням речовини, що особливо важливо для речовин, які не демонструють чітких ефектів через класичні рецепторні механізми. Комплексне біоінформатичне моделювання дозволить спрогнозувати потенційні фармакокінетичні властивості, взаємодію з ферментними системами та метаболічну стабільність молекули.
Значну увагу слід приділити оптимізації методів біотехнологічного отримання CBGVA – зокрема, за допомогою генно-інженерних підходів із використанням модельних мікроорганізмів (наприклад, Saccharomyces cerevisiae, Escherichia coli) для біосинтезу канабіноїдних кислот з контрольованими параметрами продуктивності. Такий напрям потребує створення синтетичних метаболічних шляхів із залученням ферментів, що беруть участь у природному синтезі CBGVA у рослинах, та їх подальшої оптимізації через еволюційне проектування. У перспективі це відкриє можливості для промислового виробництва речовини без необхідності вирощування канабісу.
Перспективи застосування в альтернативній медицині
На тлі глобальної тенденції до інтеграції нетрадиційних медичних практик у межах доказової медицини, канабігероваринова кислота демонструє потенціал як унікальний кандидат для створення інноваційних терапевтичних платформ. Завдяки відмінному профілю взаємодії з системами регуляції організму, що не обмежуються канабіноїдною системою, CBGVA розглядається як ключовий компонент в майбутніх підходах до персоналізованої медицини.
Однією з провідних концепцій є використання CBGVA у рамках комплементарної фармакотерапії, коли речовина виступає в ролі модулятора ендогенних механізмів захисту без прямого блокування чи стимуляції класичних рецепторів. У цьому контексті важливим напрямом дослідження є вивчення впливу CBGVA на регуляцію епігенетичних механізмів, зокрема ацетилювання гістонів і мікроРНК-посередкованих шляхів, що може мати значення для таких патологічних станів, як хронічний біль, нейрозапалення, або порушення нейропластичності.
Існує також концептуальна гіпотеза про здатність CBGVA модулювати сигнальні каскади, пов’язані із гліальними клітинами головного мозку, які є ключовими учасниками у розвитку нейродегенеративних процесів. Це відкриває перспективи використання речовини у стратегіях нейропротекції, зокрема при початкових стадіях хвороби Паркінсона, аміотрофічному латеральному склерозі та хворобі Гентінгтона, де традиційні медикаментозні втручання демонструють обмежену ефективність.
Крім того, CBGVA може бути інтегрований у мультикомпонентні фітотерапевтичні препарати, що будуть націлені на гармонізацію взаємодії між ендокринною, імунною та вегетативною системами. Підхід “ентураж-ефекту”, хоча й потребує подальшої валідації для CBGVA, дозволяє передбачити, що комбінація цієї сполуки з іншими нефрагментованими компонентами фітокомплексу може призводити до синергічного ефекту без необхідності високих дозування.
Альтернативна медицина також може розглядати CBGVA як м’який регулятор метаболічних процесів, зокрема у контексті порушень вуглеводного обміну або окисного стресу. Потенціал використання речовини у нутрицевтичних або адаптогенних продуктах вимагає ґрунтовних клінічних оцінок, однак початкові експериментальні результати свідчать про здатність CBGVA опосередковано впливати на метаболічну гомеостазу, що особливо цікаво для пацієнтів із метаболічним синдромом або предіабетичними станами.
У межах глобального тренду на екологічну фармакологію, що фокусується на використанні природних біоактивних сполук з мінімальним рівнем токсичності, CBGVA набуває особливої актуальності як потенційний хемосенсибілізатор – речовина, що здатна підвищувати ефективність класичних фармакологічних засобів, знижуючи необхідне дозування та побічні ефекти. Такий підхід, інтегрований у структуру персоніфікованих програм лікування, може стати основою для наступного покоління фітоканабіноїдних продуктів медичного спрямування.
Висновок
Канабігероваринова кислота (CBGVA) – це малодосліджений, але надзвичайно перспективний фітоканабіноїд, який відкриває нові горизонти у фармакології, біохімії та біотехнологіях. Вона постає як один із ключових проміжних метаболітів у біосинтезі варинових похідних канабіноїдів, зокрема тетрагідроканабігероварину (THCV) та канабідігероварину (CBDV), проте на відміну від похідних, має власний спектр біологічної активності, що досі залишається лише частково охарактеризованим.
Вивчення її хімічної структури виявило складну взаємодію між ароматичними та карбоксильними фрагментами, що зумовлює її унікальну хімічну поведінку, включно з підвищеною реактивністю в умовах кислотно-основного впливу, нестабільністю до світла та термічного розпаду. Незважаючи на це, молекулярна структура CBGVA демонструє специфічну хемоселективність, яка відкриває потенціал для розробки нових похідних через хімічну модифікацію або функціоналізацію.
З біосинтетичної точки зору, CBGVA утворюється шляхом специфічної терпенової конденсації із залученням геранілпірофосфату (GPP) та диваринолінової кислоти, що є вариновим аналогом оліветолової кислоти. Цей біохімічний шлях, хоч і частково ідентичний до синтезу CBG-A, має специфічності у ферментативному каталізі, зокрема в реакціях, опосередкованих синтазами з високою регіоселективністю. Експериментальні дані свідчать, що кількісне накопичення CBGVA тісно корелює з рівнем експресії відповідних ферментів у трихомах канабісу, що формує підґрунтя для таргетованої генетичної селекції та інженерії.
Сучасні технології екстракції CBGVA стикаються з численними викликами, зокрема через її кислотну природу та термолабільність. Серед ефективних методик виокремлюють кріогенну екстракцію з ультразвуковою стимуляцією, супер-критичну CO₂-екстракцію з модифікованими параметрами тиску і температури, а також мікрофлюїдні системи, які дозволяють зберігати цілісність кислотної форми. Особливої уваги заслуговують ферментативні біоекстракції, які можуть забезпечити селективність за умов помірного енергетичного впливу.
Генетичні модифікації канабісу в напрямку збільшення вмісту CBGVA наразі перебувають на етапі ранніх досліджень. Створення сортів із цілеспрямованим пригніченням синтезу THCA і CBDA на користь варинових шляхів має потенціал не лише для підвищення виходу CBGVA, але й для подальшого збагачення портфоліо канабіноїдів із вузькою біологічною специфікою.
З фармакологічної точки зору, CBGVA демонструє здатність опосередковано впливати на рецептори CB1 та CB2, хоча її афінність до цих мішеней нижча, ніж у активних декарбоксильованих форм. Проте це не виключає її участі в регуляції ентоканабіноїдної системи через алостеричні механізми або модуляцію ферментів, відповідальних за метаболізм ендогенних лігандів. Первинні in vitro результати свідчать про нейромодулюючі ефекти, пригнічення мікрогліальної активації, а також потенційну антиноцицептивну дію без участі психоактивних шляхів.
Не менш важливою є антиоксидантна активність CBGVA, що проявляється через хімічне гасіння вільних радикалів, відновлення глутатіонового потенціалу клітин та захист структурних компонентів мембран від перекисного окиснення. Завдяки цьому відкриваються перспективи для його застосування у терапії хронічних запалень, дегенеративних захворювань ЦНС, а також в рамках мультимодальної протизапальної стратегії у системній медицині.
Попри значний науковий потенціал, впровадження CBGVA в клінічну практику стикається з низкою технічних і правових обмежень. Зокрема, нестабільність нативної форми у біологічних середовищах, потреба в стабілізації формул, обмежений доступ до стандартизованих екстрактів та фрагментарність доклінічної доказової бази – всі ці чинники уповільнюють перехід до масштабного дослідження у клінічному середовищі. Крім того, у багатьох юрисдикціях CBGVA досі не відокремлений правовим статусом від основних психоактивних канабіноїдів, що ускладнює дозвільні та етичні аспекти досліджень.
Щодо технічного застосування в медицині та фармацевтиці, CBGVA розглядається як перспективна сировина для розробки нових фармацевтичних субстанцій, зокрема у формі кислотостійких мікрокапсул, пролонгованих наноформ, або як субстрат для напівагоністичних похідних. Підходи до інкапсуляції з використанням ліпосом, твердих ліпідних частинок або полімерних носіїв забезпечують збереження хімічної цілісності молекули при доставці в біологічні системи. У цьому контексті критичним залишається завдання стандартизації промислових методів отримання, які можуть бути адаптовані до GMP-рівня виробництва.
З погляду майбутнього, CBGVA уособлює нову фазу в дослідженні неактивних кислотних форм канабіноїдів, які тривалий час залишались поза увагою фармакології. Застосування CBGVA в альтернативній медицині виглядає вірогідним, особливо в рамках інтегративного підходу до лікування хронічного болю, тривожних станів, імуноопосередкованих патологій та метаболічних порушень. Її комбінація з іншими кислотними формами або адаптогенами природного походження може створити новий клас багатокомпонентних фітопрепаратів із мінімальною токсичністю та широким профілем дії.
Джерела
- Udoh M. et al. – Одне з небагатьох експериментальних досліджень CBGVA, де показано, що ця сполука може взаємодіяти з іонними каналами та GPR55-рецепторами. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9652735/
- Valliere M.A. et al. – Робота, що описує біосинтетичну платформу для отримання канабіноїдів, включаючи CBGVA, поза межами живої рослини. Важливе джерело з біотехнологічної точки зору. https://www.nature.com/articles/s41467-019-08385-z
- Shoyama Y. et al. – Оригінальна робота з ізоляції CBGVA з тайського канабісу, важлива для історії вивчення сполуки. https://diverdi.colostate.edu/C442/references/other/handbook%20of%20cannabis%20-%20pertwee/ch%2001.pdf
- NIST (2024) – Звіт Національного інституту стандартів і технологій США щодо якості аналітики канабіноїдів, включаючи нові кислоти. Підтверджує складність точного вимірювання таких сполук як CBGVA. https://nvlpubs.nist.gov/nistpubs/ir/2024/NIST.IR.8519.pdf
- DOE OSTI – Офіційна публікація Міністерства енергетики США про альтернативні способи біосинтезу канабіноїдів, зокрема CBGVA. https://www.osti.gov/biblio/1613646
- Academia.edu – Відкрита версія дослідження з фармакології CBGVA та його впливу на нейрональні канали. Зручна для швидкого доступу до основних висновків.
https://www.academia.edu/123143988/The_anticonvulsant_phytocannabinoids_CBGVA_and_CBDVA_inhibit_recombinant_T_type_channels - PubChem (NIH/NLM) – Повна хімічна інформація про молекулу CBGVA: структура, ідентифікатори, властивості, CID. https://pubchem.ncbi.nlm.nih.gov/compound/Cannabigerovarinic-acid
- EMCDDA – Офіційне агентство Європейського Союзу з інформацією про правовий статус та дослідження канабіноїдів. Підходить для розділів, пов’язаних із регуляцією та перспективами. https://www.emcdda.europa.eu/publications/topic-overviews/cannabis-legal-status-europe_en
- FDA – Позиція Управління з контролю за продуктами і ліками США щодо канабіноїдів у медицині. Це важливо для розділу про медичне застосування.
https://www.fda.gov/news-events/public-health-focus/fda-regulation-cannabis-and-cannabis-derived-products-including-cannabidiol-cbd - ClinicalTrials.gov – Офіційна база клінічних випробувань. Через ключові слова можна віднайти як прямі, так і суміжні дослідження CBGVA.
https://clinicaltrials.gov/