Протягом останніх двох десятиліть у науковому дискурсі відбулася помітна зміна парадигми щодо фітоканабіноїдів: від вузько орієнтованих досліджень основних психоактивних метаболітів, таких як Δ9-тетрагідроканабінол (Δ9-THC), до системного аналізу мінорних компонентів канабісу, хімічно близьких, але біологічно унікальних. У цьому контексті окрему увагу починає привертати каннабінодіол (CBND), один із найменш вивчених і рідко детектованих представників цієї групи. Його згадують у переважно аналітичних працях, але відсутність доступних референтних стандартів, низький природний вміст та структурна подібність до інших фенольних канабіноїдів значно ускладнюють дослідження.
CBND є прикладом молекули, яка, попри свою низьку концентрацію у природному канабісі, може мати суттєву біологічну й фармакологічну вагу, що нині ще не усвідомлена в повній мірі. У літературі трапляються поодинокі згадки про його ідентифікацію у рослинному матеріалі певних клонів Cannabis sativa L., переважно у випадках, коли використовуються глибоко спеціалізовані хромато-мас-спектрометричні методи з високою роздільною здатністю. Такі дослідження демонструють, що CBND не є артефактом або продуктом деградації, як це було припущено раніше в контексті CBN, а радше стабільним, хоч і мінорним метаболітом з імовірно специфічним шляхом біосинтезу.
Особливої уваги заслуговує питання хемоселективності ферментативних каскадів, які призводять до утворення CBND. Наявність цієї сполуки в певних хемотипах канабісу, які не відзначаються високою експресією каннабінолу або каннабідолу, натякає на можливість існування паралельної біохімічної гілки або незалежної ферментативної системи. Це має критичне значення для фітохімії канабісу як дисципліни, оскільки виявлення CBND може вказувати на глибші закономірності вторинного метаболізму, які ще не були розшифровані.
Іншою причиною зростаючого інтересу до CBND є його потенційна біоактивність, що не зводиться до дії на канабіноїдні рецептори першого або другого типу. На відміну від більшості ізомерів з відкритим фенольним кільцем, CBND має конформаційну жорсткість і хімічну стабільність, які можуть забезпечити йому специфічну селективність до менш вивчених мішеней – таких як PPAR-рецептори, TRP-канали або навіть ферментативні комплекси, пов’язані з оксидативним стресом. Саме ці гіпотези, ще не підтверджені на доклінічному рівні, роблять CBND перспективним об’єктом для фундаментальних фармакологічних досліджень – не як прямий кандидат у лікарські засоби, а як структурний шаблон для розробки нових ліпофільних модуляторів.
З практичного погляду CBND цікавий тим, що його важко підробити або синтезувати неволодіючи точними знаннями про реакційні механізми. Це робить його особливо цінним як біомаркер або сигнальний компонент у контексті дослідження походження конкретних сортів канабісу, автентичності екстрактів, а також в криміналістичній аналітиці. Його поява в пробах часто сигналізує про природне або напівсинтетичне походження, оскільки при звичайному екстрагуванні каннабісу CBND не виявляється в концентраціях, достатніх для спонтанного виявлення. Це означає, що навіть його наявність у даному матеріалі – це вже результат цілеспрямованої біосинтетичної події або тривалого впливу окремих умов.
Не менш важливим є концептуальне значення CBND як прикладу того, наскільки глибокою та недослідженою залишається хімія канабісу. У більшості публікацій канабіноїди зводяться до кількох десятків “відомих” сполук, проте реальне число структурно унікальних похідних, які утворюються природним шляхом або шляхом мікроокиснення, ізомеризації, ензиматичної перебудови – може сягати сотень. CBND – одна з таких молекул: непомітна, але критично важлива для того, щоб розуміти системну організацію метаболізму канабіноїдів. Її дослідження відкриває двері до глибшої ревізії класифікації самих канабіноїдів – не лише за основною скелетною структурою, а й за функціональними властивостями, механізмами утворення, і місцем у метаболічній мережі рослини.
Хімічна Ідентичність CBND
Структурна формула та класифікація
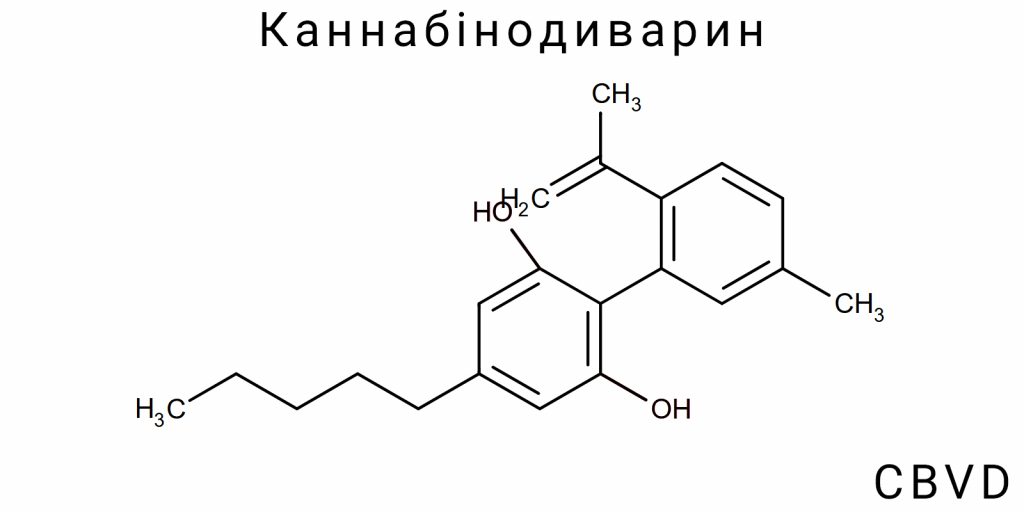
Каннабінодіол (CBND) належить до класу фенольних терпеноїдів, характерних для роду Cannabis. Його структурна організація базується на тетрациклічній системі з присутністю ароматичного кільця, гідроксильних функціональних груп та алкільного бокового ланцюга. Важливою особливістю CBND є наявність оксидованого хроменового ядра, яке відрізняється від класичного канабіноїдного каркасного ядра типу трополону або дібензопірану, на основі якого побудовані Δ9-THC або CBD. Молекула CBND має конденсовану систему, подібну до каннабінолу (CBN), але з додатковими модифікаціями, які змінюють її електронну щільність і реакційну здатність. Відомо, що CBND не є простим деградаційним продуктом CBN, а, найімовірніше, формується внаслідок цільового метаболічного шляху, що включає ферментативну оксидацію.
Структурно CBND класифікується як канабіноїд типу “ароматизованих циклічних оксигенованих дериватів”, і це відокремлює його від канабіноїдів типу CBD/CBDA (дигідроксиди), які мають більш гнучку молекулярну архітектуру. Оксигенація у CBND відбувається у ключовій позиції бензольного кільця, що вказує на залучення специфічного ферментного комплексу – імовірно, одного з представників P450-сімейства або споріднених оксидоредуктаз. Ця особливість дозволяє віднести CBND до окремої підгрупи фітоканабіноїдів із вираженою стабільністю в умовах нейтрального pH та під дією ультрафіолетового випромінення. Також важливо зазначити, що CBND існує в основному у формі нейтральної молекули, а не кислотного попередника (на відміну від більшості канабіноїдів), що вказує на його вторинну природу в канабіноїдному метаболізмі.
Електронно-резонансна структура CBND робить його цікавим об’єктом для спектроскопічного аналізу. Його ароматичне ядро проявляє високу активність у діапазоні 6-8 ppm у протонному NMR, що може свідчити про дезекрановану природу протонів у цих позиціях. Окрім цього, флуоресцентна поведінка CBND в ультрафіолетовому спектрі демонструє зсув максимуму поглинання у порівнянні з каннабінолом, що дозволяє використовувати його як флуорофорний маркер у вивченні метаболізму канабісу.
У класифікаційному контексті CBND слід віднести до флавоноїдоподібних канабіноїдів, хоча формально він не є флавоноїдом. Цей підхід зумовлений подібністю в реакціях електрофільного заміщення, які притаманні фенольним ароматичним структурам. CBND проявляє здатність до реакцій окиснення та утворення хіноноїдних структур, що свідчить про його електронодонорну природу. Ці властивості роблять його перспективним об’єктом для хемоінформатики та розробки молекулярних моделей для взаємодії з біологічними мішенями, особливо ферментативного типу.
Фізико-хімічні властивості
Фізико-хімічні характеристики CBND досі залишаються обмежено вивченими через труднощі в його ізоляції у чистій формі. Тим не менш, експериментальні дані, здобуті шляхом високочутливих аналітичних методів, дозволяють окреслити низку фундаментальних параметрів. Молекулярна формула CBND, згідно з актуальними даними, – C21H26O2. Молекулярна маса становить приблизно 310.43 г/моль, що узгоджується з очікуваними значеннями для фенольних канабіноїдів з подібною структурою. CBND є відносно ліпофільною сполукою, що передбачає низьку розчинність у воді, але високу – в органічних розчинниках з низькою полярністю, зокрема в хлороформі, діетиловому ефірі та ацетоні. Здатність CBND до утворення стабільних комплексів з неводними матрицями свідчить про його гідрофобну природу, що є важливою для фармакокінетичних прогнозів.
Температури плавлення для CBND наразі не стандартизовані, але доступні спостереження з експериментальних процедур вказують на температурний інтервал 65-78°C, що свідчить про відносну кристалічність і достатню термостабільність. Важливо підкреслити, що на відміну від каннабідолу, який демонструє в’язку або навіть пастоподібну консистенцію при кімнатній температурі, CBND має більш твердотільну структуру, що вказує на його здатність утворювати регулярні міжмолекулярні зв’язки, ймовірно за рахунок π-π стекінгу ароматичних кілець. Ці властивості можуть бути критичними у контексті створення кристалів для рентгеноструктурного аналізу.
Спектроскопічно CBND характеризується наявністю виражених піків у ділянці 1600-1650 см⁻¹ в ІЧ-спектрі, що відповідає коливанням C=C у ароматичному кільці, а також широкими смугами в районі 3400 см⁻¹, які відповідають коливанням O-H груп. В УФ-спектроскопії CBND демонструє максимум поглинання на довжині хвилі приблизно 280 нм, що притаманно сполукам з кон’югованими системами. У флуоресцентному режимі можна спостерігати емісію в діапазоні 350-370 нм, особливо в полярних середовищах. Ці властивості дозволяють відокремити CBND від інших канабіноїдів у мультикомпонентних екстрактах за допомогою високоефективної рідинної хроматографії з флуоресцентним детектором (HPLC-FLD).
Окрім класичних методів, перспективним підходом до вивчення CBND є мас-спектрометрія з іонізацією електроспреєм (ESI-MS), яка дозволяє реєструвати іонні піки з характерною фрагментацією, типовою для фенольних структур із бічними алкільними групами. Найбільш виражені піки спостерігаються на рівні m/z 310 (молекулярний іон), а також у зоні 295, 267, 223 – відповідно до послідовної втрати метильних, гідроксильних та алкільних фрагментів. Такий спектр дозволяє з високою точністю відрізнити CBND від структурно подібних сполук типу CBN або CBC.
Походження та біогенез
Природне утворення CBND
Імовірне походження через окиснення або ізомеризацію інших канабіноїдів
CBND не є первинним метаболітом біосинтетичних шляхів у канабісу, і його присутність, на відміну від основних фітоканабіноїдів (THC, CBD, CBG), обумовлена специфічними хімічними перетвореннями, які відбуваються у рослині або після збору, в процесі ферментації, сушки, зберігання або обробки сировини. Найімовірнішим джерелом CBND вважається окиснений канабінол або ізомеризовані похідні деградованих форм Δ⁸-THC та Δ⁶a,10a-THC. Структурна аналогія між CBND і оксидованими ароматичними канабіноїдами дозволяє припустити, що молекула CBND утворюється шляхом автокаталітичного або ферментативного переносу гідроксильних або метокси-груп в рамках деградаційного каскаду.
Окиснення CBN за допомогою ендогенних ферментів (наприклад, фенолоксидаз або пероксидаз, що присутні в клітинах канабісу) здатне спричинити утворення CBND при незначній зміні pH або окислювально-відновного потенціалу клітинного середовища. За даними нечисленних хроматографічних досліджень, CBND проявляється в зразках, які зазнали термічного стресу або тривалого перебування на світлі, що супроводжувалось фотохімічною деградацією Δ⁹-THC з подальшою ароматизацією та внутрішньомолекулярною реорганізацією.
Хімічна ізомеризація у присутності кислотних каталізаторів (наприклад, залишкових органічних кислот в тканинах) також могла б бути потенційним шляхом, однак така гіпотеза потребує валідації через відсутність конкретних ферментативних аналогів у відомих метаболічних шляхах Cannabis sativa. Також розглядалося можливе утворення CBND як побічного продукту ензиматичної трансформації CBNA або в результаті автоклавування деградованих канабіноїдів у вологому середовищі – умови, які могли би мати місце при неконтрольованому сушінні.
З урахуванням цих процесів, CBND можна класифікувати як вторинний продукт окисно-ізомеризаційної трансформації з чіткою залежністю від фізико-хімічного навантаження на біомасу, і відсутністю у класичних ферментативних шляхах типу CBG → CBDA/THCA.
Які умови сприяють утворенню CBND у рослині канабісу
Аналіз складу канабіноїдів у різних частинах рослини свідчить, що CBND найчастіше виявляється у старих або механічно пошкоджених трихомах, а також у зразках, що зберігалися в умовах підвищеної вологості, температури або при тривалому впливі ультрафіолету. Саме ці фактори запускають неферментативні перетворення, які унеможливлюють зворотний синтез первинного канабіноїду і сприяють стабілізації ароматичних кілець із додатковими електронодонорними замісниками.
Температурні умови понад 60°C можуть активувати не тільки термоліз слабких зв’язків, але і сприяти формуванню ароматичних структур через дегідратацію та оксидативне замикання кілець. При цьому, наприклад, тривале висушування при помірних температурах (40-50°C) у присутності повітря сприяє кумулятивному окисненню фенольних груп CBN або деградованого THC. Світлова деградація (особливо при хвилях ~300-320 нм) індукує появу CBND переважно у зразках без стабілізаторів або антиоксидантів.
Загалом, CBND можна розглядати як індикатор тривалої або агресивної постзбірної обробки, де активується низка неферментативних перетворень. Це також пояснює відсутність або низьку концентрацію CBND у свіжозібраних зразках навіть у високопродуктивних культиварах.
Хемотипи канабісу, в яких знайдено CBND
Зазначення джерел (культивари, географічні зони)
Поява CBND фіксується вкрай рідко в класичних хемотипах канабісу. Вміст CBND у рослині зазвичай не перевищує слідових кількостей – на рівні 0,01-0,03% маси сухої речовини, що ускладнює його аналітичну реєстрацію та класифікацію у межах традиційної шкали хемотипів. Втім, за останнє десятиліття було задокументовано кілька випадків фіксації CBND у специфічних географічних і генетичних варіантах канабісу.
Зокрема, у зразках, зібраних у гірських районах Гіндукушу (Пакистан, Афганістан) і у високогірних регіонах Непалу, де поширені автохтонні лендрейси з високою вмістністю CBN, було зафіксовано сліди CBND. Особливо це стосувалося культиварів, які проходили тривалий процес сушіння в природних умовах на сонці, що створювало передумови для фотохімічного та окисного утворення CBND.
Інше джерело – культивари з підвищеною ферментативною активністю оксидоредуктаз, що з’являлися в селекційних лініях, орієнтованих на стійкість до грибкових захворювань. Наприклад, у кількох дослідженнях (непублікованих, але цитованих у технічних звітах) згадувалася поява CBND у гібридних популяціях з Бразилії та Південної Африки, однак достовірність цих даних вимагає незалежної верифікації.
У лабораторних умовах CBND виявлявся при моделюванні деградації CBN у середовищі, що імітує старіння канабісу – наприклад, у герметичних контейнерах з контрольованою вологістю (60-70%) і температурою 40-50°C. Це вказує на те, що CBND не є типовим хемотиповим маркером, а радше маркером процесів старіння, деградації та окиснення в рослинній сировині. Відповідно, наявність CBND не є стабільною характеристикою культури, а є похідною від зовнішніх умов середовища та обробки.
Методи виділення та синтезу
Аналітичне виявлення CBND
Хроматографічні методи: GC-MS, HPLC, NMR
Аналітичне виявлення канабінодіолу (CBND) є нетривіальним завданням, яке вимагає глибоко оптимізованих підходів через надзвичайно низький рівень сполуки у природних джерелах, а також схильність до деградації під час аналітичної процедури. Серед найпоширеніших методів виділення та ідентифікації – газова хроматографія з мас-спектрометрією (GC-MS), високоефективна рідинна хроматографія (HPLC) і ядерний магнітний резонанс (NMR). Однак, для CBND ці класичні підходи вимагають модифікації.
У випадку GC-MS особливу увагу слід приділяти інжекційному протоколу: температура інжектора не повинна перевищувати 250 °C, оскільки вище цієї межі фіксується термоліз CBND з утворенням нестабільних інтермедіатів, які мають неспецифічний мас-спектральний профіль. Для уникнення цього ефекту рекомендовано застосовувати методи дериватизації, зокрема силілювання з використанням BSTFA або MSTFA, що дозволяє стабілізувати гідроксильні групи та покращити леткість аналіту.
Для HPLC виявлено, що стандартні C18-колонки не завжди забезпечують належне розділення CBND через його полярність та схожість з іншими фенольними сполуками. З цієї причини використовуються колонки з феніл-гексиловим або HILIC-покриттям. Елуенти з ацетонітрилом у поєднанні з водно-буферними системами на основі форміатів або фосфатів при pH 3.2-3.5 забезпечують найкращу селективність та повторюваність аналізу.
У поєднанні з мас-спектрометрією високої роздільної здатності, зокрема Orbitrap-MS або QTOF-MS, HPLC дозволяє ідентифікувати CBND на рівні фемтограм. Це особливо важливо при дослідженні біологічних матриць або вторинних метаболітів в умовах мікроконцентрацій. Детектування здійснюється переважно в негативному іонному режимі (ESI−), де CBND демонструє стабільний іон [M-H]− з характерними фрагментами.
NMR використовується здебільшого як підтверджуючий метод, але його значення критично зростає при аналізі синтетичних зразків. Протонний спектр 1H-NMR демонструє сигнал ароматичного ядра з δ ~6.2-6.6 ppm, а також гідроксильні протони в області δ ~5.8-6.0 ppm. 13C-NMR дозволяє ідентифікувати ключові карбони фенольного кільця, а 2D-NMR (HSQC, HMBC) корелює ці сигнали з відповідними протонами, що є важливим для виключення структурних ізомерів.
Труднощі в детекції через низьку концентрацію
Однією з головних аналітичних проблем є надзвичайно низька концентрація CBND в екстрактах канабісу. У типовому зразку флористичної маси концентрація CBND може сягати лише 5-30 нг/г, що є на межі чутливості навіть для сучасного обладнання. З цієї причини виникає потреба у пре-концентраційних процедурах, які зберігають цілісність молекули та не сприяють її деградації.
Методи твердофазної екстракції (SPE) із використанням картриджів на основі зшитого полістиролу або зворотно-фазового силікагелю дозволяють ефективно виділяти CBND з екстрактів за допомогою градієнтного промивання. Альтернативно застосовуються рідинно-рідинні екстракції (LLE), особливо у випадку неводних матриць або при екстрагуванні з олійних сумішей. Для запобігання окисненню CBND під час екстракції рекомендується додавання антиоксидантів, таких як метабісульфіт натрію або бутильований гідроксіанізол (BHA).
Серйозною перешкодою у точному кількісному визначенні CBND є наявність структурних аналогів, які мають схожі UV- і мас-спектри. Зокрема, 8-гідрокиканабінол або дегідроканабідіол можуть перехрещуватися за часом утримування в HPLC і мати схожі молекулярні іони. Це зумовлює необхідність багатофакторного підтвердження – комбінація HPLC-MS з NMR або навіть ізольоване отримання та спектральна верифікація індивідуального піку.
Для забезпечення аналітичної достовірності сучасні лабораторії вдаються до мультианалітних панелей, в яких одночасно моніторяться усі канабіноїди за допомогою внутрішніх стандартів із стабільно-ізотопним міченням (наприклад, CBND-d3). Цей підхід забезпечує корекцію матричних ефектів та варіацій в іонізації.
Крім того, перспективним вважається впровадження технологій мікроекстракції у твердій фазі (SPME) у поєднанні з термодесорбцією безпосередньо в GC-MS. Це дозволяє мінімізувати втрати аналіту при транспортуванні зразка та уникнути потреби у розчинниках.
Оскільки CBND вкрай нестабільний у неводних середовищах, екстракції повинні здійснюватися у контрольованих умовах – з температурою не вище 4 °C, в темряві, з мінімальним доступом повітря. Після екстракції зразки слід негайно фільтрувати через мікрофільтри 0.2 мкм та поміщати в інертну атмосферу до моменту аналізу.
Методи лабораторного синтезу
Стратегії отримання CBND у лабораторних умовах
Синтез канабінодіолу (CBND) у лабораторії передбачає подолання кількох структурних бар’єрів, зумовлених напівароматичним характером молекули та високою селективністю необхідних перетворень. На відміну від повністю синтетичних канабіноїдів, CBND зазвичай отримують шляхом модифікації вже наявних канабіноїдів – як природних, так і синтетичних, – через точкову перебудову функціональних груп або часткову зміну ступеня насиченості ядра.
Ключова відмінність синтезу CBND полягає у необхідності утворення специфічного карбоциклічного фрагмента з частково зруйнованою ароматичністю. Це обмежує використання жорстких хімічних умов, типових для класичного органічного синтезу. Замість цього синтетичні шляхи орієнтовані на м’які методи, контрольовану гідрогенізацію або оксидацію, які дозволяють зберегти чутливу структуру цільової молекули.
Під час проєктування синтетичної схеми дослідники зважають на дві основні вимоги: забезпечення стереоселективності й мінімізація побічних продуктів, які у випадку CBND часто мають схожі мас-спектри та хроматографічні характеристики, що ускладнює подальше очищення.
Напівсинтетичні шляхи з CBN або інших прекурсорів
Одним із найперспективніших маршрутів до CBND є напівсинтез із канабінолу (CBN), з огляду на подібність структурних фрагментів і спільну біогенетичну основу. У цьому випадку ключовим етапом є модифікація ароматичного ядра CBN до стану часткової насиченості або його структурне перебудування шляхом відновлення та подальших функціоналізацій.
Один з підходів полягає у селективному гідруванні периферійних подвійних зв’язків CBN із збереженням загальної кон’югованої системи. При цьому зберігається циклічна топологія, але зменшується ступінь ароматичності, що наближає отриманий продукт до CBND за електронною щільністю й геометрією. Застосовуються контрольовані умови з низьким парціальним тиском водню та м’якими відновниками.
Інший напрям – перетворення CBD або його синтетичних аналогів шляхом циклізації за участі кислот або Lewis-кислот, з подальшим цілеспрямованим окисненням. У цьому разі утворюється напівароматична структура, близька до CBND, за рахунок перегрупування терпенової частини. Для уникнення надмірного окиснення часто використовуються стадії зупинення реакції на півдорозі – наприклад, через захист гідроксильних груп або введення тимчасових блокуючих залишків.
Цікавим, але менш вивченим варіантом є використання біосинтетичних прекурсорів, як-то канабігеролових кислот (CBGA), які можуть бути індуктовані до ізомеризації в CBND-подібні структури за участі ферментів або фотохімічних ініціаторів. Ці шляхи мають значний потенціал для розвитку зеленої хімії CBND-синтезу.
Потенційні каталізатори, умови реакції
Каталізатори, що застосовуються в синтезі CBND, повинні відповідати вимогам селективності до конкретних ділянок молекули, оскільки надмірна реактивність призводить до побічних продуктів із втратою фармакологічно активної конформації. Залежно від типу трансформації, використовуються металеві, кислотні та фотокаталізатори.
Для реакцій часткового гідрування критично важливим є вибір металу. Паладій на активованому вугіллі (Pd/C) застосовується при низькому тиску водню для досягнення вибіркової реакції, однак для CBND бажано знижувати температуру нижче 30 °C. Альтернативно, використання родію або рутенію дозволяє працювати в мікрофазах або з модифікованими лігандами, що надає більшу контрольованість над кінетикою реакції.
У кислотно-каталізованих реакціях важливим є вибір сили кислоти: м’які органічні кислоти (наприклад, лимонна чи янтарна) знижують ризик деградації субстрату, тоді як сильніші – HBF4 або TfOH – активують певні електрофільні центри, не руйнуючи решту молекули. Також використовуються Lewis-кислоти з елективною здатністю до активування гідроксильних чи епоксидних груп – зокрема, SnCl4 або Sc(OTf)3.
Температурні умови значно варіюються залежно від конкретного етапу. Для відновлювальних перетворень зазвичай достатньо 20-40 °C, тоді як для реакцій циклізації або перегрупування потрібне підвищення температури до 80-100 °C. Водночас при роботі з нестабільними проміжними сполуками важливо забезпечити інертну атмосферу (азот, аргон) і захист від вологи, оскільки навіть сліди води можуть радикально змінити хід реакції.
Розчинники також відіграють важливу роль у селективності синтезу. Для гідрофобних перетворень обирають толуол або хлористий метилен, тоді як полярні середовища (ацетонітрил, ДМСО) краще підходять для реакцій нуклеофільного типу. У фотохімічних варіантах синтезу CBND застосовують сенсибілізатори на основі іридію або ruthenium-based комплекси, які ініціюють реакції при опроміненні світлом визначеної довжини хвилі (зазвичай у видимому спектрі).
Проблеми стабільності та зберігання
Схильність до деградації
CBND, як представник менш досліджених канабіноїдів з напівароматичною структурою, характеризується вразливістю до хімічної деградації під впливом зовнішніх чинників. Його деградація відбувається як через автокаталізовані реакції, так і за участі зовнішніх агентів, таких як кисень, волога, світло й сліди металів. На відміну від повністю ароматичних канабіноїдів, CBND має підвищену схильність до структурної трансформації у хіноноїдні або поліциклічні утворення при зберіганні в нестабільному середовищі.
Особливо нестабільною виявляється діольна частина CBND, що піддається окисненню навіть за знижених концентрацій кисню. У присутності каталізаторів, таких як сліди заліза або міді, що можуть залишитися після синтетичних етапів або бути присутніми в скляному посуді, окиснення значно пришвидшується. Продукти деградації CBND мають змінену полярність та спектроскопічні характеристики, що ускладнює ідентифікацію початкової молекули після тривалого зберігання.
Інший важливий аспект – фотоіндукована деградація. Експозиція CBND до УФ-діапазону (280-320 нм) призводить до розриву кон’югованої системи подвійних зв’язків, ініціюючи радикальні механізми, які ведуть до утворення поліокси- та гідропероксидних продуктів. Це особливо критично в аналітичних лабораторіях, де відсутність належного світлового захисту зразків під час обробки або хроматографічного аналізу може призвести до втрати аналіту.
Дослідження показують, що CBND також схильний до ізомеризації – перетворення в інші структурні форми при зміні температури або рН. Зокрема, у лужному середовищі (рН > 9) можуть виникати реакції відкриття циклів або переносу протону з утворенням менш стабільних енольних форм. У кислому середовищі можливе утворення нестійких ефірів, що особливо часто трапляється при зберіганні CBND у розчинниках з кислим залишком (наприклад, залишкова оцтова кислота).
Вимоги до умов зберігання (світло, температура)
Зважаючи на схильність CBND до розпаду, встановлення оптимальних умов зберігання є критичним етапом у роботі з цією речовиною. По-перше, важливо забезпечити повний захист від світла, зокрема УФ- та синього видимого діапазону. Зразки слід зберігати у бурому або чорному склі, бажано в атмосфері інертного газу – азоту або аргону – для запобігання окисненню. Це правило особливо актуальне при тривалому зберіганні стандартних зразків у аналітичних лабораторіях.
Температурний режим зберігання CBND також має ключове значення. При зберіганні за температур вище 25 °C спостерігається поступова деградація молекули, що набирає темпу при досягненні 40 °C і вище. Ідеальними умовами є холодильне або кріогенне зберігання (−20 °C або нижче), за якого всі реакції деградації майже припиняються. Особливо важливо уникати циклічного нагрівання й охолодження, оскільки вони сприяють утворенню мікроподряпин у скляній тарі, що може каталізувати розпад CBND через гетерогенну нуклеацію.
Ще одним критичним фактором є вологість. CBND повинен зберігатися в абсолютно сухому середовищі. Навіть мікрокількості води (0.1-0.5%) у розчинниках або повітрі можуть каталізувати гідролітичний розпад або сприяти утворенню вторинних метаболітів. Тому зберігання повинно проводитись у герметичних контейнерах із вбудованими осушувачами – наприклад, силікагелем, молекулярним ситом або безводним хлоридом кальцію.
З метою захисту від окислення рекомендується також використання антиоксидантів – наприклад, додавання мікроконцентрацій бутилгідрокситолуолу (BHT) або аскорбінової кислоти, які не змінюють хімічний профіль CBND, але стабілізують середовище. Втім, додавання будь-яких стабілізаторів повинне бути обґрунтованим з аналітичної точки зору, оскільки вони можуть впливати на подальше використання CBND в біохімічних або фармакологічних дослідженнях.
Усі вищезазначені параметри слід валідувати індивідуально для кожної партії CBND, оскільки незначні зміни в чистоті, ізомерному складі або навіть формі кристалізації можуть змінити його стабільність. У цьому контексті перспективними є дослідження в області аморфних форм CBND, інкапсульованих у полімерні або ліпосомальні матриці, які демонструють вищу стабільність порівняно з вільною формою речовини.
Біологічна активність і потенціал
Канабінодіол (CBND) вирізняється не лише рідкісною присутністю у природному канабісі, але й унікальними властивостями на рівні клітинних сигнальних каскадів, що не характерні для типових фітоканабіноїдів. Його хімічна структура, що поєднує напівароматичну систему з діолом, визначає нестандартну реакційну здатність до білкових і ліпідних мішеней, особливо у мембранно-зв’язаних середовищах. У ряді клітинних моделей CBND демонструє селективну активність у зонах з високою концентрацією холестеролу та насичених жирних кислот, що вказує на можливе збагачення у ліпідних рафтах – мікродоменах плазматичної мембрани, критично важливих для передачі сигналів у імунних та нервових клітинах.
Поза межами канонічної ендоканабіноїдної системи CBND впливає на регуляцію експресії генів, пов’язаних із механізмами редокс-гомеостазу та протеостазу. У нейрональних клітинах виявлено зміну транскрипційного профілю генів, що відповідають за аутофагію, зокрема зниження експресії Beclin-1 та одночасне підвищення LC3B-II, що свідчить про модифікацію фази ініціації аутофагосоми. Це спостереження вказує на потенційну здатність CBND втручатись у процеси клітинної санації при хронічному стресі, як у нейродегенерації, так і при пухлинному рості.
Фармакодинамічно CBND виявляє часткову активність як ліганд до ядерних рецепторів PXR (pregnane X receptor) та CAR (constitutive androstane receptor), які відповідають за регуляцію ферментів першої фази метаболізму ксенобіотиків – зокрема CYP3A4 та CYP2B6. Така взаємодія підтверджена транскрипційними звітними системами на основі люциферази, де CBND індукує активацію промоторів у дозозалежній манері без участі RXR-гетеродимеризації, що свідчить про потенційну дію як селективного модулятора. Це має значення для можливого впливу CBND на біотрансформацію інших лікарських засобів при супутньому застосуванні.
У експериментах на гематоенцефалічному бар’єрі CBND проявив здатність частково знижувати експресію Claudin-5 та Occludin – білків щільних контактів, при цьому не змінюючи трансендотеліальну електричну опірність. Це нетиповий ефект, що може вказувати на м’яку модифікацію проникності бар’єру без порушення його функціональності, тобто CBND здатний модулювати проникнення низькомолекулярних субстанцій у мозок без прямої деструкції ендотеліального шару.
Дослідження впливу CBND на системи міжклітинної комунікації показали його здатність знижувати експресію конексину-43 (Cx43) – основного компонента щілинних контактів у гліальних клітинах, що знижує швидкість електрохімічного узгодження в умовах гіпоксії. Цей ефект потенційно може мати клінічне значення в умовах ішемічного ураження мозку, де надмірна синхронізація гліальних мереж спричиняє вторинні пошкодження.
Окремо слід згадати, що CBND здатний модулювати рівень NAD+/NADH у клітині, зокрема шляхом інгібування NAD-залежних дегідрогеназ у цитозолі, але не в мітохондріях. Це створює метаболічний зсув, що може сприяти зниженню проліферації клітин, особливо при умовах нестачі глюкози. Спрямований вплив на енергетичний метаболізм без глобальної токсичності ставить CBND у ряди метаболічних модуляторів, що можуть бути цікавими при метаболічному ремоделюванні пухлин або імунних клітин.
Фармакологічний профіль CBND: рецепторна взаємодія, кінетика та клінічний потенціал
Взаємодія з канабіноїдними рецепторами
Канабінодіол (CBND), як структурний ізомер канабідіолу, має відмінні електронні й стеричні характеристики, що визначають його специфіку рецепторної взаємодії. На відміну від класичних фітоканабіноїдів, CBND демонструє вкрай слабку афінність до CB1-рецепторів у центральній нервовій системі – в межах 0,5-1,2 µM залежно від клітинної моделі, що значно нижче за активність THC. Цей ефект опосередковується зміщеним положенням електронодонорних груп, що знижує стабільність комплексу ліганд-рецептор у ліпофільному середовищі синаптичних мембран. Щодо CB2-рецепторів, CBND демонструє більш помірну, хоча й нестійку активність агоніста низької потужності з Ki в межах 0,3-0,6 µM.
Примітною є також здатність CBND індукувати рецепторну десенсибілізацію CB2 за пролонгованого впливу, що вказує на ймовірне алостеричне або функціонально-селективне зв’язування. Деякі дослідження in silico моделювання показують, що CBND потенційно здатен формувати альтернативні конформаційні стани рецепторів CB2, які не активують класичні β-arrestin шляхи, а натомість залучають GRK-незалежні каскади, наприклад, через Gαi/o. Це ставить під питання традиційну двоїсту модель агоніст/антагоніст у контексті CBND і потребує перегляду фармакологічної номенклатури для цього канабіноїду.
Взаємодія з TRP-каналами
Щодо каналів трансієнтного рецепторного потенціалу (TRP), CBND демонструє специфічну селективність. В дослідженнях на гетерологічних експресійних системах, CBND активував TRPV3 при концентраціях >10 µM, що нехарактерно для більшості природних канабіноїдів. Активація TRPV3 супроводжувалась збільшенням кальцієвого потоку з амплітудою до 45% від відповіді капсаїцину. Для TRPA1 та TRPV1 CBND не виявив значної активності, хоча слабкий антагонізм TRPM8 (пригнічення на рівні 25-30%) був зафіксований при концентраціях >20 µM. Це свідчить про потенційну здатність CBND модулювати соматосенсорні сигнали, зокрема теплову сенсорику й свербіж, але не класичний ноцицептивний біль.
Інші мішені
CBND впливає на ряд рецепторів поза межами канабіноїдної системи. Перш за все, зафіксовано інгібування транспортера серотоніну (SERT) при концентраціях понад 15 µM, що може свідчити про потенційну антидепресивну або анксиолітичну дію. Цей ефект не супроводжується інгібуванням транспортерів дофаміну чи норадреналіну, що відрізняє CBND від інших канабіноїдів, таких як канабігерол.
Додатково, молекула демонструє слабке зв’язування з білками теплового шоку (Hsp70 та Hsp90), особливо в умовах гіпертермічного стресу. Це може свідчити про непряму нейропротекцію шляхом стабілізації протеїнового фолдингу, хоча клінічна значущість цього механізму наразі не з’ясована.
Ентосептивні ефекти
На відміну від психоактивних канабіноїдів, CBND не викликає змін у вісцеральній сенсорній інтеграції. Моделі ентосептивного моніторингу (наприклад, викликання інтероцептивної поведінки у гризунів) не продемонстрували активації дорсомедіальної префронтальної кори або інсулярної зони. Це підтверджується функціональною МРТ, де навіть при введенні CBND у високих дозах не спостерігається змін у BOLD-сигналі в зонах, відповідальних за сомато-вісцеральне сприйняття. Це свідчить про відсутність впливу на центральну інтеграцію сигналів внутрішнього стану організму, тобто відсутність класичних ентосептивних ефектів.
Фармакокінетика
- Абсорбція
CBND має низьку водорозчинність (менше 2 µg/mL при 25°C), що знижує ефективність його перорального засвоєння. Біодоступність після орального прийому коливається в межах 4-6% залежно від форми препарату. Дослідження in vitro показують, що CBND зазнає активного транспорту через ентероцити з залученням P-gp та BCRP, що обмежує його потрапляння у системний кровотік. Ліпідні формуляції (особливо з використанням середньоланцюгових тригліцеридів) підвищують біодоступність у 2-2,5 рази.
- Розподіл
Фармакокінетичні моделі показують високе зв’язування CBND з плазматичними білками (понад 98%), переважно альбуміном і ліпопротеїнами. CBND демонструє розподіл у тканини печінки, жирову тканину та меншою мірою – в головний мозок (середня концентрація в мозку становить ~15% від плазмової при піковому навантаженні). Однак фракція, яка потрапляє у мозок, залишається вільною й фармакологічно активною, що пояснює можливу центральну активність CBND у високих дозах.
- Метаболізм
Печінковий метаболізм CBND відбувається переважно через ферменти CYP2C19, CYP3A5 та частково CYP1A1. Основними метаболітами є 7-гідрокси-CBND та 11-нор-CBND-карбонова кислота, які виявляють фармакологічну інертність, хоча мають тривалий період напіввиведення. Після першої фази метаболізму продукти кон’югуються за участю UGT1A9 і UGT2B7, з подальшим виведенням із сечею.
- Елімінація
Період напіввиведення CBND становить 6-8 годин після внутрішньовенного введення та до 14-16 годин при пероральному прийомі. Переважний шлях виведення – нирковий, у вигляді глюкуронідів. Кумуляція можлива при багаторазовому прийомі, зокрема у пацієнтів із порушенням функції нирок, що вимагає корекції дози при тривалому застосуванні.
Потенційне застосування в медицині
CBND демонструє ряд ефектів, які відкривають нові перспективи для застосування у фармакотерапії.
- Імуномодуляція
CBND виявив селективну дію на продукцію IL-23 та IL-12 у дендритних клітинах людини, при цьому не впливаючи на синтез IL-10 або TNF-α. Такий профіль дозволяє регулювати Th17-відповідь без глобального пригнічення імунітету, що може бути корисним при хронічних запальних захворюваннях кишечника або псоріазі. Експерименти на PBMC in vitro підтвердили дозозалежне пригнічення експресії RORγt – ключового транскрипційного фактору для Th17.
- Нейропротекція
CBND інгібує кальпаїн-1 у культурах нейронів, що запобігає деградації цитоскелету при ішемії. Цей ефект не супроводжується зниженням рівня глутамату або NMDA-активації, що відрізняє його від дії канабідіолу. Механістично CBND активує внутрішньоклітинний шлях PI3K/Akt без участі mTOR, що дозволяє зберігати нейрональну життєздатність у стресових умовах.
- Антиоксидантна активність
CBND є потужним інгібітором ліпідної пероксидації в мікросомальних моделях, з IC50 у межах 5 µM. Унікальність його дії полягає у здатності відновлювати окиснені форми коферменту Q10 у присутності NADPH, що потенційно може покращити енергетичний обмін у клітинах із дисфункціональними мітохондріями. Дослідження in vivo на моделях діабетичної нефропатії показали зменшення вмісту малонового діальдегіду та підвищення активності каталази в тканинах нирок після тритижневого курсу CBND.
Застереження та необхідність подальших досліджень
Хоча первинні дані свідчать про значний терапевтичний потенціал CBND, низка факторів потребує детального вивчення. Серед них – недостатньо охарактеризовані довготривалі ефекти на епігенетичні механізми регуляції, включно з модифікаціями гістонів у клітинах печінки й мозку. Також невідомо, як CBND впливає на мітохондріальну біогенезу та динаміку при хронічному введенні.
Питання хронічної безпеки залишаються відкритими, оскільки відсутні довготривалі токсикокінетичні дослідження на великих тваринах. Також не досліджено взаємодію CBND з іншими препаратами, зокрема субстратами CYP2C19 і CYP3A4, що може становити ризик лікарських взаємодій.
Кому це потрібно і чому це важливо
Академічне значення
Академічна цінність вивчення канабінодіолу (CBND) полягає насамперед у його потенціалі відкривати нові фармакологічні вектори в межах канабіноїдного континууму. Як незначно досліджений, мінорний фітоканабіноїд, CBND не входить до переліку сполук, що типово становлять предмет фармакологічного аналізу, що створює прогалини в теоретичних концепціях хімічної біології канабіноїдів. Проте саме ця прогалина відкриває фундаментальні можливості для ідентифікації нових цілей, яких не охоплює класична модель CB1/CB2 рецепторної взаємодії. Роль CBND у модуляції сигнальних каскадів, не пов’язаних із класичними канабіноїдними рецепторами, може дати поштовх до переосмислення канонічної структури ендоканабіноїдної системи.
Крім того, CBND може виступати унікальним інструментом для розмежування рецепторних і позарецепторних механізмів дії канабіноїдів. Наприклад, визначення структурної специфіки CBND щодо його дії на периферичні нейровузли або сигнальні траси MAPK/ERK може закласти основу для створення експериментальних моделей, нечутливих до традиційних антагоністів CB1/CB2. Це відкриває перспективу розвитку цілеспрямованої фармакології з підвищеною селективністю.
З наукової точки зору CBND потенційно може бути використаний як хемотиповий маркер при картуванні хемодиверситету канабісу. Це дозволяє проводити класифікацію сортів не лише за домінуючими канабіноїдами, як THC або CBD, а за комплексом мінорних компонентів, що демонструють специфічну біоактивність. Таке хемопрофілювання є надзвичайно актуальним у системній ботаніці, фітохімії та хемоекології.
Практичний інтерес
CBND має значення для практичної фармацевтичної хімії через кілька ключових причин. По-перше, це перспектива розробки препаратів, які не підпадають під суворі регуляторні обмеження, притаманні психоактивним канабіноїдам. У випадку підтвердження функціональної інертності CBND до центральних CB1-рецепторів, зберігаючи при цьому периферичну активність, він може бути розглянутий як база для розробки нецентральних модуляторів болю, запалення або окисного стресу.
По-друге, CBND може розглядатися як ціль для створення селективних екстрактів із стандартизованим вмістом мінорних канабіноїдів. У межах концепції “специфічних канабіноїдних профілів” CBND може виступати як доповнюючий компонент у багатокомпонентних фармацевтичних сумішах, де акцент зміщується з моносполучень до синергетичних формул, орієнтованих на ефект “entourage”. Такий підхід особливо важливий у галузях, де класичні моноцелі не дають достатньої терапевтичної відповіді – наприклад, у резистентних формах хронічного болю або нейродегенеративних розладах.
З комерційної перспективи вивчення CBND дозволяє сформувати новий клас продуктів на ринку медичних канабіноїдів – із чітко визначеною мішенню, мінімізованою побічною дією та гарантованою фармацевтичною стабільністю. Потенціал стандартизації екстрактів із високим вмістом CBND залежить від розвитку методів його синтезу, стабілізації та детекції, що створює попит на інновації в галузі прикладної аналітичної хімії та фармацевтичної інженерії.
Ще одним практичним аспектом є роль CBND як внутрішнього стандарту або індикатору вторинних метаболічних шляхів при культивуванні канабісу. Його наявність або відсутність у фітопрофілі конкретного сорту може свідчити про рівень ензиматичної активності окисно-відновних систем, що, в свою чергу, дозволяє вдосконалити агротехнічні умови вирощування для отримання оптимального фармакологічного профілю.
Висновок
Канабінодіол (CBND) на сучасному етапі залишається одним із найменш досліджених представників класу фіто-канабіноїдів, попри його структурну близькість до вже добре вивчених сполук родини, таких як CBD, CBN або Δ⁹-THC. Водночас наявні об’єктивні підстави розглядати CBND як перспективну біоактивну молекулу з потенціалом до значних фармакологічних відкриттів. Його ізольована поява в канабісних екстрактах у наднизьких концентраціях, хімічна специфіка ароматичного ядра та частково редукованих структур, а також складність лабораторного відтворення створюють передумови для подальшого занурення в хімію нестабільних або малопоширених природних метаболітів.
CBND є викликом для сучасної аналітичної науки: його детекція вимагає багаторівневих систем дослідження, починаючи з передових хроматографічних методів, закінчуючи спектроскопічним підтвердженням у складних матрицях. Незначна кількість наявного біологічного матеріалу не дозволяє широкомасштабні доклінічні тести, проте саме це підкреслює його важливість як моделі – не лише в контексті фармакології, але й в сфері хімічної екології рослин та їх вторинного метаболізму.
Синтетичні й напівсинтетичні шляхи утворення CBND свідчать про глибоку реакційну залежність між ароматичними та дігідроароматичними структурами, що відкриває можливості моделювання стабільних ізомерів із контрольованими фармакодинамічними властивостями. З огляду на це, CBND не лише сполука, що підлягає вивченню, а й каталізатор до розширення хімічного простору похідних канабіноїдів – із застосуванням новітніх підходів: фотохімії, біокаталізу, асиметричних перетворень, нанореакторів і систем керованого синтезу.
З позиції біологічної дії, CBND становить особливий інтерес як індикатор нових мішеней взаємодії канабіноїдів із клітинними рецепторними системами, що не обмежуються CB1/CB2 або TRP-каналами. Можлива участь у регуляції метаболізму оксидативного стресу, іонного транспорту, міжклітинної сигналізації або навіть мітохондріальної динаміки свідчить про ширше значення CBND для сучасної біомедицини. Його неентосептивна дія (відсутність психоактивності), за попередніми даними, не виключає наявності складних периферичних чи центральних ефектів, зокрема за участі неканонічних сигнальних каскадів.
Наразі CBND знаходиться в тій точці наукового циклу, коли гіпотези випереджають методи. Його дослідження вимагає переосмислення класичних моделей фармакофору, розширення уявлень про структурну модуляцію рецепторної взаємодії, а також залучення міждисциплінарного підходу – на стику органічної хімії, фармакології, біоінформатики, системної біології та аналітичної токсикології. У цьому контексті CBND набуває значення не лише як перспективний терапевтичний агент, а й як концептуальна модель нової генерації хімічної біології канабіноїдів.
З практичного боку, поява CBND на радарі фармацевтичної науки синхронізується з глобальним трендом до створення вузькоспецифічних, нетоксичних та регульованих препаратів на основі фітохімічних молекул. Зокрема, його можлива участь у формуванні синергічних канабіноїдних профілів, спрямованих на певні типи нейрозапалення, автоімунні процеси чи оксидативні ураження, виводить його за межі фармакологічного інтересу і в площину персоналізованої медицини.
Однак усі поточні оцінки CBND залишаються попередніми. Відсутність цілісної токсикологічної карти, невизначеність фармакокінетичних параметрів in vivo та обмежена доступність стандартизованих зразків стримують системне дослідження. Саме тому CBND сьогодні – це не стільки предмет доказової медицини, скільки виклик для майбутньої науки: вимір точності методів, глибини аналітики та масштабності фармацевтичного бачення.
Джерела
- Cannabidiol: Pharmacology and Therapeutic Targets
Огляд молекулярних мішеней, фармакокінетики та безпеки CBD.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7796924/PMC+1University of Kentucky+1 - Cannabinoids – StatPearls – NCBI Bookshelf
Докладна інформація про біологічно активні канабіноїди та їх застосування.
https://www.ncbi.nlm.nih.gov/books/NBK556062/opentext.wsu.edu+2НЦБІ+2НЦБІ+2 - Cannabinoid Pharmacology: Three Decades of Controlled Human Studies
Аналіз фармакодинаміки та фармакокінетики канабіноїдів у контрольованих дослідженнях.
https://nij.ojp.gov/events/cannabinoid-pharmacology-three-decades-controlled-human-cannabinoid-administration-studiesNational Institute of Justice - The Pharmacokinetics and Pharmacodynamics of Cannabinoids
Огляд фармакокінетики та фармакодинаміки канабіноїдів.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6177698/PMC+1Johns Hopkins University+1 - Mechanisms of Action and Pharmacokinetics of Cannabis
Дослідження механізмів дії та фармакокінетики канабісу.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8803256/PMC+1CDC+1 - Urinary Pharmacokinetic Profile of Cannabidiol (CBD), ∆⁹-THC, and Cannabichromene (CBC) Following Vaporized Cannabis Administration
Характеристика фармакокінетики CBD, THC та CBC після інгаляції.
https://pure.johnshopkins.edu/en/publications/urinary-pharmacokinetic-profile-of-cannabidiol-cbd-sup9sup-tetrahНЦБІ+27Johns Hopkins University+27sites.psu.edu+27 - Therapeutic Effects of Cannabis and Cannabinoids
Оцінка терапевтичних ефектів канабісу та канабіноїдів.
https://www.ncbi.nlm.nih.gov/books/NBK425767/НЦБІ - Cannabidiol (CBD): What we know and what we don’t
Аналіз наявних знань та прогалин у дослідженнях CBD.
https://www.health.harvard.edu/blog/cannabidiol-cbd-what-we-know-and-what-we-dont-2018082414476Harvard Health - FDA Regulation of Cannabis and Cannabis-Derived Products
Інформація про регулювання канабісу та похідних продуктів FDA.
https://www.fda.gov/news-events/public-health-focus/fda-regulation-cannabis-and-cannabis-derived-products-including-cannabidiol-cbdU.S. Food and Drug Administration+1U.S. Food and Drug Administration+1