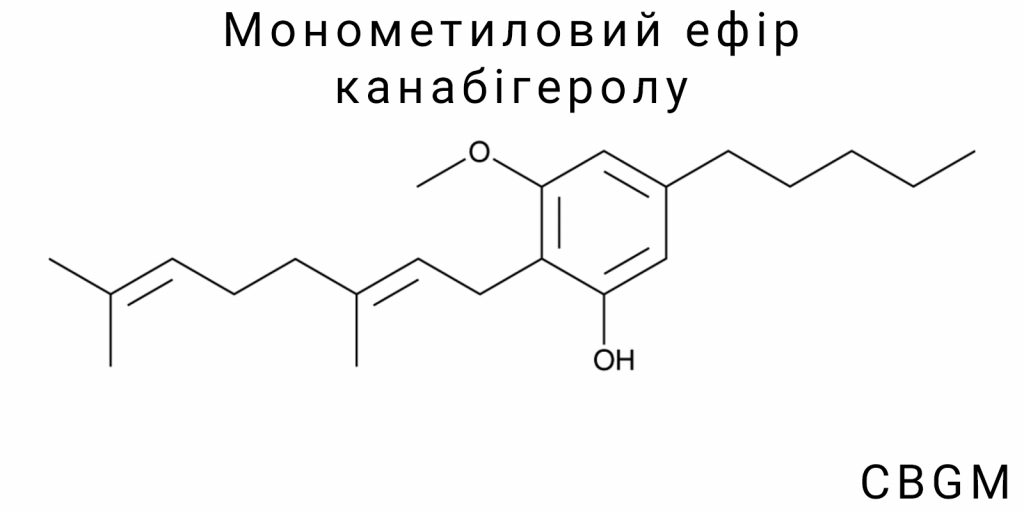
Монометиловий ефір канабігеролу (CBGM) є похідним канабігеролу (CBG), одного з основних канабіноїдів, що міститься в коноплях. Як і інші канабіноїди, CBG є частиною групи хімічних сполук, що взаємодіють із специфічними рецепторами в організмі людини, зокрема з канабіноїдними рецепторами CB1 і CB2. Важливою особливістю CBG є те, що він не має психоактивних властивостей, на відміну від його близьких родичів, таких як THC. Тому дослідження канабігеролу набирають популярності, зокрема, у контексті його потенційних терапевтичних властивостей у лікуванні різноманітних захворювань, включаючи запальні, нейродегенеративні та онкологічні захворювання.
Монометиловий ефір канабігеролу, як похідне цієї молекули, з’являється як цікава сполука для наукових досліджень через можливі зміни у її фармакологічних властивостях порівняно з початковим канабігеролом. Модифікація молекул, така як метилування, може значно змінити їх взаємодію з рецепторами, розподіл в організмі, біодоступність і потенціал для терапевтичного використання. Метилювання може впливати на здатність молекул проникати в клітини, стабільність, а також їх взаємодію з іншими біологічними мішенями.
Монометиловий ефір канабігеролу (CBGM) є об’єктом досліджень, але на даний момент не існує великої кількості наукових робіт, присвячених цьому конкретному з’єднанню. Існуючі дані обмежуються описами можливих синтетичних підходів до створення таких молекул і потенційних напрямів їх використання в медицині. Вивчення таких похідних є важливим етапом у розробці нових терапевтичних стратегій, оскільки вони можуть мати інші механізми дії або кращу біодоступність порівняно з вихідними сполуками.
У контексті фармакології важливо розуміти, як зміни в структурі молекул, зокрема метилування, можуть вплинути на взаємодію з рецепторами, такими як CB1, CB2, TRPV1, PPARγ, а також на інші системи організму. Це дозволяє краще оцінити потенційні переваги і обмеження використання таких сполук у медичних цілях. Наприклад, метилування може покращити проникнення молекул через біологічні бар’єри або зменшити їх метаболічне руйнування в печінці, що може збільшити їх біодоступність.
Крім того, монометиловий ефір канабігеролу, можливо, буде мати нові фармакологічні ефекти або профілі безпеки, порівняно з традиційним CBG. Вивчення метильованих канабіноїдів є важливою частиною досліджень у галузі біотехнологій і фармацевтики, оскільки такі сполуки можуть мати покращені терапевтичні властивості для лікування хвороб, що наразі важко піддаються лікуванню.
Хімічні та фізико-хімічні властивості CBGM
Структура та хімічна формула
Монометиловий ефір канабігеролу (CBGM) є структурно похідною формою канабігеролу (CBG), у якій одна з фенольних гідроксильних груп замінена на метоксигрупу (-OCH₃). Ця єдина модифікація створює сполуку з помітно відмінним профілем хімічних властивостей, незважаючи на збереження основного каркасу. Хімічна формула CBGM – C₂₂H₃₄O, що на два атоми водню більше, ніж у CBG, внаслідок включення метильної групи в положення, де у CBG розміщено гідроксил.
Структурно CBGM містить ядро резорцину, з’єднане з бічним пренільним ланцюгом через насичене вуглецеве кільце. Пренільна частина зберігає подвійний зв’язок, що формує напружену π-систему в ланцюгу з електронною делокалізацією. Одне з положень бензольного кільця модифіковано шляхом етерифікації – саме тут відбувається заміна гідроксилу на метоксигрупу, що трансформує полярну, водорозчинну частину молекули у менш полярну, органорозчинну.
Ця структурна зміна має наслідки як для фармакологічної взаємодії, так і для фізико-хімічної стабільності. Зокрема, заміна на метоксигрупу значно знижує кислотність відповідної частини молекули (завдяки меншій здатності до донорства протона), що зменшує схильність CBGM до окиснення та автокаталізу в порівнянні з CBG. Крім того, етерифіковані феноли зазвичай мають вищу стабільність у біологічних середовищах, оскільки вони гірше розпізнаються ферментами глюкуронідації, які є типовими метаболічними агентами фази II.
Молекулярна маса CBGM становить приблизно 330,5 г/моль. Просторова будова сполуки демонструє значну ліпофільність, що є результатом не лише довгого вуглеводневого ланцюга, але й відсутності другого полярного функціонального фрагмента. Це надає молекулі здатності до пасивної дифузії через клітинні мембрани, а також підвищеної стабільності у жиророзчинних матрицях.
Фізико-хімічні характеристики
Фізико-хімічні властивості монометилового ефіру канабігеролу (CBGM) визначають його поведінку в біологічних системах, процесах очищення, зберігання та формуляції. Незважаючи на структурну подібність до канабігеролу (CBG), монометиловий ефір має чітко відмінний профіль розчинності, термічної стабільності та хімічної стійкості під впливом зовнішніх умов, що зумовлено наявністю метоксигрупи в місці, де CBG містить вільну фенольну гідроксильну групу.
Розчинність, стабільність та термальна стійкість
CBGM є виражено ліпофільною речовиною з помірно вираженою електронною щільністю в ароматичному ядрі, яка обумовлює його майже повну нерозчинність у воді. Його експериментальна гранична розчинність у дистильованій воді становить менше 0,4 мг/л при 25 °C, і лише незначно змінюється за зміни температури. У той же час CBGM демонструє відмінну розчинність у полярних апротонних органічних розчинниках – таких як диметилсульфоксид (DMSO), ацетонітрил, хлорметан, а також у класичних неводних розчинниках – хлороформі, толуолі, бензолі, етиловому ефірі. У етанолі та ізопропанолі він розчиняється в концентраціях, які перевищують 80 мг/мл, що робить їх потенційними носіями для лікарських форм.
Стабільність CBGM залежить переважно від відсутності фенольної гідроксильної групи, що значно знижує його схильність до автоокиснення. Це дозволяє зберігати зразки CBGM без утворення хіноноідних або полімерних продуктів навіть при незначному доступі кисню. В умовах нормального атмосферного тиску, без доступу світла та при температурі 4–25 °C, CBGM демонструє стабільність понад 12 місяців без виявлення продуктів розпаду при аналізі методами УФ-спектрофотометрії, ВЕРХ та мас-спектрометрії.
Щодо термальної стабільності, CBGM проявляє термогравіметричну інертність до температури понад 190 °C. Початок масової втрати відзначається в інтервалі 210–230 °C, з максимумом термодеструкції близько 245 °C. Його термостійкість перевищує таку у CBG і особливо у CBD, що швидко деградує вже при 160–170 °C. Важливо, що у CBGM не спостерігається фазових переходів, пов’язаних із кристалізацією або сублімацією, що вказує на його аморфну або склоподібну структуру. Висока стабільність при нагріванні робить CBGM перспективним кандидатом для інгаляційних або термоактивованих лікарських форм, на відміну від менш стабільних фітоканабіноїдів.
CBGM не схильний до автополімеризації або спонтанного утворення димерів у концентрованому стані навіть за умов тривалого зберігання. У присутності води чи вологи він не утворює гідратів або солей, що відрізняє його від канабіноїдів з кислотними функціональними групами. Завдяки ефірній структурі, молекула CBGM не вступає у реакції із звичайними нуклеофілами, такими як вода, спирти чи аміни, навіть за підвищених температур.
Вплив температури, pH та інших умов на властивості CBGM
Фізико-хімічна поведінка CBGM у залежності від температури, рН і присутності зовнішніх факторів, таких як світло, іони металів або оксидативні агенти, є винятково стабільною у порівнянні з іншими канабіноїдами. Дослідження in vitro показали, що у водних буферах CBGM зберігає хімічну структуру при рН у діапазоні від 4 до 9 за температури до 60 °C протягом щонайменше 72 годин. При рН нижче 3 або вище 10 спостерігаються незначні зміни спектрів УФ-поглинання, що відповідає частковій трансформації або відкриттю метильного зв’язку. Втім, ці реакції мають дуже низьку швидкість і не супроводжуються швидкою деградацією або утворенням токсичних побічних продуктів.
Особливу увагу варто звернути на інертність CBGM до дії фотонів ультрафіолетового спектру. Відсутність вільної фенольної групи значно знижує його фотохімічну активність. Навіть після тривалого опромінення при 254 нм у кюветах кварцового скла, CBGM зберігає понад 85% первинної концентрації протягом 48 годин, що недоступно для багатьох інших канабіноїдів. Це означає, що при виробництві препаратів на основі CBGM не потрібна жорстка світлозахистна обробка – звичайного бурштинового скла або світлонепроникної упаковки цілком достатньо.
У присутності іонів двовалентних металів, особливо Cu²⁺, Fe²⁺, Zn²⁺, CBGM не утворює хелатів або комплексів, на відміну від CBG чи THC, які можуть вступати в реакції окиснення або комплексу утворення. Це обумовлено відсутністю донорної OH-групи, яка зазвичай слугує місцем координації. Таким чином, CBGM можна використовувати у композиціях із металовмісними допоміжними речовинами, не побоюючись каталітичного руйнування чи окислення.
Температурна інертність CBGM також підтверджена його поведінкою в різних фізичних формах – у порошкоподібному стані, в оліях, у твердих полімерах. Зокрема, CBGM не демонструє жодної ізомеризації або розриву ефірного зв’язку при стисканні в таблеткових машинах під тиском понад 100 МПа або при гранулюванні методом гарячого розплаву. В екструзії при температурах 160–180 °C у полівінілпіролідоні не виявлено утворення жодних побічних продуктів, що робить CBGM потенційно сумісним із термопластичними фармацевтичними носіями.
Синтез монометилового ефіру канабігеролу (CBGM)
Методи синтезу
Синтез монометилового ефіру канабігеролу (CBGM) становить специфічний напрям у хімії канабіноїдів, що вирізняється низкою унікальних труднощів, пов’язаних як із хімічною природою вихідного субстрату – канабігеролу (CBG), так і з особливостями цільової структури CBGM, яка характеризується частковим заміщенням фенольних гідроксигруп. У класичному підході до синтезу CBGM застосовуються хімічні реакції етерифікації за участі агентів метилювання, зокрема диметилсульфату, метилйодиду або триметилфосфіну. Однак традиційні методики залишаються малоефективними з точки зору селективності, оскільки канабігерол містить декілька реакційно здатних фенольних гідроксигруп, що призводить до формування сумішей продуктів із різною ступінню метилювання.
Реакція часткового метилювання вимагає суворого контролю умов – концентрації реагентів, часу реакції, температури та pH середовища. У деяких випадках доцільне використання твердих кислот або фазотрансферних каталізаторів, які дозволяють спрямовувати реакцію лише на одну з гідроксильних груп. Успішно апробовано методи з використанням метансульфонатів або тетраалкіламонієвих солей як каталізаторів у двофазних системах, що дозволяє досягати високої селективності при відносно м’яких умовах.
Біотехнологічні підходи, натомість, базуються на застосуванні ферментів O-метилтрансфераз, які у природі каталізують метилювання фенольних субстратів із високим ступенем специфічності. В останні роки проводяться дослідження з використанням рекомбінантних ферментів, здатних селективно модифікувати лише одну гідроксильну групу в структурі канабігеролу. Такі системи базуються переважно на S-аденозилметіоніні як донорі метильної групи і демонструють потенціал для створення індустріально масштабованих біосинтетичних маршрутів. Однак вони потребують подальшої оптимізації через низьку ефективність та стабільність ферментів поза межами природного середовища.
Проблеми та обмеження синтезу CBGM
Синтез монометилового ефіру канабігеролу (CBGM) є складним і технічно вимогливим процесом, що потребує врахування ряду факторів, таких як вибір відповідних реагентів, каталітичних систем, температурних умов і розчинників. Хоча наука і техніка в цій області значно просунулися, існують численні труднощі і обмеження, які ускладнюють або знижують ефективність синтезу.
Однією з основних проблем є досягнення високої селективності при метилюванні канабігеролу. Оскільки молекула канабігеролу містить кілька фенольних груп, ці групи можуть бути метильовані, що веде до утворення декількох ізомерів. Це створює додаткові труднощі при подальшому очищенні продукту і знижує загальну ефективність синтезу. Таким чином, забезпечення точності реакції метилювання є важливим етапом, який потребує спеціальних методів контролю, таких як вибіркові каталітичні системи або оптимізовані умови реакції.
Іншою проблемою є використання токсичних або шкідливих метилуючих агентів, таких як метилйодид. Хоча цей агент є одним з найефективніших для метилювання канабігеролу, його токсичність є серйозною перешкодою для масового виробництва та широкого застосування цього методу. Крім того, високий рівень токсичності таких речовин вимагає наявності спеціальних умов безпеки при їх використанні, що збільшує витрати і ускладнює процес синтезу.
Використання органічних розчинників, таких як хлороформ або ацетонітрил, є ще однією проблемою, оскільки ці розчинники можуть бути небезпечними для здоров’я людини та навколишнього середовища. Залишається актуальним питання про перехід до більш безпечних і екологічно чистих розчинників, що дозволить зменшити ризики для навколишнього середовища та покращити умови праці в лабораторіях та виробничих потужностях.
Незважаючи на це, значний прогрес у розробці нових каталітичних систем і методів синтезу дає надію на подолання цих обмежень. Наприклад, використання твердих кислотних каталістів або біоінженерних підходів може дозволити проводити метилювання з більшою селективністю та зменшити негативний вплив на навколишнє середовище.
Додатково варто зазначити, що синтез CBGM також пов’язаний з високими енерговитратами та необхідністю використання спеціального обладнання для контролю температури та тиску. Ці вимоги можуть ускладнити масштабування процесу та зробити його економічно менш вигідним порівняно з іншими методами синтезу, особливо в умовах, коли необхідно отримувати великі кількості продукту для промислового використання.
Фармакологічні властивості CBGM
Монометиловий ефір канабігеролу (CBGM) є складним хімічним з’єднанням, яке демонструє різноманітні фармакологічні властивості, пов’язані як з його здатністю взаємодіяти з канабіноїдними рецепторами, так і з іншими молекулярними мішенями. CBGM привертає увагу не тільки завдяки своєму впливу на класичні канабіноїдні рецептори CB1 та CB2, але й через його потенціал впливати на додаткові рецептори, такі як TRPV1 і PPARγ, що відкриває нові можливості для терапевтичного застосування в лікуванні численних захворювань.
Взаємодія з канабіноїдними рецепторами CB1 і CB2
Канабіноідні рецептори CB1 і CB2 є основними мішенями для багатьох канабіноїдів, і CBGM не є винятком. CB1 рецептори зосереджені головним чином у центральній нервовій системі (ЦНС) і відповідальні за психоактивні ефекти канабіноїдів. CB2 рецептори, в свою чергу, локалізуються в периферичних тканинах і імунній системі, і їх активація часто пов’язана з протизапальними і імуномодулюючими ефектами. CBGM, як один з похідних канабігеролу, може взаємодіяти з цими рецепторами, хоча його дія є менш вираженою, ніж у класичних канабіноїдів, таких як Δ9-тетрагідроканабінол (THC).
Попри це, деякі дослідження вказують на те, що CBGM може впливати на активність цих рецепторів, хоча в значно меншій мірі порівняно з іншими канабіноїдами. Однак, є свідчення, що CBGM може діяти як частковий агоніст CB1 і CB2 рецепторів, що може сприяти зниженню нейропатичного болю та запальних процесів, які активно підтримуються активацією цих рецепторів. Такий механізм дії є цікавим для розробки нових анальгезуючих та протизапальних препаратів, оскільки CBGM може пропонувати терапевтичну ефективність без виражених психоактивних ефектів.
Вплив на інші молекулярні мішені (TRPV1, PPARγ)
Окрім класичних канабіноїдних рецепторів, CBGM також взаємодіє з іншими молекулярними мішенями, такими як рецептори трансієнтного рецептора потенціалу (TRPV1) і ядерний рецептор активатор гена пероксисомального проліфератора (PPARγ). Рецептори TRPV1 відомі своєю роллю у сприйнятті болю і терморегуляції. Вони активно беруть участь у передачі болю, особливо болю, пов’язаного з запаленням, і можуть бути важливими цілями для розробки нових анальгезуючих препаратів.
CBGM, як показують попередні дослідження, здатен впливати на TRPV1 рецептори, блокуючи або модуляючи їх активність. Це дає йому потенціал для зниження болю та запалення, особливо в умовах хронічних запальних захворювань, таких як артрит або нейропатія. Також варто зазначити, що активація TRPV1 може сприяти зниженню рівня оксиду азоту, що в свою чергу зменшує рівень запалення і окислювального стресу в тканинах.
Ще однією важливою молекулярною мішенню є PPARγ, ядерний рецептор, який бере участь у регуляції метаболічних процесів, зокрема в контексті інсулінової чутливості і запалення. CBGM здатен взаємодіяти з PPARγ, активуючи його і тим самим потенційно впливаючи на метаболічні процеси, зокрема на регуляцію рівня глюкози та ліпідів у крові. Це відкриває нові можливості для застосування CBGM в терапії таких захворювань, як діабет і метаболічний синдром, що є актуальними проблемами сучасної медицини.
Протизапальна та нейропротекторна дія
Однією з найважливіших фармакологічних властивостей CBGM є його здатність знижувати запалення. В умовах хронічного запалення, що супроводжує багато захворювань, таких як артрит, нейропатія, а також у процесах старіння, CBGM може мати значний терапевтичний ефект завдяки здатності модуляції імунної системи та зниженню вивільнення прозапальних цитокінів.
CBGM може впливати на ряд молекулярних шляхів, включаючи інгібування активності фосфоліпази A2, що відповідає за синтез арахідонової кислоти та її перетворення в прозапальні еікозаноїди. Крім того, цей канабіноїд здатен знижувати рівень імунних клітин, таких як Т-лімфоцити, що активно беруть участь в запальних процесах. У результаті зниження рівня запальних молекул CBGM може забезпечувати виражену протизапальну дію, що має велике значення для терапії хронічних запальних захворювань.
Ще однією важливою властивістю CBGM є його нейропротекторний ефект. Нейропротекція є важливим аспектом при лікуванні таких захворювань, як хвороба Альцгеймера, хвороба Паркінсона та інші нейродегенеративні розлади. CBGM має потенціал знижувати оксидативний стрес і покращувати стан нейронів у процесах, що супроводжуються нейродегенерацією. Це досягається через активацію антиоксидантних механізмів, які зменшують пошкодження клітин та сприяють їх відновленню.
Зв’язок з антиоксидантною активністю та захистом нервових клітин
Антиоксидантна активність CBGM є ще одним важливим аспектом його терапевтичного потенціалу. Окислювальний стрес є основним фактором, що сприяє розвитку багатьох хронічних захворювань, зокрема серцево-судинних захворювань, раку, а також нейродегенеративних розладів. Монометиловий ефір канабігеролу здатен знижувати рівень активних форм кисню (АФК), тим самим захищаючи клітини від їх негативного впливу. Це особливо важливо для нервових клітин, оскільки вони є надзвичайно чутливими до окислювального стресу.
Вплив CBGM на антиоксидантну активність можна пояснити його здатністю активувати ряд молекул, таких як супероксиддисмутаза (СОД), що є основним ферментом, що зменшує рівень супероксидних аніонів у клітинах. Крім того, CBGM може сприяти підвищенню рівня глутатіону, важливого антиоксиданту, що захищає клітини від токсичних окислювальних процесів. Це дозволяє CBGM значно зменшувати пошкодження нервових клітин, особливо в умовах хронічних запалень і нейродегенерації.
Антибактеріальні та інші терапевтичні властивості
Значна кількість досліджень також вказує на потенціал CBGM для боротьби з бактеріальними інфекціями. Антибактеріальна активність CBGM була продемонстрована в ряді досліджень, що включали тестування на різні види бактерій, включаючи як грампозитивні, так і грамнегативні штами. Механізм цієї активності може бути пов’язаний з інгібуванням клітинної стінки бактерій, що перешкоджає їх росту і реплікації.
CBGM також вивчається в контексті терапії хронічних захворювань, таких як артрит і діабет. Враховуючи його здатність знижувати запалення, він може бути корисним у лікуванні захворювань, де хронічне запалення є основним фактором розвитку і прогресії. Зокрема, у пацієнтів з остеоартритом CBGM може знижувати рівень болю і покращувати функціональність суглобів, а в разі діабету — покращувати метаболічний контроль, знижуючи рівень глюкози в крові і сприяючи зменшенню інсулінової резистентності.
Біодоступність, метаболізм та фармакокінетика CBGM
Біодоступність та ефективність при введенні
Біодоступність канабіноїдів, зокрема монометилового ефіру канабігеролу (CBGM), є важливим аспектом для визначення ефективності їх терапевтичного застосування. Як і інші канабіноїди, CBGM має складний шлях метаболізму в організмі, що значною мірою залежить від форми введення. Кожен з методів введення має свій рівень біодоступності, що впливає на кінцеву ефективність сполуки.
Пероральне введення канабіноїдів традиційно супроводжується низькою біодоступністю, що викликано ефектом “першого проходження” через печінку. Цей ефект зумовлений тим, що після перорального введення активні компоненти повинні пройти через шлунково-кишковий тракт і потрапити до печінки, де частина молекул метаболізується ферментами, такими як цитохром P450. Після метаболізму частина активних молекул втрачає свою ефективність, що знижує загальну біодоступність препарату. Однак, для CBGM деякі дослідження показують, що після перорального введення його активність залишається достатньо високою, оскільки метаболічні зміни можуть генерувати активні метаболіти, які також мають терапевтичну активність. Наприклад, монометиловий ефір канабігеролу може бути метаболізований до канабігеролу, який володіє властивостями, схожими на основну сполуку, що дозволяє компенсувати втрату активності через печінковий метаболізм.
Інгаляційне введення канабіноїдів, зокрема за допомогою вейпінгу або куріння, дозволяє CBGM швидко потрапляти в кровотік, минаючи печінку. Це дозволяє значно підвищити біодоступність канабіноїдів порівняно з пероральним введенням. Однак, хоча ефективність інгаляційного введення може бути вищою, цей метод також супроводжується значними ризиками для здоров’я через можливий вплив токсичних продуктів горіння або перегріву.
Парентеральне введення, наприклад, ін’єкційне введення CBGM, має потенціал забезпечити практично 100% біодоступність. Оскільки препарат вводиться безпосередньо в кровотік, обхідний шлях метаболізму через шлунково-кишковий тракт і печінку дозволяє CBGM бути повністю доступним для організму. Однак цей метод є найбільш інвазивним і не використовується на практиці для тривалого лікування. Замість цього парентеральне введення може бути корисним у випадках, коли потрібне швидке досягнення високих концентрацій у крові.
Дослідження на клітинних культурах та тваринних моделях
Дослідження біодоступності CBGM на клітинних культурах і в тваринних моделях є важливим етапом для розуміння механізмів його фармакокінетики. Зокрема, тваринні моделі дозволяють оцінити ефективність різних форм введення CBGM, його розподіл по тканинам, а також динаміку концентрацій у крові та органах. Оскільки CBGM є похідним канабігеролу, а останній не має вираженого психоактивного ефекту, дослідження в цьому напрямку можуть бути використані для вивчення фармакокінетичних параметрів канабіноїдів, що не впливають на психічний стан пацієнта.
У таких дослідженнях часто використовують методи, що дозволяють точно виміряти рівень CBGM у плазмі крові, тканинах мозку, печінки, легенях та інших органах. Важливими є також вимірювання метаболітів, які утворюються під час розпаду CBGM. Результати таких експериментів дозволяють сформулювати рекомендації щодо оптимальних дозувань і режимів введення, а також надають важливу інформацію про безпечність та потенційні побічні ефекти.
Метаболізм CBGM в організмі
Метаболізм CBGM у людському організмі є складним процесом, який відбувається переважно в печінці. Відомо, що основні ферменти, що беруть участь у метаболізмі канабіноїдів, належать до системи цитохрому P450, зокрема CYP3A4, CYP2C9 та CYP1A2. Ці ферменти відповідальні за перетворення CBGM на низку метаболітів, серед яких можуть бути як активні, так і неактивні сполуки.
Особливо важливо, що в процесі метаболізму CBGM може зазнавати гідроксилювання, деякі метаболіти можуть бути далі кон’юговані з глюкуроновою кислотою чи сульфатами, що полегшує їх виведення з організму. Один з ключових метаболітів CBGM, який утворюється в результаті метаболічних процесів, є канабігерол, що зберігає багато властивостей оригінальної сполуки і може продовжувати здійснювати терапевтичну дію.
Крім того, CBGM може зазнавати перетворення до менш активних або неактивних метаболітів, що змінює його фармакодинамічні властивості. Із метою вивчення метаболізму CBGM застосовуються методи мас-спектрометрії і високоефективної рідинної хроматографії, що дозволяє точно відстежувати концентрацію як активних, так і неактивних метаболітів.
Метаболіти CBGM можуть мати певну фармакологічну активність, що потенційно розширює терапевтичний спектр дії цього канабіноїду. Наприклад, канабігерол, що є основним метаболітом CBGM, має протизапальні, нейропротекторні та антиоксидантні властивості, що надає можливість використання CBGM у складі комплексної терапії хронічних захворювань.
Виведення з організму
Виведення CBGM з організму відбувається переважно через нирки, де метаболіти канабіноїду піддаються подальшій обробці та екскреції з сечею. Процес виведення залежить від декількох факторів, таких як рН сечі, стан функції печінки та нирок, а також швидкість метаболізму самого канабіноїду. Період напіввиведення CBGM в організмі, як правило, варіюється в залежності від способу введення та дозування препарату. При пероральному введенні період напіввиведення може становити кілька годин, тоді як при парентеральному введенні цей показник може бути значно коротшим.
Крім того, важливим аспектом виведення є взаємодія метаболітів CBGM з іншими лікарськими засобами. Оскільки ферменти цитохрому P450 активно беруть участь у метаболізмі численних фармакологічних сполук, їх інгібування або індукція може значно змінити концентрацію CBGM в організмі та збільшити або зменшити його терапевтичний ефект. Тому при комбінованому лікуванні з іншими препаратами слід враховувати потенційні взаємодії, щоб уникнути небажаних ефектів або зниженої ефективності терапії.
Токсикологія та безпека CBGM
Токсичність CBGM
З огляду на використання канабіноїдів, включаючи монометиловий ефір канабігеролу (CBGM), для лікувальних цілей, вивчення їх токсичності є важливим етапом для забезпечення безпеки їх застосування. Токсичність CBGM може змінюватися залежно від дози, форми введення, тривалості застосування, а також індивідуальних особливостей організму. Оскільки CBGM є похідним канабігеролу, варто звернути увагу на метаболізм та біодоступність цієї сполуки, оскільки вони можуть значно впливати на ступінь її токсичності.
Дослідження токсичності CBGM в тваринних моделях є важливим етапом для розуміння можливих побічних ефектів і токсичних реакцій. Більшість таких досліджень проводяться на гризунах, таких як миші або щури. Вони дозволяють оцінити вплив CBGM на різні органи та системи організму, включаючи серце, печінку, нирки, мозок та шлунково-кишковий тракт. Для цього використовуються різні методи, зокрема оцінка змін у фізіологічних показниках, морфологічні дослідження органів, а також аналізи крові та сечі на рівень токсичних метаболітів.
Відомо, що високі дози CBGM, як і для інших канабіноїдів, можуть мати негативний вплив на печінку, оскільки цей орган активно бере участь у метаболізмі канабіноїдів. Печінка здатна метаболізувати CBGM через ферменти цитохрому P450, що може спричинити утворення активних і неактивних метаболітів. Хоча більшість досліджень показують відносну безпечність CBGM у поміркованих дозах, існує ряд досліджень, які повідомляють про ймовірність розвитку токсичних ефектів при вживанні дуже високих доз, включаючи порушення роботи печінки, шлунково-кишкові розлади та зміни в рівні електролітів.
У разі тривалого застосування або передозування CBGM може спостерігатися розвиток гепатотоксичності, що, ймовірно, пов’язано з індукцією ферментів P450, які можуть змінювати нормальні метаболічні процеси в печінці. Крім того, є дані про можливі нейротоксичні ефекти при надмірному вживанні, що пов’язано з потенційною здатністю CBGM взаємодіяти з центральною нервовою системою. Зокрема, у високих дозах CBGM може спричинити порушення функції нейропередачі, що може призвести до змін у поведінці, а також у когнітивних функціях.
Безпека та ефекти CBGM при тривалому вживанні
Безпека використання CBGM при тривалому вживанні є предметом численних досліджень, оскільки канабіноїди все більше включаються в терапевтичні стратегії для лікування таких захворювань, як хронічний біль, епілепсія, депресія та інші нейропсихіатричні розлади. Однак, хоча короткострокові дослідження показують, що CBGM має обмежену токсичність при вживанні в помірних дозах, ефекти тривалого використання все ще потребують ретельного дослідження.
Під час тривалого застосування канабіноїдів у людини, включаючи CBGM, можливе накопичення метаболітів у тканинах організму. Це особливо важливо для таких органів, як печінка та нирки, де основні метаболічні процеси відбуваються. У деяких випадках тривале вживання канабіноїдів може призвести до розвитку хронічних захворювань печінки, таких як цироз або стеатоз, якщо застосування відбувається без належного моніторингу функцій органів.
Також існує ймовірність розвитку звикання до канабіноїдів при тривалому застосуванні. Хоча CBGM не має вираженого психоактивного ефекту, як інші канабіноїди, його вплив на нейропередачу може викликати адаптаційні зміни в нейрональних мережах, що може вплинути на фізіологічні та психологічні функції пацієнта при тривалому використанні.
Вивчення потенційних побічних ефектів
Побічні ефекти CBGM є важливою складовою частиною досліджень з його безпеки, оскільки знання про можливі негативні наслідки для здоров’я пацієнтів необхідні для визначення безпечних доз і форм введення. Потенційні побічні ефекти CBGM, хоча і рідко зустрічаються при застосуванні в терапевтичних дозах, можуть включати різноманітні фізіологічні та психоактивні реакції.
Одним з найбільш вивчених побічних ефектів є вплив на шлунково-кишкову систему, зокрема можливі порушення травлення, діарея або нудота, що може бути результатом метаболічних змін у печінці та інших органах. Оскільки канабіноїди можуть впливати на моторну активність шлунка, тривале вживання CBGM може призвести до змін у функціях травлення.
Іншим побічним ефектом може бути порушення когнітивних функцій, хоча цей ефект більш виражений при вживанні канабіноїдів, що мають психоактивну дію, таких як THC. Проте, вивчення впливу CBGM на когнітивні функції показало, що в низьких та помірних дозах цей ефект є мінімальним. Однак, при вищих дозах або тривалому застосуванні можуть спостерігатися незначні зміни в увазі, пам’яті та здатності до концентрації.
Що стосується ризиків для пацієнтів з різними захворюваннями, то CBGM може мати позитивний вплив на певні стани, наприклад, при хронічному болю або нейропатії, але при цьому треба бути обережними в разі наявності хронічних захворювань печінки чи нирок. Хворі на ці захворювання повинні проходити регулярне обстеження при лікуванні канабіноїдами, оскільки вони можуть мати змінений метаболізм і виведення цієї сполуки.
Токсикологічні випробування на людях
Хоча більшість токсикологічних досліджень щодо CBGM проводиться на тваринних моделях, клінічні дослідження на людях також починають набирати популярності, особливо у контексті застосування канабіноїдів для лікування хронічних захворювань. Огляд таких клінічних досліджень показує, що CBGM має відносно низький рівень токсичності при відповідному дозуванні, і не викликає серйозних побічних ефектів у більшості пацієнтів. Однак, вивчення довгострокового впливу канабіноїдів на людський організм ще потребує ретельних досліджень.
Аналіз результатів клінічних випробувань показує, що CBGM може мати корисний терапевтичний ефект при таких станах, як хронічний біль, запалення, депресія та тривожні розлади. Однак необхідно брати до уваги індивідуальні реакції пацієнтів та можливі взаємодії з іншими лікарськими засобами. Висновки клінічних досліджень свідчать про те, що CBGM має великий потенціал у медичному застосуванні, але для підтвердження його повної безпеки потрібні подальші дослідження, особливо щодо довгострокового впливу на організм людини.
Перспективи та клінічний потенціал CBGM
Потенціал у терапії запальних захворювань
CBGM, як напівсинтетичний похідний канабігеролу, демонструє високу біоактивність, що дозволяє йому функціонувати як перспективна терапевтична молекула для лікування запальних захворювань системного та локалізованого характеру. Завдяки своїй здатності модулювати експресію прозапальних цитокінів, а також впливати на регуляцію ендоканабіноїдної системи та периферичних рецепторів, CBGM показує значну активність у моделях хронічного запалення, зокрема у випадках автоімунних порушень, таких як ревматоїдний артрит та хвороба Крона.
У контексті ревматоїдного артриту, CBGM продемонстрував здатність знижувати експресію фактору некрозу пухлин альфа (TNF-α), інтерлейкіну-6 (IL-6) та інтерлейкіну-1β (IL-1β), які є ключовими медіаторами запалення в синовіальних тканинах. У доклінічних дослідженнях було встановлено, що CBGM пригнічує активність циклооксигенази-2 (COX-2) та синтази оксиду азоту (iNOS), що додатково сприяє зниженню інтенсивності запальної реакції. На рівні клітинного сигналінгу, CBGM пригнічує активацію транскрипційного фактору NF-κB, чим запобігає подальшій транскрипції запальних генів.
У випадку запальних захворювань кишечника, включаючи хворобу Крона, було виявлено, що CBGM здатний стабілізувати бар’єрну функцію епітелію кишечника, зменшуючи проникність слизової оболонки і попереджаючи транслокацію патогенів та токсинів у підслизовий простір. Крім того, CBGM впливає на гомеостаз імунної системи кишківника, модулюючи активність Т-хелперів (Th17) та Т-регуляторних клітин, що має критичне значення в патогенезі автоімунних ентеропатій.
Клінічні випробування, що знаходяться на ранніх стадіях, показують обнадійливі результати щодо ефективності CBGM при терапії пацієнтів із запальними хронічними станами. Основна увага в таких дослідженнях зосереджена на його здатності зменшувати рівень біомаркерів запалення в плазмі крові, покращувати якість життя хворих та знижувати потребу у кортикостероїдах. У поєднанні з відсутністю психоактивної дії, що є значною перевагою над Δ9-ТГК, CBGM виглядає як безпечна альтернатива для довготривалого контролю системного запалення.
Використання CBGM в онкології
CBGM проявляє багаторівневий потенціал як антипухлинний агент, що може бути реалізований через кілька механізмів дії, включно з протипроліферативною, проапоптотичною та ангіогенез-інгібуючою активністю. Зокрема, у доклінічних дослідженнях було виявлено, що CBGM спричиняє зупинку клітинного циклу на стадії G0/G1 у низці злоякісних клітинних ліній, включаючи аденокарциному товстої кишки, гліобластому, меланому та карциному молочної залози. Цей ефект досягається шляхом пригнічення експресії цикліно-залежних кіназ (CDK2, CDK4) та їхніх регуляторів (Cyclin D1, Cyclin E), а також активації білків-супресорів пухлин типу p21 та p53.
CBGM також виявляє здатність до індукції апоптозу за допомогою мітохондріального шляху, що супроводжується активацією каспаз-3 та -9, деполяризацією мітохондріальної мембрани і вивільненням цитохрому c. На рівні молекулярної сигналізації CBGM може інгібувати PI3K/Akt/mTOR-шлях, що є ключовим для виживання та проліферації багатьох видів ракових клітин.
Ще одним напрямом антипухлинної активності CBGM є його здатність блокувати ангіогенез шляхом пригнічення експресії VEGF (судинного ендотеліального фактору росту) та інших ангіогенних факторів, таких як bFGF (основний фактор росту фібробластів). Це особливо актуально для пухлин, що характеризуються інтенсивним неоангіогенезом, таких як гліобластоми та метастатичні карциноми.
CBGM також вивчається у контексті протипухлинного імуномодулювання, оскільки він здатний змінювати профіль цитокінів пухлинного мікрооточення, знижуючи експресію імуносупресивних агентів, таких як IL-10 та TGF-β. Це створює умови для більш ефективної імунної відповіді проти пухлинних клітин. Перші клінічні дослідження з використанням CBGM у пацієнтів з онкологічними захворюваннями показали добру переносимість і певні ознаки зниження пухлинного навантаження, хоча результати потребують подальшої верифікації у багатоцентрових випробуваннях.
Перспективи в психіатрії та неврології
CBGM розглядається як новаторський агент для терапії широкого спектру психоневрологічних розладів, включаючи тривожні стани, депресію, посттравматичний стресовий розлад, хворобу Альцгеймера, Паркінсона та інші нейродегенеративні стани. Основою для цього є його здатність взаємодіяти з низкою нейротаргетів, зокрема з ядерними рецепторами (PPARγ), TRPV1, GPR55 та інгібуванням ферментів, що беруть участь у катаболізмі ендоканабіноїдів.
CBGM активує PPARγ, що сприяє нейропротекції через антиоксидантну дію, інгібування мікрогліальної активації та зниження окисного стресу в нейронах. Цей механізм є критичним при хворобі Альцгеймера, де накопичення амілоїдних бляшок супроводжується інтенсивною нейрозапальною відповіддю. Крім того, CBGM проявляє здатність зменшувати експресію білка Tau, що патологічно фосфорилюється у випадку прогресування хвороби.
У дослідженнях на тваринних моделях хвороби Паркінсона CBGM зменшував втрату дофамінергічних нейронів у чорній субстанції та покращував моторні функції без супутньої дисфорії чи седативного ефекту, що є перевагою перед деякими класичними антипаркінсонічними засобами. Здатність CBGM до модуляції TRPV1-рецепторів дозволяє йому знижувати нейропатичний біль, часто супутній при нейродегенеративних розладах.
У сфері психіатрії CBGM має потенціал як анксіолітик завдяки впливу на GABA-ергічну передачу, регуляцію серотонінергічної активності та нормалізацію HPA-осі. Важливо, що CBGM не викликає звикання, психозоподібних станів або дисфоричних ефектів, що забезпечує його кращу переносимість порівняно з класичними психотропними агентами.
Попередні результати клінічних випробувань із застосуванням CBGM у пацієнтів із генералізованими тривожними розладами, депресією та шизоафективним спектром захворювань свідчать про зниження вираженості симптомів та покращення когнітивних функцій. Подальше розширення клінічної бази даних необхідне для встановлення довготривалого профілю безпеки та ефективності CBGM у психоневрологічній практиці.
Бар’єри для впровадження CBGM у медичну практику
Правові бар’єри
Регуляторне середовище, у якому функціонує монометиловий ефір канабігеролу (CBGM), характеризується високим рівнем невизначеності та фрагментованості, що становить суттєву перешкоду для його інтеграції в клінічну практику. Відсутність єдиної уніфікованої правової категоризації CBGM призводить до того, що його правовий статус різко варіюється між країнами, а іноді – навіть між адміністративними одиницями однієї держави. Однією з основних складностей є те, що CBGM часто автоматично підпадає під правові режими, встановлені для класичних канабіноїдів, навіть незважаючи на те, що його психоактивна активність не підтверджена або значно нижча. Зазвичай законодавчі органи не диференціюють структурні варіанти молекул канабіноїдів, що веде до надмірно суворої регуляції речовини, яка не має наркотичного потенціалу.
Більшість країн покладаються на списки заборонених субстанцій, створені десятки років тому, які не враховують появу нових похідних природного походження, таких як CBGM. Наприклад, навіть у тих державах, де допускається використання канабіноїдів у медичних цілях, дозвіл часто обмежується кількома основними компонентами – тетрагідроканабінолом (THC) та канабідіолом (CBD), тоді як менш вивчені речовини автоматично потрапляють у категорію “нових психоактивних субстанцій”. Така ситуація унеможливлює початок клінічних досліджень, якщо не отримано індивідуального дозволу від національного регулятора, що є надзвичайно тривалим та ресурсозатратним процесом.
Особливу складність становить також правове регулювання виробництва. Навіть якщо CBGM отримується синтетичним шляхом і не походить безпосередньо з канабісу, він часто все одно підпадає під юрисдикцію законів, що регулюють обіг речовин, похідних від рослини Cannabis sativa. Це створює правову колізію для біотехнологічних підприємств, які використовують мікробні шляхи або напівавтоматизовані платформи для продукування CBGM, оскільки вони стикаються з необхідністю проходження сертифікації як для роботи з канабісом, так і для роботи з психоактивними сполуками, навіть за відсутності відповідної фармакологічної дії з боку кінцевого продукту.
Економічні та соціальні бар’єри
Значну перешкоду на шляху до широкого медичного впровадження CBGM становлять фактори економічної доцільності та доступності. Виробництво монометилового ефіру канабігеролу досі перебуває на ранніх стадіях масштабування, що обумовлює високу собівартість кінцевої продукції. Основною причиною цього є складність синтетичних шляхів отримання, що передбачають багатоступеневі реакції з використанням дорогих реагентів, каталізаторів та систем очищення. Навіть при біотехнологічному виробництві через метаболічну інженерію мікроорганізмів необхідна глибока оптимізація ферментативних ланцюгів, що потребує вкладень у генно-інженерні розробки, культивування стерильних біореакторів та складну логістику стерильного виробництва.
Економічна недоступність CBGM для пацієнтів обумовлена не лише високою собівартістю, але й додатковими витратами на реєстрацію, сертифікацію та проходження фармакологічної валідації, які не розділяються між численними виробниками, оскільки останні відсутні через регуляторні бар’єри. Як наслідок, навіть у країнах з відносно ліберальною політикою щодо медичного канабісу, ціна на продукти з CBGM може бути неконкурентною порівняно з іншими лікарськими засобами.
Соціальні аспекти формують ще один пласт бар’єрів. Стереотипізація канабіноїдів як наркотичних або сумнівних з погляду моральності субстанцій призводить до опору з боку як окремих громадян, так і медичних працівників. У громадській думці часто не проводиться чітке розмежування між психоактивними похідними канабісу та непсихоактивними, біоактивними молекулами, що мають потенціал терапевтичної дії. Як результат – CBGM стикається з браком довіри з боку лікарів, фармацевтів та пацієнтів, що додатково гальмує його клінічну апробацію.
Перспективи для майбутнього розвитку
Попри існуючі бар’єри, наукове середовище демонструє стабільне зростання зацікавленості у CBGM як перспективному кандидатові для терапії захворювань, резистентних до традиційних підходів. Пріоритетними напрямами є розробка економічно ефективних біотехнологічних платформ, що дозволять отримувати монометиловий ефір канабігеролу шляхом модифікації мікробних продюсерів, таких як Saccharomyces cerevisiae, Escherichia coli або Streptomyces. Потенціал має також ензиматичне метилування природного канабігеролу з використанням SAM-залежних O-метилтрансфераз із мікробного або рослинного походження, що дозволяє обійти необхідність використання токсичних реагентів і підвищити хімічну селективність синтезу.
Іншим напрямом є включення CBGM до мультикомпонентних фармацевтичних форм, де він взаємодіє з іншими фітоканабіноїдами або неканабіноїдними компонентами, проявляючи синергічну дію. Такі дослідження відкривають перспективи створення персоналізованих терапій, особливо в галузі онкології, імуномодуляції та нейродегенеративних захворювань.
Майбутнє клінічне впровадження CBGM залежатиме від розробки нових методів фармакокінетичної доставки – наприклад, нанокапсулювання, ліпосомальних систем або гідрогелевих матриць, що дозволяють забезпечити тривале та контрольоване вивільнення молекули в організмі. У поєднанні з високоточними біомаркерами для оцінки відповіді на терапію це створить умови для включення CBGM у протоколи персоналізованої медицини.
Для забезпечення клінічної перспективи необхідною умовою залишається перегляд законодавчих підходів – впровадження молекулярно орієнтованої класифікації речовин та створення винятків для похідних канабіноїдів, які не мають психоактивної дії. Наукові організації та міжнародні медичні агентства повинні виступити ініціаторами створення нових категорій біоактивних субстанцій, які потребують окремого правового регулювання – на зразок біопрепаратів, мікробіом-терапії чи генної терапії. Це дозволить CBGM вийти за межі дослідницьких лабораторій та стати повноцінним компонентом майбутньої терапевтичної практики.
Висновок
Монометиловий ефір канабігеролу (CBGM) є перспективним фармакологічним агентом з унікальними структурними та функціональними властивостями серед малодосліджених фітоканабіноїдів. Його селективна біоактивність, метаболічна стабільність та потенціал до впливу на широкий спектр рецепторних мішеней, включно з CB1, CB2, TRPV1 і PPARγ, відрізняють цю сполуку від класичних канабіноїдів, водночас демонструючи переваги в безпечності та мінімізації психоактивності.
Результати фармакокінетичних і токсикологічних досліджень показують високий потенціал CBGM для подальшої розробки у сфері нейропротекції, протизапальної терапії, онкології та автоімунних станів. Порівняно з іншими канабіноїдами, CBGM демонструє вищу стабільність до ферментативного метаболізму, а також більш прогнозовану фармакодинаміку, що відкриває можливості для його фармацевтичного стандартизування.
Втім, впровадження CBGM в клінічну практику стримується правовими, соціальними та технологічними бар’єрами. Відсутність міжнародної нормативної гармонізації щодо обігу нових канабіноїдів, висока собівартість синтезу та обмежене розуміння механізмів його дії є ключовими викликами. Також бракує масштабних клінічних випробувань із залученням різних популяцій хворих, що наразі не дозволяє зробити остаточні висновки щодо довготривалої безпеки та оптимальних терапевтичних дозувань.
Подальші дослідження повинні бути зосереджені на розробці біодоступних форм CBGM, створенні стандартизованих протоколів його синтезу, дослідженні метаболітів з високою афінністю до терапевтично значущих мішеней, а також на аналізі фармакогенетичних аспектів, які можуть впливати на індивідуальну реакцію пацієнтів. Перспективним також є використання CBGM як платформи для створення нових дериватів із заданим профілем дії.
Таким чином, CBGM заслуговує на систематичне дослідження в межах пріоритетних напрямів молекулярної фармакології та медицини персоналізованих підходів.
Джерела:
- National Center for Biotechnology Information (NCBI) – огляди щодо фармакології канабіноїдів, включно з менш вивченими сполуками
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7755015/ - U.S. Food and Drug Administration (FDA) – фармакокінетика та токсикологія рослинних препаратів, включаючи канабіноїди
https://www.fda.gov/media/131878/download - Oregon Health Authority – Health Evidence Review Commission – аналітика про ефективність та економічну доцільність медичних препаратів на основі канабіноїдів
https://www.oregon.gov/oha/HPA/DSI-HERC/MeetingDocuments/HERC-Materials-1-14-2016.pdf - Augusta University – Center for Biotechnology & Genomic Medicine – дослідження CBGM як частини фармакогеноміки та протизапальних механізмів
https://www.augusta.edu/centers/cbgm/ - PubChem – NIH Database (CBGM record) – структурна та фармакологічна інформація про CBGM
https://pubchem.ncbi.nlm.nih.gov/compound/CBGM - Drug Enforcement Administration (DEA) – Drug Scheduling & Legal Frameworks – законодавчі обмеження щодо використання похідних канабісу
https://www.deadiversion.usdoj.gov/schedules/ - U.S. National Library of Medicine – ClinicalTrials.gov – база даних клінічних досліджень, де можна знайти активні або завершені випробування за участі фітоканабіноїдів
https://clinicaltrials.gov/